46ху что это кариотип
Расшифровка анализа на кариотипирование
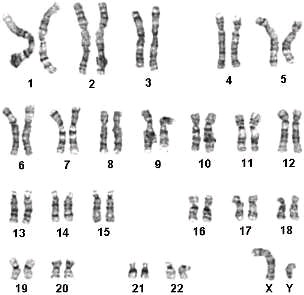
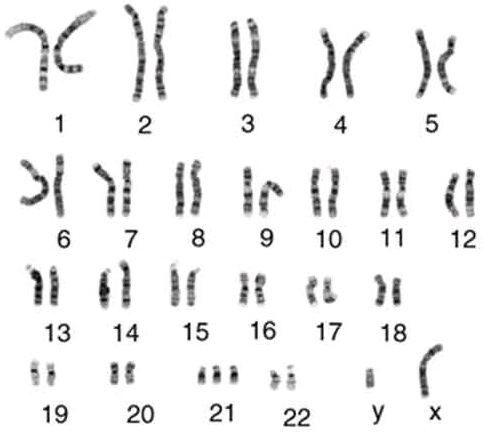
Нормальный кариотип человека содержит 46 хромосом: 22 пары аутосом и 1 пару половых хромосом – ХХ у женщин и ХY у мужчин. Нарушение этой генетической структуры является причиной наследственных болезней, бесплодия и самопроизвольного прерывания беременности.
Плохой результат кариотипирования выглядит как:
Что значит изменение количества хромосом в кариотипе
Аномалии кариотипа приводят к порокам развития плода, поэтому такие беременности в 50-60% случаев заканчиваются выкидышем в 1 триместре. Избыток генетического материала – причина трисомий 13 (47ХХ или ХY, 13+), 18 (47ХХ или XY, 18+) и синдрома Дауна (47ХХ или ХY, 21+).
Потеря участка короткого плеча пятой хромосомы (46ХХ или ХY,5р-) вызывает синдром кошачьего крика, такой же дефект длинного плеча пятнадцатой хромосомы (46ХХ или ХY, del15q11-q13) – болезнь Прадера Вилли, признаками которой являются низкие тонус мышц и плотность костей, задержка психического и речевого развития, гипогонадизм.
Нарушения кариотипа, связанные с гоносомами, имеют менее выраженные патологические проявления: их носители могут отличаться только высоким ростом и чуть сниженным интеллектом.
Таблица расшифровки аномалий половых хромосом
| Кариотип | Заболевания |
|---|---|
| 45ХО | Синдром Шерешевского-Тернера, встречается только у женщин (1:2000 случаев). Для синдрома Тернера характерны бесплодие, рост на 20-30 см ниже среднего, короткая шея, низкое положение ушных раковин. |
| 47ХХХ | Синдром трисомии-Х, чаще всего определяется случайно, при профилактическом обследовании. Это здоровые внешне женщины с генетической склонностью к невынашиванию беременности и хромосомным аномалиям у потомков. |
| 47ХYY | Синдром полисомии-Y встречается у мужчин высокого роста (1:1000 случаев), способных зачать ребенка. Для носителей полисомии-Y характерны сниженный интеллект и склонность к агрессии. |
| 47ХХY | Синдром Клайнфельтера – мужская патология (1:500 случаев), может проявляться в виде азооспермии, отсутствия сперматозоидов в эякуляте и бесплодия. |
Результаты кариотипирования помогут доктору выбрать тактику ведения бесплодной пары или пациентки с привычным невынашиванием беременности, а также оценить шансы супругов на здоровое потомство.
Также в МЖЦ у вас есть возможность сдать биоматериал (кровь или слюну) для детального ХМА-анализа, диагностирующего более 1000 генетических синдромов и болезней, связанных с аберрациями.
Кариотипирование супругов. Анализ на кариотип
Кариотип и кариотипирование супругов
Кариотипирование супругов – это углубленное лабораторное обследование для выявления изменений кариотипа, которое сдает пара в тех случаях, когда необходимо понять причину бесплодия, невынашивания беременности, а также заранее исключить генетические проблемы перед протоколом ЭКО и планированием беременности.
Кариотип – хромосомный набор человека с совокупностью признаков. Генетический фактор занимает достаточно большой процент среди супружеских пар с бесплодием, невынашиванием беременности, а также в группах мужчин с тяжелым нарушением сперматогенеза.
Анализ на кариотип сдают один раз в жизни. Поскольку это важный генетический анализ, то рекомендуется сдавать в специализированных центрах. В нашей лаборатории кариотипирование проводят высококвалифицированные лабораторные генетики. Анализируется материал всех 23 пар хромосом. Результат выдается согласно международной цитогенетической номенклатуре.
В норме результаты кариотипа выглядят следующим образом:
46, XX – нормальный женский кариотип;
46, XY – нормальный мужской кариотип.
Изменения кариотипа могут представлять собой изменения количества хромосом (анеуплоидии) либо структуры хромосом (или аберрации: транслокации, инверсии и др.). Внешне здоровый человек может быть носителем хромосомных аномалий, которые могут являться причиной бесплодия, невынашивания беременности или рождения у супружеских пар детей с пороками развития.
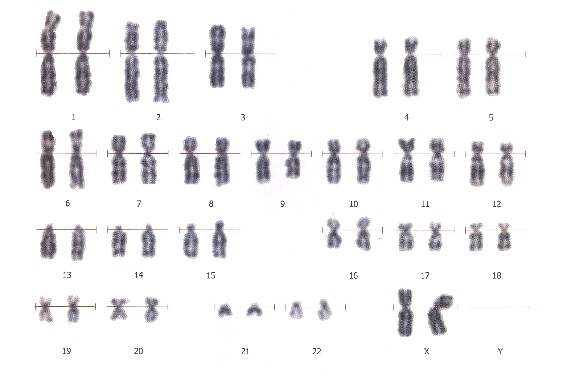
46, XX – нормальный женский кариотип 46, XY – нормальный мужской кариотип
46, XY, +21 – дополнительная хромосома 21 (синдром Дауна)
Классическим методом определения кариотипа является цитогенетический. Также этим методом выполняют кариотипирование супругов. Метод основан на культивировании клеток крови с последующим приготовлением и фотографированием препаратов окрашенных хромосом. Метод ХМА представляет собой современную молекулярную технологию исследования кариотипа и показан при задержке развития и роста человека, наличием врожденных пороков развития (ВПР) у детей, аутизме, подозрении на микроделеционные синдромы.
В Лаборатории ЦИР кариотипирование супругов проводят цитогенетическим методом:
Что такое аберрации?
Почему экспертного уровня?
Мы являемся одной из немногих клиник, работающих более 20 лет в области репродукции. В нашей лаборатории цитогенетики кариотипирование проводится специалистами высокого уровня, где идет просмотр каждой хромосомы.
Как сдать анализ на кариотип. Подготовка.
Смотрите также:
«Замершая» беременность: каковы причины? Какое значение имеет генетический фактор в развитии «замершей» беременности?
Анализ на кариотип (кариотипирование). Как интерпретировать анализ на кариотип? Отвечает Гузов И.И.
ГЕНЫ и БЕРЕМЕННОСТЬ. Генетические причины невынашивания беременности.
Мозаичность кариотипа
Выявление мозаицизма кариотипа зависит от процентного содержания его (если есть) в кариотипе и от выбранной методики анализа. Однозначно при ХМА более вероятно обнаружение мозаицизма в пределах разрешающей способности (наличие более 25% в кариотипе). Также можно обнаружить мозаицизм при наличии его в исследуемых клетках в Определении кариотипа с аберрациями цитогенетическим методом. В связи с ограничениями цитогенетического метода если процент мозаицизма мал, то, скорее всего, его можно не увидеть.
Хромосомный микроматричный анализ (ХМА)
Однако для диагностики ряда заболеваний, связанных с хромосомными аномалиями, существует более современная технология исследования кариотипа – хромосомный микроматричный анализ. Анализ на кариотип выполняется молекулярно-генетическим методом aCGH (микроматричная сравнительная геномная гибридизация), который в отличие от классического цитогенетического метода, имеет высокую разрешающую способность, позволяющую обнаружить более мелкие структурные изменения кариотипа.
Методы диагностики хромосомной патологии
46ху что это кариотип
Цитогенетическое исследование – кариотипирование – является основным методом диагностики хромосомных нарушений и проводится в целях выявления нарушений количества и структуры хромосом. Используется для пренатальной диагностики.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Кариотипирование – цитогенетическое исследование, изучение хромосомного набора человека, позволяющее обнаружить отклонения в структуре и числе хромосом. Оно помогает выявить нарушения хромосом, вероятно, не влияющие на здоровье человека, но тем не менее важные для планирования будущей беременности и для здоровья будущего ребенка (патологии плода, аномалии развития).
Кариотип – это полный хромосомный набор клетки человека. В норме он состоит из 46 хромосом, из них 44 аутосомы (22 пары), имеющих одинаковое строение и в мужском, и в женском организме, и одна пара половых хромосом (XY у мужчин и XX у женщин). Каждая хромосома несет гены, ответственные за наследственность. Кариотип 46, ХХ – соответствует нормальному женскому кариотипу, а кариотип 46, XY – это нормальный мужской кариотип. Кариотип остается неизменным в течение всей жизни.
Нарушения хромосомного набора могут являться причиной наследственной патологии, бесплодия, невынашивания беременности, рождения ребенка с различными пороками развития.
Для цитогенетического исследования хромосом чаще всего используют препараты кратковременной культуры крови, реже клетки костного мозга и культуры фибробластов.
Кариотипирование культуры лимфоцитов периферической крови человека – сложное многоступенчатое цитогенетическое исследование, проводится, когда клетки входят в фазу митоза – непрямого деления с тождественным распределением генетического материала между дочерними клетками. Оно включает в себя следующие этапы:
Различают несколько видов нарушений структуры хромосом:
Хромосомные нарушенияразличаются также по принципу регулярности. Регулярные мутации присутствуют при делении каждой клетки или большинства клеток. Они проявляются в момент зачатия плода либо в первые несколько дней беременности. Нерегулярные аберрации появляются в результате негативного воздействия радиации, химических средств и т.д.
Нарушение расхождения хромосом может произойти во время клеточного деления (мейоза). Если такое нарушение происходит в процессе образования сперматозоидов или яйцеклеток, то в половой клетке появляется лишняя хромосома, которая при зачатии будет передана ребенку. В результате она будет присутствовать во всех клетках организма ребенка. Примером трисомии может служить синдром Дауна (лишняя 21-я хромосома) или синдром Патау (трисомия 13-й хромосомы). Также нарушение расхождения хромосом может произойти при первых делениях оплодотворенной яйцеклетки. Например, утрата Х-хромосомы приводит к развитию Х0-синдрома, или синдрома Шерешевского – Тернера. Аномалии, связанные с нарушением расхождения хромосом, встречаются не так часто, поэтому вероятность их повторения в одной и той же семье достаточно мала.
Структурные же нарушения хромосом передаются по наследству, при этом степень семейного риска и дальнейшая передача дефекта от поколения к поколению становится значительно высокой.
Кариотипирование также рекомендуют проводить в тех семьях, где есть высокая вероятность рождения ребенка с болезнью, сцепленной с Х-хромосомой.
Когда назначается исследование?
Показания для кариотипирования супружеских пар:
Показания для кариотипирования детей:
Что означают результаты?
Для мужчин нормальным считается кариотип 46,XY. Это означает, что определено 46 нормальных хромосом, в том числе X и Y хромосома.
Для женщин нормальным считается кариотип 46,XX. Это означает, что определено 46 нормальных хромосом, в том числе две X хромосомы.
В случае выявления патологического кариотипа, необходима консультация медицинского генетика по результатам исследования для правильной его интерпретации.
Синдром Клайнфельтера: мужчина с женской хромосомой
Елена Шведкина об одном из самых распространенных генетических заболеваний — больные жалуются на бесплодие, эректильную дисфункцию, гинекомастию и остеопороз
Синдром Клайнфельтера — генетическое заболевание, характеризующееся дополнительной женской половой хромосомой Х (одной или даже несколькими) в мужском кариотипе ХY. При этом в мужских половых железах — яичках — образуется недостаточно половых гормонов.
Классификация: виды кариотипов при синдроме Клайнфельтера
По количеству дополнительных Х-хромосом различают следующие варианты синдрома Клайнфельтера:
Кроме того, к синдрому Клайнфельтера также относят мужские кариотипы, включающие, помимо дополнительных Х-хромосом, дополнительную Y-хромосому — 48,ХХYY. И, наконец, среди пациентов с этим синдромом встречаются лица с мозаичным кариотипом 46,ХY/47,ХХY (то есть часть клеток имеет нормальный хромосомный набор).
История открытия синдрома
Синдром получил свое название в честь Гарри Клайнфельтера — врача, в 1942 году впервые описавшего клиническую картину болезни. Клайнфельтер с коллегами опубликовали отчет об обследовании 9 мужчин, объединенных общими симптомами, такими как слабое оволосение тела, евнухоидный тип телосложения, высокий рост и уменьшенные в размерах яички. Позднее, в 1956 г., генетики Планкетт и Барр (Е. R. Plankett, М. L. Barr) обнаружили у мужчин с синдромом Клайнфельтера тельца полового хроматина в ядрах клеток слизистой оболочки полости рта, а в 1959 году Полани и Форд (P. E. Polanyi, S. E. Ford) с сотрудниками показали, что у больных в хромосомном наборе имеется лишняя Х-хромосома.
Активные исследования данной патологии велись в 70‑х годах в США. Тогда всех новорожденных мальчиков подвергали кариотипированию, в результате чего удалось достоверно выявить распространенность и генетические особенности синдрома Клайнфельтера.
Распространенность заболевания
Синдром Клайнфельтера является одним из наиболее распространенных генетических заболеваний: на каждые 500 новорождённых мальчиков приходится 1 ребёнок с данной патологией.
Кроме того, синдром Клайнфельтера — третья по распространенности эндокринная патология у мужчин (после сахарного диабета и патологии щитовидной железы) и наиболее частая причина врожденного нарушения репродуктивной функции у мужчин.
Этиология и причины нарушения
Синдром Клайнфельтера относится к генетическим заболеваниям, не передающимся по наследству, поскольку больные, за редким исключением, бесплодны. Патология, как правило, возникает в результате нарушения расхождения хромосом на ранних стадиях формирования яйцеклеток и сперматозоидов. При этом синдром Клайнфельтера, возникающий за счет нарушения в женских половых клетках, встречается в три раза чаще. Мозаичные формы обусловлены патологией деления клеток на ранних стадиях эмбриогенеза, поэтому часть клеток у таких пациентов имеет нормальный кариотип. Причины нерасхождения половых хромосом и нарушения деления клеток на самых ранних стадиях эмбриогенеза до сих пор малоизучены. В отличие от других хромосомных заболеваний, влияние возраста родителей отсутствует или выражено незначительно.
Ранние признаки
В отличие от большинства заболеваний, связанных с нарушением количества хромосом, внутриутробное развитие детей с синдромом Клайнфельтера проходит нормально, склонности к преждевременному прерыванию беременности не наблюдается. Так что в младенческом и раннем детском возрасте заподозрить патологию практически невозможно. Более того, клинические признаки классического синдрома Клайнфельтера проявляются, как правило, только в подростковом периоде. Однако есть симптомы, которые позволяют заподозрить наличие синдрома Клайнфельтера в препубертатном периоде:
У части пациентов наблюдается некоторая задержка в развитии речи.
В подростковом возрасте синдром часто проявляется гинекомастией, которая при данной патологии имеет вид двустороннего симметричного безболезненного увеличения грудных желез. Так как такого рода гинекомастия часто наблюдается у совершенно здоровых подростков, этот симптом часто остается без внимания. В норме подростковая гинекомастия бесследно исчезает в течение нескольких лет, у пациентов же с синдромом Клайнфельтера обратной инволюции грудных желез не происходит. В некоторых случаях гинекомастия может не развиваться вовсе, и тогда патология проявляется признаками андрогенной недостаточности уже в постпубертатный период.
Симптомы андрогенной недостаточности при синдроме Клайнфельтера
Андрогенная недостаточность при синдроме Клайнфельтера связана с постепенной атрофией яичек, что приводит к снижению синтеза тестостерона. Степень недостаточности андрогенов резко варьирует.
В первую очередь обращают на себя внимание внешние признаки гипогонадизма:
Поскольку дегенерация половых желез, как правило, развивается в постпубертатный период, у большинства пациентов размеры мужских половых органов, за исключением яичек, соответствуют возрастным нормам.
Пациенты могут жаловаться на ослабление либидо и снижение потенции. У многих мужчин с синдромом Клайнфельтера половое влечение вовсе не возникает, а некоторые — напротив, заводят семью и живут нормальной половой жизнью. Наиболее постоянный признак патологии — бесплодие, именно оно чаще всего становится причиной обращения таких пациентов к врачу. У 10 % мужчин с азооспемией обнаруживают синдром Клайнфельтера.
Недостаток андрогенов приводит к развитию остеопороза, анемии и слабости скелетной мускулатуры. У трети больных можно наблюдать варикозное расширение вен голеней.
Андрогены влияют на обмен веществ, поэтому больные с синдромом Клайнфельтера склонны к ожирению, нарушению толерантности к глюкозе и сахарному диабету второго типа.
Доказана предрасположенность таких пациентов к аутоиммунным заболеваниям (ревматоидный артрит, системная красная волчанка, аутоиммунные заболевания щитовидной железы и другие).
Психологические особенности
Коэффициент интеллекта у больных с классическим синдромом Клайнфельтера варьирует от значений ниже среднего до показателей, значительно превышающих средний уровень. Однако во всех случаях отмечается диспропорция между общим уровнем интеллекта и вербальными способностями, так что нередко пациенты с достаточно высоким IQ испытывают трудности при восприятии больших объемов материала на слух, а также при построении фраз, содержащих сложные грамматические конструкции. Такие особенности причиняют пациентам много неприятностей в период обучения и нередко продолжают сказываться на профессиональной деятельности.
Данные о психологических особенностях больных с синдромом Клайнфельтера достаточно противоречивы, однако большинство специалистов оценивают пациентов как скромных, робких людей с несколько заниженной самооценкой и повышенной чувствительностью. Есть данные, свидетельствующие о склонности пациентов с синдромом Клайнфельтера к гомосексуализму, алкоголизму и наркомании. Сложно сказать, вызваны ли особенности психики у таких больных непосредственным влиянием хромосомной аномалии, или же это реакция на проблемы в сексуальной сфере.
В отношении разных цитогенетических вариантов синдрома Клайнфельтера справедливо правило, что с увеличением количества дополнительных Х-хромосом увеличивается количество и выраженность патологических симптомов.
Диагностика синдрома Клайнфельтера
Во многих странах синдром Клайнфельтера часто диагностируется ещё до рождения ребёнка, так как многие женщины позднего детородного возраста, в связи с высоким риском генетических дефектов у будущего потомства, используют пренатальную генетическую диагностику плода. Нередко пренатальное выявление синдрома Клайнфельтера является поводом для прерывания беременности, в том числе и по рекомендации врачей. В России анализ кариотипа будущего ребёнка проводится крайне редко.
При подозрении на синдром Клайнфельтера проводят лабораторный анализ крови для определения уровня мужских половых гормонов. Необходима дифференциальная диагностика с другими заболеваниями, протекающими с проявлениями андрогенной недостаточности. Точный диагноз синдрома Клайнфельтера ставят на основании изучения кариотипа (набора хромосом) больного.
Исследования, необходимые для подтверждения диагноза
47,ХХY (80 % случаев)
48,ХХYY
48,ХХХY
49,ХХХХY
46,ХY/47,ХХY
46ху что это кариотип
ФГБУ Эндокринологический научный центр Минздравсоцразвития Российской Федерации
ФГБУ «Эндокринологический научный центр» МЗ РФ, Москва
ФГБУ «Эндокринологический научный центр» Минздрава РФ, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития Российской Федерации, Москва
ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, Москва, Россия
ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, Москва, Россия
Институт детской эндокринологии Эндокринологического научного центра, Москва
Эндокринологический научный центр, Москва
Нарушение формирования пола 46,XY, ассоциированное с мутациями в гене MAP3K1. Описание клинических случаев
Журнал: Проблемы эндокринологии. 2018;64(1): 45-49
ФГБУ Эндокринологический научный центр Минздравсоцразвития Российской Федерации
Причинами нарушения формирования пола (НФП) 46,XY могут быть мутации ряда генов, вовлеченных в процесс дифференцировки гонад. XY-инверсия пола может являться также следствием нарушений на уровне гена митоген-активированной протеинкиназы (MAPK) киназы киназы 1 (MAP3K1) и MAPK-сигнального пути. В последнее десятилетие было доказано участие MAPK-пути в инициации экспрессии гена SRY при формировании мужского гонадного пола у млекопитающих. Роль MAPK-сигнального пути в формировании пола у людей изучена недостаточно. Вероятно, MAP3K1 и MAPK-сигнальный путь являются одним из генетических путей, контролирующих нормальное развитие яичек. В настоящее время в литературе описано несколько семей и спорадических случаев НФП 46,XY вследствие мутаций в гене MAP3K1. Клиническая картина НФП у этих пациентов различна и варьирует от женского фенотипа с правильным строением наружных гениталий до мужского фенотипа с гипоспадией. Мы приводим описания редких клинических случаев нарушений формирования пола 46,XY (семейный случай НФП у единоутробных сестер и спорадический случай) с не описанными ранее мутациями в гене MAP3K1. В статье также кратко анализируется литература по данной патологии.
ФГБУ Эндокринологический научный центр Минздравсоцразвития Российской Федерации
ФГБУ «Эндокринологический научный центр» МЗ РФ, Москва
ФГБУ «Эндокринологический научный центр» Минздрава РФ, Москва
ФГУ Эндокринологический научный центр Минздравсоцразвития Российской Федерации, Москва
ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, Москва, Россия
ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России, Москва, Россия
Институт детской эндокринологии Эндокринологического научного центра, Москва
Эндокринологический научный центр, Москва
Нарушения формирования пола (НФП) — группа врожденных патологий, сопровождающихся атипичным развитием хромосомного, гонадного и анатомического пола [1]. Формирование мужского пола определяется в первую очередь экспрессией гена SRY на Y-хромосоме, способствующего развитию недифференцированных гонад в тестикулы [2]. Наряду с геном SRY идентифицирован ряд генов и сигнальных путей, участвующих в детерминировании пола и ассоциированных с широким фенотипическим спектром НФП [3]. В недавних исследованиях были выявлены мутации в гене митоген-активированной протеинкиназы (MAPK) киназы киназы 1 (MAP3K1, также известном как MEKK1), которые были связаны с нарушением формирования пола 46, XY [4, 5]. Роль сигнального пути MAPK в определении пола у людей не изучена. Вероятно, MAP3K1 и MAPK-сигнальный путь является одним из генетических путей, контролирующих нормальное развитие яичек. В настоящее время в литературе описано несколько семейных и спорадических случаев НФП 46, XY, обусловленных мутациями в данном гене [4, 5]. Известные случаи НФП 46, XY, ассоциированные с геном MAP3K1, отличаются различной клинической картиной, варьирующей от женского фенотипа с правильным строением наружных гениталий до мужского фенотипа с микропенисом и гипоспадией различной степени.
Клинический случай № 1
Пациентка О. при рождении была зарегистрирована в женском поле и воспитывалась как девочка. По данным медицинской документации, при первичном патронаже была выявлена гипертрофия клитора, однако обследование не проводилось, к эндокринологу не обращались. У пациентки отмечался спонтанный поздний пубертат с нарушенным порядком появления вторичных половых признаков (адренархе в 14 лет, телархе в 17 лет), первичная аменорея. Впервые была обследована по месту жительства в возрасте 16 лет. Был выявлен гипергонадотропный гипогонадизм (ЛГ 23,4 мМе/мл, ФСГ 99,1 мМЕ/мл), кариотип 46, XY.
Девочка была госпитализирована в детское отделение ФГБУ ЭНЦ в возрасте 17 лет. При объективном осмотре отмечался нормальный рост (164,3 см, SDS роста +0,35), половое созревание соответствовало стадии II по Таннеру (В2Р2). Наружные половые органы были сформированы неправильно [клитор гипертрофирован (2,5—3 см) с головкой, слабо развитые кавернозные тела, меатус у основания клитора, скротолабиальный шов расщеплен, вход во влагалище сужен]. Отмечались высокий уровень гонадотропинов [ЛГ 88 Ед/л (2,6—12), ФСГ 104 Ед/л (1,9—11,7)], эстрадиола [70 пмоль/л (97—592)], тестостерона [3,11 нмоль/л (0,1—2,7)]. Показатели дигидроэпиандростендиона-сульфата (ДГЭА-С) и 17-гидроксипрогестерона (17-ОНП) находились в пределах референсных значений [7,52 мкмоль/л (0,92—7,6) и 3,6 нмоль/л (0,1—7,0) соответственно]. При МРТ органов малого таза определялись матка в виде тяжа 2,3×0,9 см и гонады (справа 2×1 см, слева 0,7×1,4 см). Был установлен диагноз: нарушение формирования пола 46, ХУ и рекомендована диагностическая лапароскопия, при которой в малом тазу были обнаружены гипоплазированная двурогая матка, две маточные трубы, дисгенетичные гонады с обеих сторон. При морфологическом исследовании операционного материала в ФГБУ ЭНЦ была верифицирована двусторонняя гонадобластома. При повторном исследовании гистологических препаратов в ФНКЦ ДГОИ им. Д. Рогачева была подтверждена двусторонняя гонадобластома с трансформацией в дисгерминому с правой стороны. Девочка была консультирована онкологом. Учитывая данные КТ органов грудной клетки (очаговых и инфильтративных изменений не выявлено), гистологический тип опухоли и стадию заболевания, химиотерапия не назначалась. Рекомендована непрерывная заместительная терапия женскими половыми гормонами. В последующем проведена феминизирующая пластика наружных гениталий.
Пациентка Б., 13,5 года, единоутробная сестра пациентки О., была обследована в связи с отсутствием спонтанного пубертата и диагностированием НФП 46, XY у старшей сестры (см. рисунок). 
При рождении отмечалось правильное строение наружных гениталий. По данным обследования, проведенного в возрасте 13 лет, был также определен кариотип 46, XY, при УЗИ органов малого таза — аплазия матки и яичников. При клиническом осмотре рост девочки составил 155,9 см (SDS роста = –0,64), половой статус соответствовал стадии I по Таннеру. Наружные половые органы были сформированы по женскому типу. Лабораторно был подтвержден гипергонадотропный гипогонадизм [ЛГ 39,9 Ед/л (2,6—12), ФСГ 137 Ед/л (1,9—11,7), эстрадиола 43,3 пмоль/л (97—592)], отмечался нормальный уровень тестостерона [0,6 нмоль/л (0,1—2,7)]. При МРТ органов малого таза была выявлена матка в виде тяжа, гонады не визуализировались. При диагностической лапароскопии в малом тазу обнаружена гипоплазированная матка, две маточные трубы, гонады в виде стреков. Морфологическое исследование операционного материала верифицировало дисгенезию гонад по овотестикулярному типу.
Обеим пациенткам было проведено молекулярно-генетическое исследование методом высокопроизводительного параллельного секвенирования с использованием разработанной в ФГБУ ЭНЦ панели олигонуклеотидов, предназначенной для анализа 45 генов, ассоциированных с различными формами нарушения формирования пола. У обеих девочек была выявлена гетерозиготная мутация p. C691R в гене MAP3K1. Данная мутация не была прежде описана. У матери пациенток молекулярно-генетическое исследование на данный момент не проведено. Однако учитывая наличие идентичной гетерозиготной мутации MAP3K1 у единоутробных сестер, зачатых от разных отцов, можно сделать вывод, что данная миссенс мутация была унаследована от матери и, вероятно, послужила причиной НФП 46, XY.
Клинический случай № 2
У пациента М. при рождении отмечалось неправильное строение наружных половых органов. При обследовании по месту жительства был определен кариотип 46, ХУ. В гормональном профиле в возрасте 8,5 мес отмечался незначительно повышенный уровень ФСГ (5,28 мМЕ/мл), низкие показатели тестостерона, ЛГ и 17-ОНП. При УЗИ яички лоцировались в мошонке (справа 0,75×0,52 см, слева 0,87×0,59 см). При К.Т. малого таза предстательная железа и семенные пузырьки не визуализировались.
Ребенок впервые был обследован в ФГБУ ЭНЦ в возрасте 11 мес. При осмотре обращало на себя внимание неправильное строение наружных гениталий [яички пальпировались в расщепленной мошонке, искривленный половой член длиной около 3 см, кавернозные тела плотные, головка полового члена сформирована, по дорсальной поверхности — рассекающая борозда полового члена; узкий урогенитальный синус, открывающийся на мошонке (мошоночная форма гипоспадии); половой член за счет искривления утоплен в мошонке]. Отмечались: незначительное повышение уровня ФСГ [3,8 Ед/л (0—2)], низкие показатели тестостерона [(0,17 нмоль/л (0,3—0,6)], ЛГ [0,2 Ед/л (0—1,5) и антимюллерова гормона [12,8 нг/мл (63—132)]. При мультистероидном анализе крови данных за нарушение стероидогенеза не получено. При пробе с хорионическим гонадотропином (4 инъекции по 1000 МЕ) отмечалось повышение уровня тестостерона до 5,7 нмоль/л, что свидетельствовало о нормальном функционировании клеток Лейдига. Ребенку был установлен диагноз: НФП 46, XY, в дальнейшем были проведены пластические операции по устранению искривления полового члена и гипоспадии. При молекулярно-генетическом исследовании (панель генов «нарушение формирования пола») выявлена гетерозиготная мутация с.2858 2872del CAАCААCААCААCАА р.944 948del в гене MAР3К1. Данная мутация также не была ранее описана. Планируется проведение молекулярно-генетического исследования гена MAР3К1 с целью поиска аналогичной делеции.
Обсуждение
MAPK активируются посредством эволюционно консервативного трехкомпонентного сигнального каскада, состоящего из митоген-активированной протеинкиназы киназы киназы-1 (MAP3K1), MAP2K и MAPK [3]. MAPK-сигнальные пути являются ключевыми путями регуляции клеточной пролиферации и дифференцировки [6, 7]. Нарушения в регуляции MAPK-каскада способствуют развитию ряда онкологических заболеваний [8]. Относительно недавно была выявлена ассоциация MAP3K1 с нарушением формирования пола 46, XY, однако роль MAPK-сигнального пути в развитии данной патологии у людей до сих пор не изучена. Экспрессия MAP3K1 наблюдается в эмбриональной гонаде мышей на 11-й день после зачатия, что соответствует стадии формирования гонад, а также на 13-й день после зачатия в канальцах яичек [4]. Роль MAPK-пути в определении пола у млекопитающих была определена посредством идентификации мутаций гена MAP3K4 у мышей, у которых инверсия пола предположительно связана с неспособностью активировать экспрессию гена SRY [9, 10]. Показано, что при отсутствии двух изоформ митоген-активированной протеинкиназы киназы киназы-1 (p38a и p38b) формируется инверсия пола XY, которая также обусловлена нарушениями на уровне экспресии SRY [11]. Таким образом, имеющиеся в литературе данные свидетельствуют об участии MAPK-пути в инициации соответствующей экспрессии SRY при формировании мужского гонадного пола у млекопитающих. У людей взаимосвязь между мутациями в гене MAP3K1 и нарушением формирования пола 46, XY была впервые прослежена при анализе сцепления генов на длинном плече 5 хромосомы у пациентов с НФП из двух семейств и в 11 спорадических случаях [4]. Было идентифицировано 6 мутаций в гене MAP3K1 и проведен их функциональный анализ. Клинические проявления в описанных случаях были различны, начиная от полностью женского фенотипа без вирилизации наружных гениталий до мужчин с микропенисом и/или с гипоспадией. Различный фенотип при одной и той же мутации отмечался и среди пациентов в пределах одной семьи. В другом исследовании у 4 пациентов с НФП 46, XY, преимущественно с мужским фенотипом и разной степенью нарушения развития наружных гениталий, были также выявлены мутации в гене MAP3K1 [5]. При сопоставлении генотипа и фенотипа при одной из идентифицированных миссенс-мутаций было установлено, что у всех пациентов с этой мутацией отмечался мужской фенотип с гипоспадией. Данная миссенс-мутация также ассоциирована с бронхиальной астмой [12]; аномалии развития наружных гениталий ранее не были описаны. Таким образом, ее значимость остается неизвестной.
Интересно, что у нокаутных по MAP3K1 мышей не наблюдается реверсии пола [13, 14]. Эти животные остаются жизнеспособными с сохранной репродуктивной функцией, но со сниженным количеством клеток Лейдига и увеличенной длиной эмбриональных гонад. Поэтому авторы предположили, что MAP3K1 не играет существенной роли при формировании тестикулов у мышей. Это может свидетельствовать о том, что сигнальные пути MAP-киназы у человека и мыши не идентичны [3]. На сегодняшний день роль MAP3K1 в определении пола у людей остается малоизученной. Фенотип полной дисгенезии гонад 46, XY аналогичен фенотипу при мутациях в гене SRY, т. е. мутации MAP3K1 могли бы влиять на ранние стадии формирования яичек.
У наших пациентов с НФП 46, XY при молекулярно-генетическом исследовании на панели, которая включала 45 генов, ассоциированных с различными формами нарушения формирования пола, мутации были найдены только в гене MAP3K1. В описанных нами случаях у пациентов с идентифицированными мутациями в гене MAР3К1 отмечалась различная клиническая картина НФП 46, XY, характеризующаяся разной степенью дифференцировки гонад и формирования наружных гениталий. В первой представленной нами семье предполагается наследование гетерозиготной мутации от матери, что характерно для семей с НФП 46, XY вследствие мутаций гена MAP3K1 [4]. Выявленные гетерозиготные мутации прежде в литературе не были описаны. С целью подтверждения их патологической значимости планируется проведение молекулярно-генетического исследования родителям пациентов.
Заключение
Причиной нарушения формирования пола 46, XY может служить патология целого ряда генов, вовлеченных в процесс дифференцировки гонад. Участие гена MAP3K1 и MAP-киназного сигнального пути в развитии НФП было установлено относительно недавно и в настоящее время недостаточно изучено. Клинические проявления у пациентов с 46, XY НФП, предположительно обусловленных мутациями в гене MAP3K1, отличаются выраженной гетерогенностью. Данных о значимой корреляции генотипических и фенотипических особенностей в литературе нет. Учитывая вероятность вовлечения MAP3K1 и MAPK-сигнального пути в процесс нормального развития яичек, необходимо дальнейшее изучение патологической значимости мутаций данного гена в развитии различной клинической картины НФП 46, XY.
Источники финансирования. Молекулярно-генетическое исследование на панель генов «нарушение формирования пола» выполнено при содействии Фонда поддержки и развития филантропии «КАФ». Авторы декларируют отсутствие иных явных и потенциальных конфликтов интересов, о которых необходимо сообщить.
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи. Получены письменные информированные согласия пациентов на публикацию представленных медицинских данных в этом журнале.