Сальник в брюшной полости у женщин что
Перитонеальный канцероматоз
Перитонеальный канцероматоз
Вам поставили диагноз: перитонеальный канцероматоз (опухоль брюшины)
Предлагаем Вашему вниманию краткий, но очень подробный обзор перитонеального канцероматоза.
Филиалы и отделения, где лечат перитонеальный канцероматоз
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Национальный центр лечения больных канцероматозом
МНИОИ имени П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России
Руководитель Центра к.м.н. Владимир Михайлович Хомяков – 8 495 150 11 22
Введение
Причины возникновения перитонеального канцероматоза
Развитие перитонеального канцероматоза является поэтапным процессом. Первый этап – распространение опухолевых клеток из первичного очага поражения. Это связано с нарушением межклеточного взаимодействия и приобретением клетками опухоли подвижности. При этом эпителиальные клетки меняют фенотип на мезенхимальный, происходит деградация межклеточного матрикса. Распространение опухолевых клеток может происходить в ходе оперативного вмешательства. Их механическое отделение возможно при повреждении лимфатических или кровеносных сосудов. Попавшие в брюшную полость клетки опухоли мигрируют под действием силы тяжести, сокращений внутренних органов, имплантируются в местах повышенной резорбции: большом сальнике, в области слепой кишки, дугласовых карманах.
На втором этапе опухолевые клетки взаимодействуют с мезотелием брюшины. Механизмы адгезии определяются природой клеток, особенностями морфологии брюшины, а также наличием участков ее повреждения. Далее клетки закрепляются в мезотелии, происходит их горизонтальное распространение по поверхности перитонеума, а затем инвазивный рост – прорастание в базальную мембрану, соединительную ткань. Следующим этапом является стимуляция неоангиогенеза – обязательного фактора развития опухоли. Морфопатогенетические механизмы формирования канцероматоза брюшины еще недостаточно изучены, в связи с чем отсутствуют радикальные методы лечения.
Частота развития канцероматоза брюшины зависит не только от первичной локализации опухоли, но и от ее размеров, глубины инвазии, гистотипа, степени дифференцировки (недифференцированный рак желудка осложняется поражением брюшины в 60% случаев, ограниченный – в 15%).
Классификация перитонельного канцероматоза
Единая классификация данного заболевания отсутствует, поскольку характеристики первичных опухолей, приводящих к поражению брюшины, весьма разнообразны. Наиболее распространена классификация перитонеального канцероматоза брюшины в зависимости от числа, локализации метастазов, которая предусматривает три степени:
Р1 – локальное поражение брюшины
Р2 – несколько областей канцероматоза, разделенных здоровыми участками брюшины
Р3 – многочисленные очаги поражения
Также используется метод определения индекса канцероматоза брюшины: суммируются баллы измерения максимальных очагов поражения (0-3 балла) в каждой из 13 наиболее вероятных областей поражения брюшины.
Симптомы перитонеального канцероматоза
Перитонеальный канцероматоз брюшины является вторичным поражением, поэтому его клиническая картина во многом определяется проявлениями первичной опухоли. Характерным признаком является обильный выпот в брюшную полость – формирование асцита. Зачастую асцитический синдром, развивающийся вследствие обструкции лимфатического дренажа, является единственным признаком заболевания, и пациенты могут поступать в отделение гастроэнтерологии или терапии для диагностики причин асцита. Состояние больных тяжелое, характерна значительная потеря веса. Неспецифическими признаками являются тошнота, рвота, выраженная слабость, утомляемость. При наличии крупных метастазов возможно их прощупывание через брюшную стенку.
Диагностика перитонеального канцероматоза
Перитонельный канцероматоз имеет неспецифическую клиническую картину, однако консультация гастроэнтеролога или онколога позволяет предположить данное заболевание на основании симптомов и физикальных данных. Лабораторные анализы не выявляют специфических изменений: определяется лейкоцитоз, ускорение СОЭ. Диагностическая программа обязательно должна включать УЗИ органов брюшной полости и малого таза, позволяющее обнаружить распространенное поражение, а также МСКТ брюшной полости с контрастированием. Обязательно проводится цитологическое исследование асцитической жидкости, полученной при лапароцентезе, которое дает возможность впервые установить или подтвердить диагноз, а также определить гистогенез клеток опухоли.
Информативным методом диагностики перитонеального канцероматоза является лапароскопия с осмотром перитонеума, дугласова пространства, диафрагмы, сопровождающаяся биопсией. Высокой специфичностью обладает обратнотранскриптазная полимеразная цепная реакция (ОТ-ПЦР), которая позволяет определить источник диссеминации даже при малом количестве опухолевых клеток.
Сложности диагностики возникают при наличии перитонеального канцероматоза без выявленного первичного очага. Данная форма заболевания, встречающаяся в 3-5 % случаев, проявляется клинически только при уже сформировавшемся поражении брюшины. При этом первичный очаг может иметь настолько малые размеры, что его прижизненное обнаружение невозможно.
В качестве дополнительных методов может использоваться определение онкомаркеров (кислой фосфатазы, раково-эмбрионального антигена, альфа-фетопротеина, бета-субъединицы ХГЧ). Такая диагностика не обладает высокой специфичностью, но применяется для оценки прогноза, раннего выявления диссеминации, рецидивов, а также для контроля эффективности лечения.
Лечение перитонеального канцероматоза
Хирургическое лечение канцероматоза включает удаление первичной опухоли с регионарными метастазами и отсевами по брюшине. Циторедуктивная операция выполняется в объеме перитонэктомии, может сочетаться с удалением матки и придатков, сигмовидной кишки, желчного пузыря. После проведения операции оценивается индекс полноты циторедукции: СС-0: после проведения хирургического лечения очаги поражения визуально не определяются; СС-1: имеются неудаленные очаги диаметром до 2,5 мм; СС-2: очаги диаметром 2,5 мм – 2,5 см; СС-3: очаги поражения более 2,5 см в диаметре. Однако даже при определении индекса СС-0 нельзя полностью исключить возможность диссеминации, поэтому обязательно проводится химиотерапия.
Эффективные подходы к лечению, как правило, подразумевают проведение комбинированной терапии, например, сочетания хирургического вмешательства и системной химиотерапии. Одним из наиболее эффективных методов является локальная химиотерапия. Идея локальной химиотерапии состоит в том, чтобы обеспечить доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Из-за крайне низкой проницаемости этой области для лекарственных препаратов, например, при внутривенном их введении или приеме в виде таблеток, доставка препаратов в виде аэрозоля под давлением углекислого газа даёт накопление препарата в опухоли в значительно больших концентрациях.
Методы лечения перитонеального канцероматоза
Длительное время канцероматоз брюшины и плевры считали терминальной стадией болезни, не подлежащей специальному лечению. Разработка методик непосредственного воздействия на брюшину и плевру позволила улучшить прогноз при этом состоянии. МНИОИ им. П.А. Герцена обладает уникальными возможностями лечения больных с канцероматозом, имея в арсенале весь комплекс новейших методов терапии.
Гипертермическая интраоперационная внутрибрюшная (внутриплевральная) химиотерапия (HITEC).
Это методика, при которой во время операции в брюшную или плевральную полость вводится подогретый до 42,5С, высококонцентрированный раствор химиотерапевтических препаратов, что обеспечивает их воздействие непосредственно на раковые клетки в брюшной (плевральной) полости при минимальном воздействии на другие органы. Сеанс проводится в течение часа, что позволяет разрушить опухолевые клетки, оставшиеся после так называемой циторедуктивной операции.
Внутрибрюшная (внутриплевральная) аэрозольная химиотерапия под давлением (PIРAC)
Это новейший инновационный метод лечения перитонеального канцероматоза, который обеспечивает доставку лекарственного препарата непосредственно к опухолевым клеткам, находящимся на внутренней выстилке анатомической полости. Метод совсем недавно появился в России. Процедуру проводят посредством лапароскопии (торакоскопии). В брюшной или плевральной полости под давлением углекислого газа распыляют аэрозоль химиопрепаратов и оставляют в течение 30 мин. При таком способе введения химиопрепаратов их воздействие на опухоль многократно возрастает при полном отсутствии системной токсичности. Ноу-хау МНИОИ имени П.А. Герцена в этом методе лечения стала разработка собственной специальной форсунки, которая формирует поток мелкодисперсного аэрозоля с размером капель от 1 до 40 мкм. Изделие выполнено из специализированных материалов и не уступает по качеству импортному аналогу, а по ряду технических характеристик его превосходит.
Преимущества лечения перитонеального канцероматоза в МНИОИ имени П.А. Герцена – филиале ФГБУ «НМИЦ радиологии» Минздрава России
Оментит
Оментит — воспалительное заболевание сальника, представляющего собой складку висцеральной брюшины. Болезнь проявляется острой разлитой болью в животе, тошнотой, лихорадкой, головной болью, рвотой. Пациенты принимают вынужденное полусогнутое положение, при разгибании туловища возникает резкая боль. Диагностика включает осмотр хирурга, проведение оментографии, КТ брюшной полости, диагностической лапароскопии. Лечение острой патологии хирургическое. Выполняют удаление сальника, ревизию брюшной полости и установку дренажа. При хроническом течении назначают антибактериальные и противовоспалительные препараты в сочетании с физиотерапией.
Общие сведения
Причины оментита
Исходя из этиологии воспалительного процесса, заболевание бывает первичным и вторичным. Первичный оментит формируется в результате травматического ранения, инфекционного заражения и интраоперационного повреждения брюшины. В этом случае инфекция возникает непосредственно в дупликатуре брюшины. Изолированное поражение участка сальника обнаруживается при туберкулезе и актиномикозе. В хирургии встречается преимущественно вторичное воспаление, которое возникает в результате следующих причин:
Патогенез
Ввиду обильного кровоснабжения и большого количества рыхлой жировой ткани сальник быстро вовлекается в процесс воспаления. Орган обладает резорбтивной и адгезивной способностью и выполняет защитную функцию в организме. При механическом повреждении, ишемии, инфекционном процессе повышается иммунологическая активность клеток, способность к абсорбции жидкости из полости живота, активизируется система гемостаза. При оментите отмечается гиперемия, отек складок брюшины с фиброзным наслоением и инфильтративным уплотнением тканей. При гистологическом исследовании обнаруживаются признаки воспаления (тромбоз и полнокровие сосудов, кровоизлияния, островки некроза), участки лейкоцитарной инфильтрации, большое количество эозинофилов, лимфоцитов. При туберкулезном оментите визуализируются множественные белесоватые бугорки. Мелкие образования приобретают красноватый окрас при соприкосновении органа с воздухом во время хирургических манипуляций.
Классификация
Исходя из выраженности воспалительного процесса, выделяют острый и хронический оментит. Острая форма болезни сопровождается ярко выраженными симптомами с нарастающей интоксикацией, хроническая характеризуется вялотекущим течением с периодами обострения и ремиссии. В зависимости от степени воспалительно-деструктивных изменений выделяют 3 стадии оментита:
Симптомы оментита
Клиническая картина патологии зависит от характера воспалительного процесса и причин заболевания. При остром оментите пациенты жалуются на интенсивные резкие боли в животе, не имеющие четкой локализации. Развиваются признаки интоксикации: рвота, повышение температуры тела до фебрильных значений, головная боль, головокружение. При осмотре обращает внимание мышечное напряжение брюшной стенки, иногда пальпируется болезненное образование плотной консистенции. Патогномоничным признаком является невозможность разогнуть туловище, ввиду чего пациент находится в полусогнутом состоянии. Спаечные процессы в брюшной полости могут привести к нарушению прохождения пищи по кишечнику, возникновению запора, частичной или полной кишечной непроходимости.
Хронический оментит характерен для послеоперационного и туберкулезного воспаления, проявляется дискомфортом и ноющими болями в животе, симптомы интоксикации отсутствуют или слабо выражены. При глубокой пальпации передней стенки живота определяется подвижное образование тестоватой консистенции, чаще безболезненное.
Осложнения
Диагностика
Ввиду редкости заболевания, отсутствия специфической клинической картины дооперационное установление диагноза представляет значительные трудности. Для диагностики оментита рекомендовано провести следующие обследования:
Дифференциальная диагностика оментита проводится с другими воспалительными внутрибрюшинными заболеваниями (аппендицит, холецистит, панкреатит, колит). Патология может иметь схожую симптоматику с перитонитом, перфоративной язвой желудка, 12-ПК, кишечной непроходимостью другой этиологии. Заболевание дифференцируют с доброкачественными и злокачественными новообразованиями кишечника, брыжейки. Для дополнительной диагностики и исключения заболеваний близлежащих органов проводят УЗИ ОБП.
Лечение оментита
При тяжелых поражениях органа и выраженной клинической картине проводят срочное хирургическое вмешательство. Во время операции, исходя из масштабов поражения, выполняют оментэктомию и тщательную ревизию полости живота. Линию резекции инвагинируют и ушивают тонкими кетгутовыми нитками. В брюшную полость вводят антибактериальные препараты и устанавливают дренаж. В послеоперационном периоде назначают антибиотики, анальгетики.
При подтвержденном хроническом оментите возможно проведение консервативной терапии. В условиях стационара назначают антибактериальные препараты согласно чувствительности возбудителя инфекции, противовоспалительные и обезболивающие средства. Пациентам рекомендован покой, постельный режим. После стихания воспаления выполняют курс физиотерапевтических процедур (УВЧ, магнитотерапия, соллюкс-терапия).
Прогноз и профилактика
Прогноз заболевания зависит от запущенности патологии и масштабов поражения сальника. При своевременно проведенной операции и грамотном ведении реабилитационного периода прогноз благоприятный. Пациенты через несколько месяцев возвращаются к привычному образу жизни. Генерализованное поражение с острой интоксикацией влечет развитие тяжелых жизнеугрожающих состояний (шок, сепсис). Профилактика оментита заключается в тщательной внутрибрюшной ревизии при выполнении лапаротомии, своевременном лечении острых и хронических заболеваний. Пациентам после проведения вмешательств на ОБП 1-2 раза в год показано проведение УЗИ-контроля.
САЛЬНИК
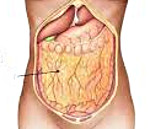
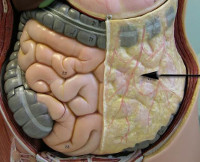
САЛЬНИК (omentum) — складка висцеральной брюшины. Различают малый и большой С. Малый С. (omentum minus) представляет собой дупликатуру брюшины, идущую от ворот печени к малой кривизне желудка и двенадцатиперстной кишке. Большой С. (omentum majus, epiploon) отходит от большой кривизны желудка.
Содержание
Эмбриология
Малый и большой С. являются производными первичных брыжеек (см. Брюшина, эмбриология). Малый С. образуется из вентральной брыжейки желудка и двенадцатиперстной кишки (вентрального мезогастрия), к-рая в результате эмбрионального поворота желудка и двенадцатиперстной кишки приобретает поперечное положение. Большой С. развивается из дорсальной брыжейки желудка (дорсального мезогастрия), по мере поворота желудка перемещающейся влево и распространяющейся в каудальном направлении. Встречаясь с брыжейкой поперечной ободочной кишки, большой С. срастается с ней и отклоняется вентрально, ложась на петли тонкой кишки. Развитие малого и большого С. связано с формированием сальниковой сумки (bursa omentalis). Ее зачаток образуется еще до начала дорсального мезогастрия, к-рое увеличивается влево, поэтому желудок, совершив поворот, оказывается лежащим вентрально от сальниковой сумки. В дальнейшем рост сальниковой сумки происходит в каудальном направлении — она располагается между пластинками большого сальника.
Анатомия
Форма, размеры и положение большого С. имеют индивидуальные особенности и изменяются с возрастом. У новорожденных С. короткий и не содержит жира. На 1-м году жизни С. быстро увеличивается в размерах, в нем появляется жировая ткань. Однако наиболее интенсивное развитие жировой ткани в С. приходится на период полового созревания.
Большой С. богато васкуляризо-ван ветвями правой и левой желудочно-сальниковых артерий (аа. gastro-epiploicae dext. et sin.). Отток крови происходит по одноименным венам в воротную вену. Лимф, сосуды впадают в правые и левые желудочно-сальниковые и средние ободочные лимф. узлы.
Гистология
Брюшина (см.), образующая С., состоит из мезотелия и собственной пластинки, содержащей рыхлую сеть эластических и коллагеновых волокон. В местах, где проходят сосуды и нервы, соединительная ткань более плотная. Между трабекулами соединительной ткани в большом С. находятся жировые дольки, а также скопления макрофагов и лимфоцитов, образующие млечные пятна (см.).
Функциональное значение сальника до конца не изучено. Известна важная роль большого С. в защите органов брюшной полости от инфекции. М. И. Штуцер (1913) показал, что при введении туши в брюшную полость экспериментальных животных основная масса ее частиц резорбируется большим С. в течение 6 мин.; смыть эти частицы или отделить их от С. не удается, тогда как с остальной поверхности брюшины тушь легко смывается. Через 24 часа после введения туши С. принимает интенсивно черную окраску, а свободных частиц туши в брюшной полости не находят. В С. тушь откладывается в лимф, узлах, эндотелии лимф, сосудов и млечных пятнах. При введении в брюшную полость взвеси бактерий часть их погибает под действием бактерицидных свойств серозной жидкости, а часть захватывается и разрушается мезотелием С., клетками его млечных пятен и гистиоцитами соединительнотканной основы.
На внутрибрюшную иммунизацию С. реагирует активной выработкой антител; при этом титр антител в нем значительно выше, чем в селезенке и печени. При проникающих ранениях живота С., закрывая раневое отверстие, препятствует эвентрации и защищает брюшную полость от инфицирования.
При повреждениях органов брюшной полости экспериментальных животных в лимф, сосудах большого С. обнаруживают частицы ткани поджелудочной железы, селезенки, печени, эпителий желчного пузыря, эритроциты, полиморфно-ядерные лейкоциты, бактерии. Инородные тела, попадающие в брюшную полость и не поддающиеся рассасыванию, осумковываются в большом С. независимо от места введения их в брюшную полость. Способность большого С. к инкапсуляции инородных тел в брюшной полости показывают и клин, наблюдения. При острых воспалительных заболеваниях органов брюшной полости во время операции обычно обнаруживают, что большой С. отграничивает очаг воспаления от свободной брюшной полости.
Методы обследования
Возможности для клин, исследования С. ограничены, т. к. патол. изменения в нем обычно сочетаются с заболеваниями или повреждениями других органов брюшной полости.
Как правило, характерных жалоб или анамнестических данных, свойственных именно патологии С., выявить не удается. Данные физикаль-ного обследования С. обычно также малоинформативны, т. к. не позволяют дифференцировать заболевания С. и органов брюшной полости. Косвенную информацию о состоянии С. удается получить с помощью контрастных рентгенологических и эндоскопических методов исследования жел.-киш. тракта. Деформация или смещение различных его отделов, обнаруживаемые при этом, могут быть обусловлены патол. процессами в С. В нек-рых случаях (напр., при кистах или опухолях С.) важное диагностическое значение имеет ультразвуковая диагностика (см.), а также компьютерная томография (см. Томография компьютерная). Распространенным и весьма информативным методом исследования С. является лапароскопия (см. Перитонеоскопия), позволяющая осмотреть значительную часть большого и малого С., а при необходимости произвести также прицельную биопсию его с последующим гистол. и цитол. исследованием.
Патология
Аномалия развития — врожденное отсутствие большого С.— встречается редко. При врожденных отверстиях в большом С. возможно ущемление как части С., так и других органов брюшной полости. Клинически это проявляется симптомами острого живота (см.).
Повреждения С. часто сочетаются с повреждениями других органов брюшной полости и могут возникать в результате закрытых и проникающих травм живота. Изолированные повреждения С. встречаются редко. В результате тупой травмы может возникать гематома С. с последующим нагноением, а при разрывах гематомы — значительные внутрибрюшные кровотечения. Лечение оперативное.
Острый воспалительный процесс в С.— оментит — обычно возникает вследствие распространения на С. воспаления с органов брюшной полости и характеризуется клин, симптоматикой острого живота. Хрон. воспаление С., как правило, является следствием острого оментита, но иногда имеет специфический (чаще туберкулезный) характер. При этом пораженный участок С. утолщается за счет развития соединительной ткани и образования спаек с органами брюшной полости. Воспалительный инфильтрат в таких случаях может достигать значительных размеров и пальпироваться через переднюю брюшную стенку. Лечение туберкулезного оментита специфическое.
При абсцедировании воспалительного инфильтрата развивается клин, картина отграниченного или диффузного перитонита (см.).
В случае приращения большого С. в результате хрон. воспаления к нижним отделам передней брюшной стенки или органам малого таза возможно сдавление сальником нек-рых органов брюшной полости, чаще тонкой или толстой кишки, что клинически проявляется симптомами рецидивирующей непроходимости кишечника (см.). При этом иногда встречается синдром натянутого С. (синдром Кноха), проявляющийся упорными болями, иногда рвотой, возникающей при попытке встать, отклонить туловище назад, разогнуться и т. д.
Ущемление С. чаще наблюдается при грыжах передней брюшной стенки, но иногда и при так наз. сальниковых грыжах (см. Грыжи). При этом в сальниковое отверстие внедряется часть С., к-рая затем вследствие нарушения кровообращения подвергается некрозу. Клинически это состояние проявляется картиной острого живота и требует срочного оперативного лечения.
Редким заболеванием является заворот большого С., как правило, приводящий к его некрозу с развитием симптомов перитонита. Лечение оперативное.
Тромбоз сосудов С., встречающийся при выраженном атеросклерозе, обычно также приводит к некрозу С.
Паразитарные заболевания С., обычно эхинококков (см.), встречаются редко. При этом в брюшной полости может пальпироваться чаще подвижное опухолевидное образование. Лечение оперативное.
Доброкачественные опухоли С. (липома, ангиома, лимфангпома и др.) встречаются редко; они представляют собой подвижные новообразования, иногда пальпирующиеся через переднюю брюшную стенку. Из злокачественных опухолей чаще наблюдается саркома, реже рак и эндотелиома. При злокачественных опухолях С. часто поражается вторично вследствие развития в нем метастазов опухолей в основном органов брюшной полости.
Операции
Операции при патол. процессах в С. и его повреждениях заключаются в основном в его резекции с удалением пораженных участков.
Анатомо-физиологические особенности большого С. позволяют использовать его при оперативных вмешательствах на ряде органов брюшной и грудной полостей. Напр., большим С. тампонируют с гемостатической целью раны печени и селезенки. При перфорации каллезной язвы желудка или двенадцатиперстной кишки часть большого С. на ножке подшивают к краям перфоративного отверстия. Участки С. могут быть также использованы для перитонизации линии анастомоза, наложенного на органах жел.-киш. тракта. При оперативном лечении цирроза печени (см.) большой С. подшивают к париетальной брюшине передней брюшной стенки (см. Тальмы — Драммонда операция) или диафрагмальной поверхности печени (омен-тогепатопексия), что приводит к развитию дополнительных портокавальных анастомозов. Для улучшения кровообращения в миокарде производят оментокардиопексию (см. Артериализация миокарда).
При операциях на поджелудочной железе, а также при ревизии задней стенки желудка верхнюю часть большого С. (желудочно-ободочную связку) рассекают и проникают в сальниковую сумку. Малый С. рассекают при операциях на внепеченоч-ных желчных путях, резекции желудка, гастрэктомии, ваготомии, при доступе к поджелудочной железе н дренировании сальниковой сумки.
Библиография: Барон М. А. Реактивные структуры внутренних оболочек (серозных, мозговых, синовиальных, эндокарда и амниона), Л., 1949; Елизаровений С. И. К хирургической анатомии полости малого сальника, Архангельск, 1949, библиогр.; Запорожец А. А. Инфицирование брюшины через физически герметичный кишечный шов, Минск, 1968; Нечипоренко Ф. П. Анатомические варианты большого сальника человека и их практическое значение в хирургии, Нов. хир. арх., № 3, с. 45, 1957; Панченков H. Р. и Стрекаловский В. П. Перекручивание большого сальника, в кн.: Вопр. диагностики и лечения забол. органов пищеварения, под ред. С. И. Бабичева и Б. С. Брискина, с. 125, М., 1974; Хирургическая анатомия живота, под ред. А. Н. Максименкова, с. 116, Л., 1972; Are у L. В. Developmental anatomy, Philadelphia, 1974.
Г. А. Покровский; В. С. Сперанский (ан., гист., эмбр.).