С чем реагируют нитраты
С чем реагируют нитраты
Азотная кислота – одноосновная, образует один ряд солей – нитраты состава X(NO3)n, где X – катион металла или NH4.
Нитраты щелочных металлов и аммония называют селитрами.
Нитраты – вещества с преимущественно ионным типом кристаллических решёток. При обычных условиях это твёрдые кристаллические вещества, которые могут быть окрашены только за счёт катионов металлов. Практически все нитрaты хорошо растворимы в воде, легкоплавки.
В водных растворах нитратов не происходит гидролиз по аниону, так как HNO3 – сильная кислота.
Нитрaты щелочных (кроме Li) и щёлочноземельных металлов разлагаются с образованием нитритов и кислорода:
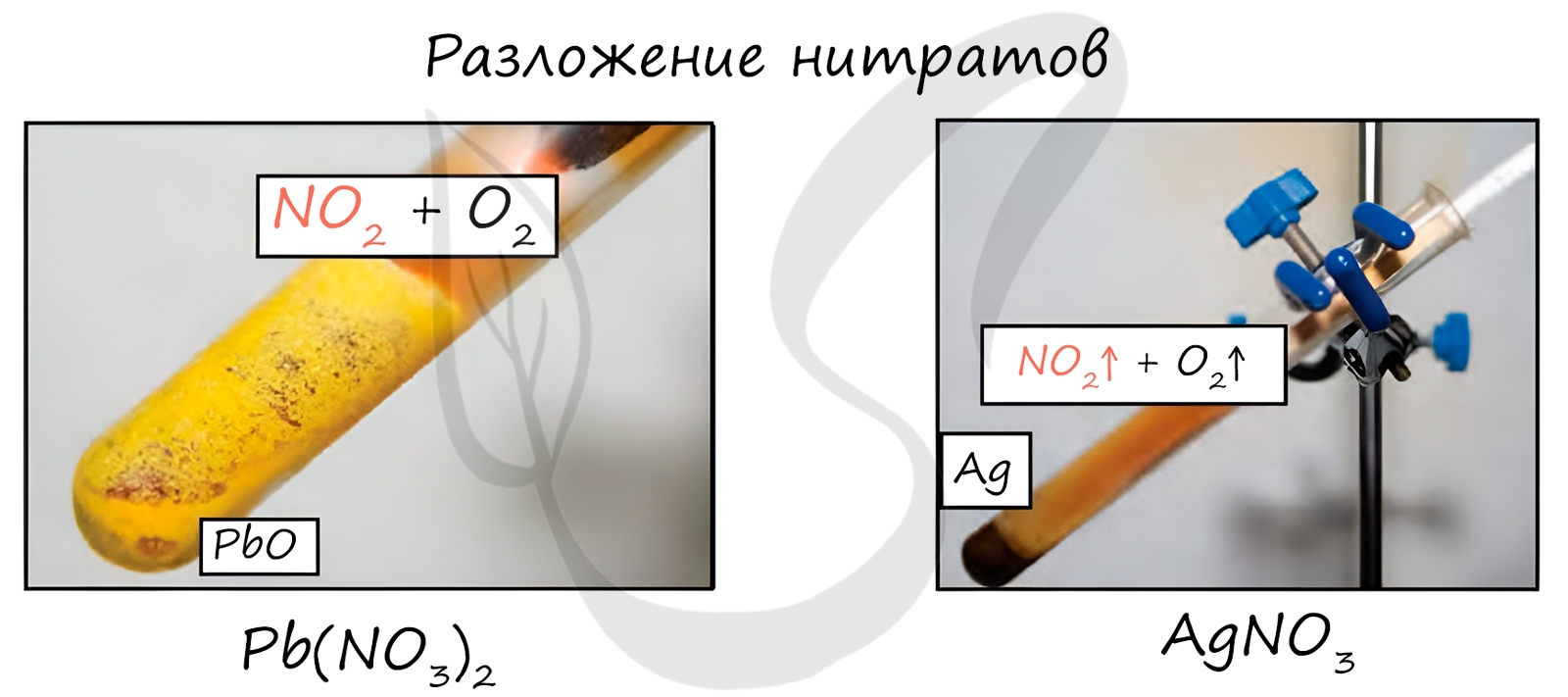
Нитpaты металлов, расположенных в электрохимическом ряду напряжений металлов от Mg до Си включительно, и нитрат Li разлагаются в соответствии со схемой:
Нитpаты металлов, расположенных в электрохимическом ряду напряжений металлов правее Си, разлагаются по схеме:
Особый случай – разложение NH4NO3. При плавлении разлагается:
Получение и применение нитратов
Нитраты получают действием азотной кислоты HNO3 на металлы, оксиды, гидроксиды, соли.
Соли азотной кислоты устойчивы при обычной температуре. Они обычно плавятся при относительно низких температурах (200—600 °C), зачастую с разложением.
Основное применение нитратов — удобрения (селитры), взрывчатые вещества (аммониты), получение стекла, производство лекарств, пищевые добавки при производстве колбас, в пиротехнике, компоненты ракетного топлива.
Соли азотной кислоты являются компонентами минеральных удобрений. Растения используют азот из соли для построения клеток организма, создания хлорофилла.
Влияние нитратов на окружающую среду и здоровье человека
Азот как основной питательный элемент влияет на рост вегетативных органов – зеленых стеблей и листьев. Избыточное употребление азотных удобрений не только ведет к аккумуляции нитратов в растениях, но и приводит к загрязнению ими водоемов и грунтовых вод. Для суммы нитрат-ионов в почве принята предельно допустимая концентрация (ПДК) – 130 мг/кг, в воде разных водоисточников – 45 мг/л.
В организм человека 70% нитратов поступает с овощами, 20% – с водой, 6% – с мясом и рыбой. Попадая в организм человека, часть нитратов всасывается в желудочно-кишечном тракте в неизмененном виде, другая часть, в зависимости от присутствия микроорганизмов, значения рН и других факторов, может превращаться в более ядовитые нитриты, аммиак, гидроксиламин NН2ОН; в кишечнике из нитратов могут образоваться вторичные нитрозамины R2N–N=О, обладающие высокой мутагенной и канцерогенной активностью. Признаки небольшого отравления – слабость, головокружение, тошнота, расстройство желудка и т. д. Снижается работоспособность, возможна потеря сознания.
Конспект урока «Соли азотной кислоты».
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.
В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.
При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
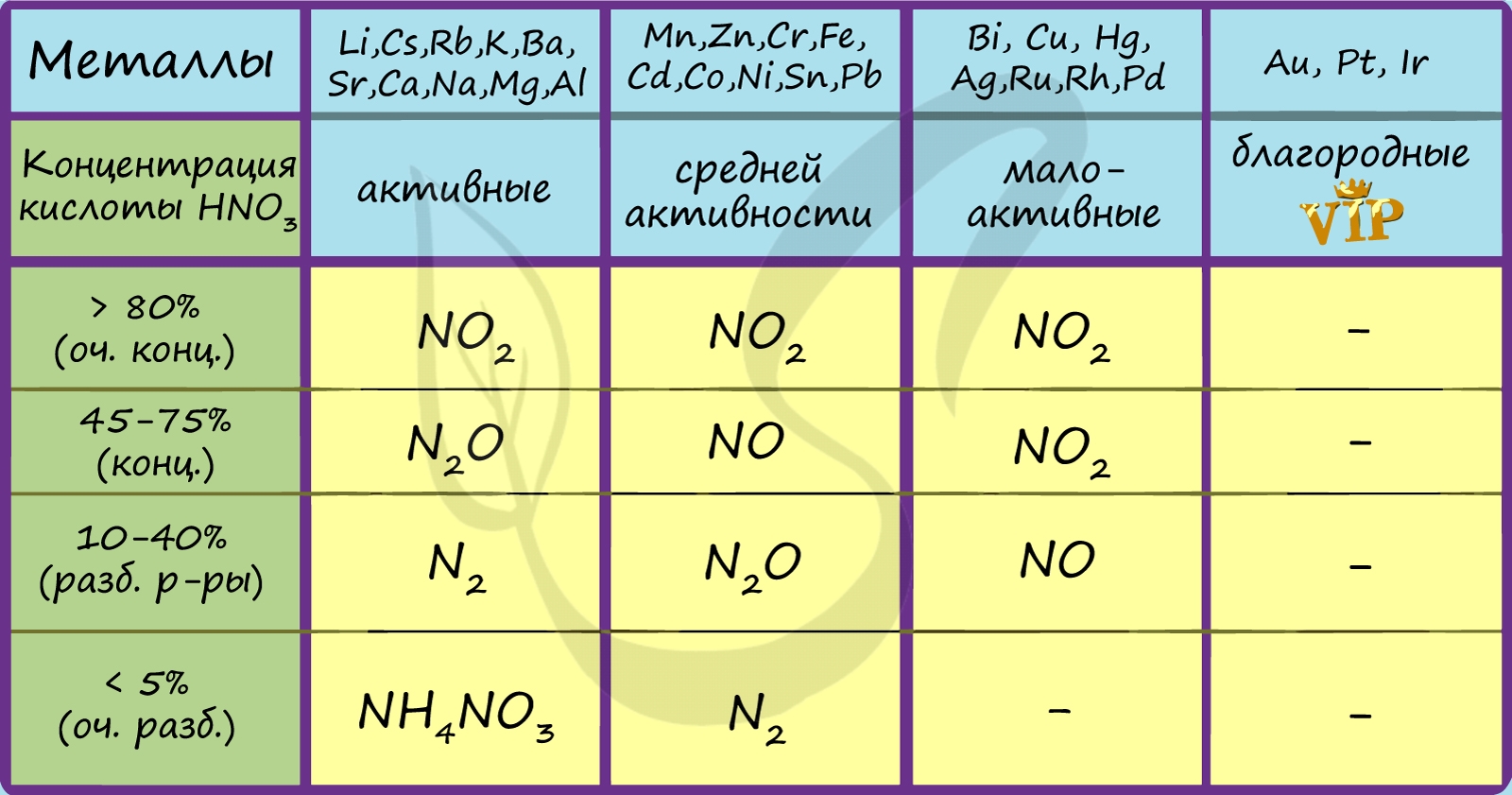
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.
Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.
Нитрат аммония получают реакция аммиака с азотной кислотой.
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
С чем реагируют нитраты
I. Нитраты (селитры)
Азотная кислота – одноосновная, образует один ряд солей – нитраты состава:
II. Физические свойства
Нитраты – вещества с преимущественно ионным типом кристаллических решёток. При обычных условиях это твёрдые кристаллические вещества, все нитраты хорошо растворимы в воде, сильные электролиты.
III. Получение нитратов
Нитраты образуются при взаимодействии:
1) Металл + Азотная кислота
2) Основный оксид + Азотная кислота
3) Основание + Азотная кислота
4) Аммиак + Азотная кислота
5) Соль слабой кислоты + Азотная кислота
В cоответствии с рядом кислот каждая предыдущая кислота может вытеснить из соли последующую:
6) Оксид азота (IV) + щёлочь
IV. Химические свойства нитратов
I. Общие с другими солями
1) Взаимодействие с металлами
Металл, стоящий в ряду активности левее, вытесняет последующие из их солей:
2) Взаимодействие с кислотами
3) Взаимодействие со щелочами
4) Взаимодействие с cолями
II. Специфические
Все нитраты термически неустойчивы. При нагреванииразлагаются с образованием кислорода. Характер других продуктов реакции зависит от положения металла, образующего нитрат, в электрохимическом ряду напряжений:
2) Нитраты менее активных металлов от Mg до Cu включительно и нитрат лития разлагаются до оксидов:
3) Нитраты наименее активных металлов (правее меди) разлагаются до металлов:
4) Нитрат и нитрит аммония:
Нитрат аммония разлагается в зависимости от температуры так:
Качественная реакция на нитрат-ион NO3 – – взаимодействие нитратов c металлической медью при нагревании в присутствии концентрированной серной кислоты или с раствором дифениламина в Н2SO4 (конц.).
Опыт: “Качественная реакция на ион NO3 – “
Протекают следующие уравнения реакций:
V. Применение нитратов
Почему азота в природе много (он входит в состав атмосферы), а растения часто дают плохой урожай из-за азотного голодания?
Растения не могут усваивать молекулярный азот N2 из воздуха. Это проблема «связанного азота». При недостатке азота задерживается образование хлорофилла, поэтому растения имеют бледно-зеленую окраску, как следствие, задерживается рост и развитие растения. Азот – жизненно важный элемент. Без белка нет жизни, а без азота нет белка.
Как же усваивается атмосферный азот? Часть связанного азота поступает в почву во время гроз. Химия процесса такова:
Существуют растения способные повышать плодородие почвы, в чем же их особенность? Эти растения (люпин, люцерна, клевер, горох, вика) относятся к семейству бобовых (мотыльковые), на корнях которых развиваются клубеньковые бактерии, способные связывать атмосферный азот, переводя его в соединения, доступные для растений.
Растения, связывающие атмосферный азот
«Классификация азотных удобрений»
Одной из важных характеристик является содержание питательного элемента в удобрении. Расчет питательного элемента для азотных удобрений ведут по содержанию азота.
Влияние нитратов на окружающую среду и организм человека
Азот как основной питательный элемент влияет на рост вегетативных органов – зеленых стеблей и листьев. Азотные удобрения не рекомендуется вносить поздней осенью или ранней весной, т. к. талые воды смывают до половины удобрений. Важно соблюдать нормы и сроки внесения удобрений, вносить их не сразу, а в несколько приемов. Применять медленно действующие формы удобрений (гранулы, покрытые защитной пленкой), при посадке использовать сорта, склонные к низкому накоплению нитратов. Коэффициент использования азотных удобрений – 40–60%. Избыточное употребление азотных удобрений не только ведет к аккумуляции нитратов в растениях, но и приводит к загрязнению ими водоемов и грунтовых вод. Антропогенными источниками загрязнения водоемов нитратами являются также металлургия, химическая, в том числе целлюлозно-бумажная, и пищевая отрасли промышленности. Одним из признаков загрязнения водоемов является «цветение» воды, вызванное бурным размножением синезеленых водорослей. Особенно интенсивно оно происходит во время таяния снега, летних и осенних дождей. Предельно допустимая концентрация (ПДК) нитратов регламентируется ГОСТом. Для суммы нитрат-ионов в почве принято значение 130 мг/кг, в воде разных водоисточников – 45 мг/л. (ПДК (NO3 – в почве) – 130 мг/кг, ПДК (NO3 – в воде) – 45 мг/л.).
Такие растения называют нитратонакопителями. В организм человека 70% нитратов поступает с овощами, 20% – с водой, 6% – с мясом и рыбой. Попадая в организм человека, часть нитратов всасывается в желудочно-кишечном тракте в неизмененном виде, другая часть, в зависимости от присутствия микроорганизмов, значения рН и других факторов, может превращаться в более ядовитые нитриты, аммиак, гидроксиламин NН2ОН; в кишечнике из нитратов могут образоваться вторичные нитрозамины R2N–N=О, обладающие высокой мутагенной и канцерогенной активностью. Признаки небольшого отравления – слабость, головокружение, тошнота, расстройство желудка и т. д. Снижается работоспособность, возможна потеря сознания.
В организме человека нитраты взаимодействуют с гемоглобином крови, превращая его в метгемоглобин, в котором железо окислено до Fe 3+ и не может служить переносчиком кислорода. Именно поэтому один из признаков острого отравления нитратами – синюшность кожных покровов. Выявлена прямая зависимость между случаями появления злокачественных опухолей и интенсивностью поступления в организм нитратов при избытке их в почве.
Опыт: “Исследование содержания нитратов в продуктах питания”
(качественная реакция на нитрат-ион NO3 – )
Первая помощь при отравлении нитратами
Первая помощь при отравлении нитратами – это обильное промывание желудка, прием активированного угля, солевых слабительных – глауберовой соли Na2SO4•10H2O и английской соли (горькая соль) MgSO4•7H2O, cвежий воздух.
Уменьшить вредное влияние нитратов на организм человека можно с помощью аскорбиновой кислоты (витамина С); если ее соотношение с нитратами составляет 2:1, то нитрозамины не образуются. Доказано, что прежде всего витамин С, а также витамины Е и А являются ингибиторами – веществами, предотвращающими и тормозящими процессы преобразования нитратов и нитритов в организме человека. Необходимо ввести в рацион питания побольше черной и красной смородины, других ягод и фруктов (кстати, в висячих плодах нитратов практически нет). И еще один естественный нейтрализатор нитратов в организме человека – это зеленый чай.
Причины накопления нитратов в овощах и способы выращивания экологически чистой продукции растениеводства
Наиболее интенсивно азот поглощается во время роста и развития стеблей и листьев. При созревании семян потребление азота из почвы практически прекращается. Плоды, достигшие полной зрелости, уже не содержат нитратов – происходит полное превращение соединений азота в белки. Но у многих овощей ценится именно незрелый плод (огурцы, кабачки). Удобрять такие культуры азотными удобрениями желательно не позднее чем за 2–3 недели до уборки урожая. Кроме того, полному превращению нитратов в белки препятствуют плохая освещенность, избыточная влажность и несбалансированность питательных элементов (недостаток фосфора и калия). Не следует увлекаться внесезонными тепличными овощами. Например, 2 кг тепличных огурцов, съеденных за один прием, могут вызвать опасное для жизни отравление нитратами. Надо также знать, преимущественно в каких частях растения накапливаются нитраты: у капусты – в кочерыжке, у моркови – в сердцевине, у кабачков, огурцов, арбузов, дыни, картофеле – в кожуре. У дыни и арбуза не следует есть незрелую мякоть, прилежащую к корке. Огурцы лучше почистить и срезать место прикрепления их к стеблю. У зеленных культур нитраты накапливаются в стеблях (петрушка, салат, укроп, сельдерей). Содержание нитратов в различных частях растений неравномерно: в черешках листьев, стебле, корне содержание их в 1,5–4,0 раза выше, чем в листьях. Всемирная организация здравоохранения считает допустимым содержание нитратов в диетических продуктах до 300 мг NO3 – на 1 кг сырого вещества. (ПДК (NO3 – в диетических продуктах) – 300 мг/кг.). Если самое высокое содержание нитратов отмечается в свекле, капусте, салате, зеленом луке, то самое низкое содержание нитратов – в репчатом луке, томатах, чесноке, перце, фасоли.
Чтобы вырастить экологически чистую продукцию, прежде всего необходимо грамотно вносить азотные удобрения в почву: в строго рассчитанных дозах и в оптимальные сроки. Выращивать овощи, особенно зеленные культуры, надо при хорошей освещенности, оптимальных показателях влажности почвы и температуры. И все же для уменьшения содержания нитратов овощные культуры лучше подкармливать органическими удобрениями. Несвоевременное внесение удобрений, особенно в избыточных дозах, в том числе и органического удобрения – навоза, приводит к тому, что поступившие в растение минеральные соединения азота не успевают полностью превратиться в белковые.
Нитраты в производстве взрывчатых веществ
Многие взрывчатые смеси содержат в своем составе окислитель (нитраты металлов или аммония и др.) и горючее (дизельное топливо, алюминий, древесную муку). Поэтому соли – нитрат калия, нитрат бария, нитрат стронция и другие – применяются в пиротехнике.
Азотное удобрение нитрат аммония вместе с алюминием и древесным углем входит в состав взрывчатой смеси – аммонала. Основная реакция, которая протекает при взрыве:
Высокая теплота сгорания алюминия повышает энергию взрыва. Применение нитрата аммония в составе аммонала основано на его свойстве разлагаться при детонации с образованием газообразных веществ:
В руках террористов взрывчатые вещества приносят мирным людям только страдания.
Нитрат серебра AgNO3, который чернит ткань, бумагу, парты и руки (ляпис), применяют как противомикробное средство для лечения кожных язв, для прижигания бородавок и в качестве противовоспалительного средства при хроническом гастрите и язве желудка: пациентам назначают пить 0,05%-й раствор АgNO3. Порошкообразные металлы Zn, Мg, Al, cмешанные с нитратом серебра, используют в петардах.
Основный нитрат висмута Вi(ОН)2NО3 назначают внутрь при язвенной болезни желудка и двенадцатиперстной кишки в качестве вяжущего и антисептического средства. Наружно – в мазях, присыпках при воспалительных заболеваниях кожи.
Соль нитрит натрия NaNО2 применяют в медицине как спазмолитическое средство.
Применение нитритов в пищевой отрасли промышленности
Нитриты применяют в колбасном производстве: 7 г на 100 кг фарша. Нитриты придают колбасе розовый цвет, без них она серая, как вареное мясо, и не имеет товарного вида. К тому же присутствие нитритов в колбасе необходимо еще и по другой причине: они предотвращают развитие микроорганизмов, выделяющих токсичные яды.
Что такое нитраты и надо ли с ними бороться
Лето – пора созревания большинства сельскохозяйственных культур. Когда, как не в это время, лакомиться плодами щедрой матушки природы! На рынках – изобилие овощей и фруктов. Продавцы наперебой предлагают свою продукцию, уверяя покупателей, что их товар – самый полезный, экологически чистый и без нитратов! Что же такое нитраты, так ли они опасны для здоровья и возможно ли вырастить урожай без них?
Нитраты – это соли азотной кислоты. Они в небольших дозах присутствуют во всех живых организмах, а растения без них просто не смогут вырасти и дать плоды. Но даже, если растение выросло без применения азотных удобрений, в нем все равно будут присутствовать нитраты. Количество их зависит от множества факторов: особенностей сорта, влажности, температуры, интенсивности освещения, использования удобрений.
В организм человека они попадают с водой или пищей, могут превращаться в нем в вещества с канцерогенной активностью, со временем провоцирующие онкологические заболевания.
Проблема не в наличии нитратов, а в их количестве и концентрации.
Для человека по данным ВОЗ предельно допустимая суточная доза нитратов составляет 3,7 мг на 1 кг массы тела. Если она превышена, может произойти отравление. Его симптомы: головокружение, тошнота, усиленное сердцебиение, общая слабость.
При появлении первых признаков отравления пострадавшему необходимо:
Принять активированный уголь.
Рекомендуется также интенсивное употребление чистой воды, через некоторое время больного напоить крепким, сладким чаем с лимоном.
В разных частях растения содержание нитратов не одинаково. Наибольшее количество солей азотной кислоты концентрируется:
 | в сердцевине |
 | в кочерыжке и жилках листа |
 | в стеблях и на кончике корня |
 | в стебле и корнях |
 | в кожуре |
 | прямо под коркой |
 | в слое, прилегающем к кожуре |
Чтобы нитраты не доставили вам неприятностей, необходимо знать несколько правил, которые сведут к минимуму возможную опасность:
нитраты содержатся преимущественно в растительных продуктах, мясо и молоко содержат их очень мало;
при правильном длительном хранении овощей нитраты со временем разрушаются;
максимально накапливаются нитраты в плодах на начальной стадии роста, по мере созревания они расходуются, поэтому незрелые плоды наиболее опасны;
не следует покупать слишком большие плоды или слишком маленькие; наименьшее количество нитратов в полностью дозревших овощах и фруктах среднего размера;
в кислых на вкус плодах наименьшее содержание нитратов, так как витамин С, содержащийся в них, разрушает их;
в соленом и консервированном виде часть вредных веществ переходит в раствор;
тщательно мойте овощи, фрукты, корнеплоды, очищайте их от кожуры;
снизить количество вредных веществ, поможет их замачивание в холодной воде на несколько часов;
при кулинарной обработке овощей большая часть нитратов разрушается;
не рекомендуется долго размораживать замороженные овощи, при этом нитраты в них преобразуются в нитриты, еще более опасные для здоровья;
выращенные в ранние сроки растения содержат намного больше нитратов, чем овощи, выросшие в свой срок в открытом грунте.
К сожалению, определить на глаз содержание нитратов в продуктах практически невозможно, но при покупке стоит обратить внимание на слишком крупный размер, наличие белых прожилок в мякоти, ее рыхлость и водянистость, чрезмерно насыщенный цвет и идеальную форму – все это может быть признаком большого содержания нитратов.
Берегите себя и своих близких, и пусть дары природы приносят вам только пользу!
Миловзорова А. М., Морозова С. М., Самойленкова Т. Г.