С чем реагирует сао
Оксид кальция
| Оксид кальция | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид кальция |
| Химическая формула | CaO |
| Физические свойства | |
| Состояние (ст. усл.) | твердое |
| Молярная масса | 56.077 г/моль |
| Плотность | 3.37 г/см³ |
| Термические свойства | |
| Температура плавления | 2570 °C |
| Температура кипения | 2850 °C |
| Молярная теплоёмкость (ст. усл.) | 42.05 Дж/(моль·К) |
| Энтальпия образования (ст. усл.) | -635,09 кДж/моль |
Окси́д ка́льция (окись кальция, негашёная и́звесть или «кипелка», «кираби́т») — белое кристаллическое вещество, формула CaO.
Негашёная известь и продукт её взаимодействия с водой — Ca(OH)2 (гашёная известь или «пушонка») находят обширное использование в строительном деле.
Содержание
Получение
В промышленности оксид кальция получают термическим разложением известняка (карбоната кальция):
Также оксид кальция можно получить при взаимодействии простых веществ:
или при термическом разложении гидроксида кальция и кальциевых солей некоторых кислородсодержащих кислот:
Физические свойства
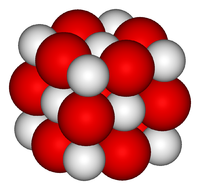
Оксид кальция — белое кристаллическое вещество, кристаллизующееся в кубической гранецентрированной кристаллической решетке, по типу хлорида натрия.
Химические свойства
Оксид кальция относится к основным оксидам. Растворяется в воде с выделением энергии, образуя гидроксид кальция:

Как основный оксид реагирует с кислотными оксидами и кислотами, образуя соли:

Применение
Основные объёмы используются в строительстве при производстве Силикатного кирпича. Раньше известь, так же использовали в качестве известкового цемента — при смешивании с водой, оксид кальция переходит в гидроксид, который далее, поглощая из воздуха углекислый газ, сильно твердеет, превращаясь в карбонат кальция. Однако в настоящее время известковый цемент при строительстве жилых домов стараются не применять, так как полученные строения обладают способностью впитывать и накапливать сырость.
Категорически недопустимо использование известкового цемента при кладке печей — из-за термического разложения и выделения в воздух удушливого диоксида углерода.
Некоторое применение также находит в качестве доступного и недорогого огнеупорного материала — плавленный оксид кальция имеет некоторую устойчивость к воздействию воды, что позволяет его использовать в качестве огнеупора там, где применение более дорогих материалов нецелесообразно.
В небольших количествах оксид кальция также используется в лабораторной практике для осушения веществ, которые не реагируют с ним.
В промышленности для удаления диоксида серы из дымовых газов, как правило используют 15% водяной раствор. В результате реакции гашеной извести и диоксида серы получается гипс СaСO3 и СаSO4. В эксперементальных установках добивались показателя в 98% отчиски дымовых газов от диоксида серы.
Так же используется в «самогреющей» посуде. Контейнер с небольшим количеством оксида кальция помещается между двух стенок стакана, а при прокалывании капсулы с водой начинается реакция с выделением тепла.
Оксид кальция

Всего получено оценок: 119.
Всего получено оценок: 119.
Негашёная известь – это оксид кальция. Его получают в лабораториях и промышленным путём из природных материалов. Вещество активно используется в строительстве и промышленности.
Физические свойства
Оксид кальция – неорганическое кристаллическое вещество в виде белого или серо-белого порошка без запаха и вкуса. Твёрдое вещество кристаллизуется в кубические гранецентрированные кристаллические решётки по типу хлорида натрия (NaCl).
Общее описание вещества представлено в таблице.
Признак
Значение
Формула соединения оксид кальция
В глицерине. В этаноле не растворяется, с водой образует гидроксид
Химическая связь в кристалле
Оксид кальция – едкое вещество, относящееся ко второму классу опасности. Агрессивные свойства проявляет при взаимодействии с водой, образуя гашёную известь.
Получение
Оксид кальция также называют жжёной известью из-за способа получения. Получают негашёную известь путём нагревания и разложения известняка – карбоната кальция (CaCO3).
Реакция получения оксида кальция из известняка выглядит следующим образом:
Кроме того, негашёную известь можно получить двумя способами:
Реакции протекают при высоких температурах. Температура сожжения известняка – 900-1200°C. При 200-300°C на поверхности металла начинает образовываться оксид. Для разложения солей и гидроксида необходима температура в 500-600°C.
Химические свойства
Оксид кальция является высшим оксидом и максимально проявляет окислительные свойства. Соединения взаимодействует с неорганическими веществами и свободными галогенами. Основные химические свойства оксида приведены в таблице.
Реакции
Что образуется
Молекулярное уравнение
Образуется гидроксид (гашёная известь). Реакция протекает бурно с выделением тепла
Растворяется, образуя соли
С оксидами неметаллов (кислотными остатками)
С углеродом при нагревании
Образуется карбид кальция
Восстанавливает кальций. Образуется оксид алюминия
Применение
Оксид используется в пищевой промышленности в качестве:
Кроме того, негашёная известь применяется в химической и строительной промышленности для производства различных веществ:
Что мы узнали?
Оксид кальция или негашёная известь – кристаллическое вещество, бурно реагирующее с водой и образующее гашёную известь. Широко используется в промышленности, в частности пищевой и строительной. Зарегистрирован как пищевая добавка Е529. Имеет высокие температуры плавления и кипения, растворяется только в глицерине. Образуется при сжигании карбоната кальция. Проявляет окислительные свойства, образует соли с оксидами и кислотами, взаимодействует с углеродом и алюминием.
Окись кальция
Окись кальция
| Оксид кальция | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Оксид кальция |
| Химическая формула | CaO |
| Молярная масса | 56.077 г/моль |
| Физические свойства | |
| Плотность вещества | 3.37 г/см³ |
| Состояние (ст. усл.) | твердое |
| Термические свойства | |
| Температура плавления | 2627 °C |
| Температура кипения | 2850 °C |
| Молярная теплоёмкость (ст. усл.) | 42.05 Дж/(моль·К) |
| Энтальпия (ст. усл.) | -635,09 кДж/моль |
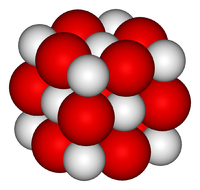
Оксид кальция — белое кристаллическое вещество, кристаллизующееся в кубической гранецентрированной кристаллической решетке, по типу хлорида натрия.
В промышленности оксид кальция получают термическим разложением известняка (карбоната кальция):
Также оксид кальция можно получить при взаимодействии простых веществ:
И при термическом разложении гидроксида кальция и кальциевых солей некоторых кислородсодержащих кислот:
Химические свойства
Оксид кальция относится к основным оксидам. Растворяется в воде с выделением энергии, образуя гидроксид кальция:
Как основной оксид реагирует с кислотными оксидами и кислотами, образуя соли:
Применение
Полезное
Смотреть что такое «Окись кальция» в других словарях:
окись кальция — Регулятор кислотности пищевого продукта, получаемый обжигом извести в печах при температурах от 900 °С до 1200 °С, содержащий основного вещества СаО не менее 95,0 % по остатку от сжигания, фторидов не более 50 мг/кг, бария не более 300… … Справочник технического переводчика
Кальция окись — Оксид кальция Общие Систематическое наименование Оксид кальция Химическая формула CaO Молярная масса 56.077 г/моль … Википедия
Кальция оксид — Оксид кальция Общие Систематическое наименование Оксид кальция Химическая формула CaO Молярная масса 56.077 г/моль … Википедия
Окись этилена — Окись этилена … Википедия
Окись азота — Оксид азота(II) Общие Систематическое наименование Оксид азота(II) Химическая формула … Википедия
Кальция окись — негашёная известь, кипелка, CaO, соединение кальция с кислородом; бесцветные кристаллы, плотность 3,4 г/см3, tпл 2585 °С. Технический продукт белое пористое вещество. К. о. жадно реагирует с водой с выделением большого количества тепла и… … Большая советская энциклопедия
Окись дифенилена — (oxyde de biphénylène, Di[Bi]phenylenoxyd) находится (около 0,3%) в смоле (Stupp, Stuppfett,), получающейся при перегонке без доступа воздуха ртутной руды в Идрии (Гольдшмидт и Шмидт); образуется при перегонке трехфенильного эфира ортофосфорной… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ОКСИД КАЛЬЦИЯ — окись кальция, негашеная известь, кипелка СаО бесцветные кристаллы; плотность 3400 кг/м3; tпл=2585° С; обладает основными свойствами. Технический продукт белое пористое вещество. Оксид кальция жадно реагирует с водой с образованием… … Металлургический словарь
ГОСТ 21639.3-93: Флюсы для электрошлакового переплава. Методы определения окиси кальция и окиси магния — Терминология ГОСТ 21639.3 93: Флюсы для электрошлакового переплава. Методы определения окиси кальция и окиси магния оригинал документа: 8.2 Аппаратура, реактивы и растворы Спектрофотометр атомно абсорбционный любого типа с источником излучения… … Словарь-справочник терминов нормативно-технической документации
Оксид кальция — Общие … Википедия
Оксид кальция. Свойства и меры предосторожности
Оксид кальция — неорганическое соединение с 
Негашеная известь называется так для отличия от гашеной извести, когда при соединении оксида кальция с водой проходит бурная реакция — известь «гасится» водой. Получается гашеная известь Ca(OH)2, востребованная во многих областях.
Жженой известью реактив называют с отсылкой на способ получения: известь (карбонат кальция CaCO3) обжигают до тех пор, пока она не начинает разлагаться, в результате чего получается жженая известь (окись кальция).
Обычно негашеной или жженой известью называют техническую квалификацию реактива.
Получить окись кальция можно разными методами.
• Промышленный способ описан выше: разложением известняка CaCO3 при нагревании.
• Разложением при нагревании гидроокиси кальция или солей кальция (солей определенных кислот, содержащих кислород). Например, разложением нитрита кальция Ca(NO3)2 получают CaO высокой чистоты.
• Прямым окислением (сжиганием) кальция в воздухе.
 |  |  |
| Полнолицевая маска «ЗМ» серии 6900 | Кальций окись «ч» | Перчатки «Неотоп» химостойкие (Ansell) (9,5-10) |
Свойства
Реагент представляет собой порошкообразное вещество белого или сероватого цвета без запаха. Структура кристаллов подобна структуре поваренной соли. Реактив гигроскопичен, поглощает из воздуха влагу и углекислый газ. Хорошо растворяется в глицерине, не растворяется в этиловом спирте. В воде не растворяется, а вступает с ней в химическую реакцию. Не горит. Токсичен.
С химической точки зрения очень активное соединение, осно́вный оксид. Реагирует с водой с образованием щелочи Ca(OH)2 и выделением большого количества тепла. В реакции с кислотами и кислотными оксидами образует соли. Взаимодействует с углеродом (получается карбид CaC2). Вступает в реакцию с метиловым спиртом, оксидами металлов, с металлами, с хлором, бромом и другими галогенами, углекислым газом, серой, фосфором, кремнием и многими другими веществами.
Меры предосторожности
Негашеная известь — едкое вещество, которое относится ко 2-му (высокоопасному) классу веществ. Особенно опасно смешивать оксид с водой. Во-первых, можно обжечься; во-вторых, образующаяся щелочь разъедает кожу. Но даже без воды оксид действует на кожу как щелочь: вытягивает влагу из кожи, разрушает белки, омыляет жиры, вызывает химический ожог.
Опасность представляют известковая пыль, ее пары и аэрозольные частицы. Они попадают в органы дыхания, вызывая раздражение и кашель. При попадании в легкие могут вызвать пневмонию. Проглатывание оксида кальция вызывает ожог пищевода и желудка.
Очень опасен реактив для слизистых носа и особенно глаз. Способен вызвать язвы слизистой носа и даже прободение носовой перегородки.
Пострадавшему от контакта с химикатом обязательно следует вызвать скорую помощь. До приезда скорой нужно хорошо промыть место поражения: кожу, глаза, пищевод.
При работе с оксидом кальция (как на производствах, так и в быту) следует использовать защитную одежду; респиратор; очки; перчатки, стойкие к щелочам. На предприятиях обязательно контролируют ПДК реактива в воздухе. Рабочее место должно располагаться в помещении с общей принудительной вентиляцией. Места высокого риска пыления дополнительно снабжаются локальной вытяжной вентиляцией.
Хранят реактив в герметичной упаковке 
В лабораториях работы следует проводить в вытяжном шкафу. Хранят реактив в герметичных стеклянных или пластиковых сосудах с обязательными предупреждающими этикетками.
Структура, свойства и применение оксида кальция (CaO)
оксид кальция (CaO) является неорганическим соединением, которое содержит кальций и кислород в ионных формах (не путать с пероксидом кальция, CaO2). Это известно во всем мире как известь, слово, которое обозначает любое неорганическое соединение, которое содержит карбонаты, оксиды и гидроксиды кальция, а также другие металлы, такие как кремний, алюминий и железо..
Это один из крупнейших природных источников кальция и является сырьем для производства оксида кальция. Как получается этот оксид? Карбонаты подвержены термическому разложению; нагревание карбонатов кальция при температуре выше 825 ° С, что приводит к образованию извести и углекислого газа.
Вышеприведенное утверждение можно описать следующим образом: CaCO3(s) → CaO (s) + CO2(G). Поскольку земная кора богата известняком и кальцитом, а в океанах и на пляжах имеются многочисленные морские раковины (сырье для производства оксида кальция), оксид кальция является относительно дешевым реагентом.
формула
Почему кальций имеет +2 заряда? Потому что кальций принадлежит к группе 2 периодической таблицы (г-н Бекамбара) и имеет только два валентных электрона, доступных для образования связей, которые уступают атому кислорода.
структура
Эта структура максимально выражает ионный характер этого оксида, хотя заметное различие радиусов (красная сфера больше, чем белая) придает более слабую кристаллическую ретикулярную энергию по сравнению с MgO.
свойства
Физически это кристаллическое белое твердое вещество без запаха и с сильными электростатическими взаимодействиями, которые ответственны за его высокие температуры плавления (2572 ° C) и кипения (2850 ° C). Кроме того, он имеет молекулярную массу 55,958 г / моль и интересную способность быть термолюминесцентным.
растворимость
CaO является основным оксидом, который обладает сильным сродством к воде в той степени, в которой он поглощает влагу (это гигроскопичное твердое вещество), и немедленно реагирует с образованием гашеной извести или гидроксида кальция:
Эта реакция является экзотермической (выделяет тепло) из-за образования твердого тела с более сильными взаимодействиями и более стабильной кристаллической решеткой. Тем не менее, реакция является обратимой, если Ca (OH) нагревается2, обезвоживание и освещение гашеной извести; затем лайм «возрождается».
Полученный раствор является очень основным, и если он насыщен оксидом кальция, он достигает рН 12,8.
Кроме того, он растворим в глицерине и в растворах кислоты и сахара. Поскольку это основной оксид, он, естественно, имеет эффективные взаимодействия с кислотными оксидами (SiO2, в2О3 и вера2О3, например) растворим в их жидких фазах. С другой стороны, он нерастворим в спиртах и органических растворителях.
приложений
CaO широко используется в промышленности, а также для синтеза ацетилена (CH≡CH), для извлечения фосфатов из сточных вод и в реакции с диоксидом серы из газообразных отходов..
Другие применения оксида кальция описаны ниже:
Как ступка
Если оксид кальция смешан с песком (SiO2) и вода спекается с песком и медленно реагирует с водой с образованием гашеной извести. В свою очередь, СО2 воздуха растворяется в воде и вступает в реакцию с солью с образованием карбоната кальция:
CaCO3 Это более стойкое и более твердое соединение, чем CaO, в результате чего раствор (предыдущая смесь) затвердевает и фиксирует кирпичи, блоки или керамику между ними или на желаемой поверхности..
В производстве очков
Основным сырьем для производства стекол являются оксиды кремния, которые смешивают с известью, карбонатом натрия (Na2Колорадо3) и другие добавки, которые затем подвергают нагреванию, в результате чего получается стеклообразное твердое вещество. Это твердое вещество впоследствии нагревается и выдувается в любых фигурах.
В горном деле
Гашеная известь занимает больший объем, чем негашеная, благодаря взаимодействиям водородных связей (О-Н-О). Это свойство используется, чтобы разбить камни изнутри.
Это достигается путем наполнения их компактной смесью извести и воды, которая герметизирована, чтобы сосредоточить ее тепло и экспансивную силу в породе..
Как средство для удаления силикатов
CaO сплавляется с силикатами с образованием коалесцирующей жидкости, которая затем извлекается из сырья определенного продукта..
Например, железные руды являются сырьем для производства металлического железа и стали. Эти минералы содержат силикаты, которые являются нежелательными примесями для процесса и устраняются только что описанным способом..
Наночастицы оксида кальция
Оксид кальция можно синтезировать в виде наночастиц, варьируя концентрации нитрата кальция (Са (NO3)2) и гидроксид натрия (NaOH) в растворе.
Эти частицы являются сферическими, основными (а также твердыми на макроуровне) и имеют большую площадь поверхности. Следовательно, эти свойства выгодны каталитическим процессам. Что? В настоящее время следствие отвечает на этот вопрос.
Эти наночастицы были использованы для синтеза замещенных органических соединений, полученных из пиридинов, при разработке новых лекарств для проведения химических превращений, таких как искусственный фотосинтез, для очистки воды от тяжелых и вредных металлов, а также для фотокаталитические агенты.
Наночастицы могут быть синтезированы на биологической подложке, такой как листья папайи и зеленый чай, для использования в качестве антибактериального средства..