Bacillus cereus ip 5832 что это такое
Дисбактериоз кишечника и роль пробиотиков в его коррекции
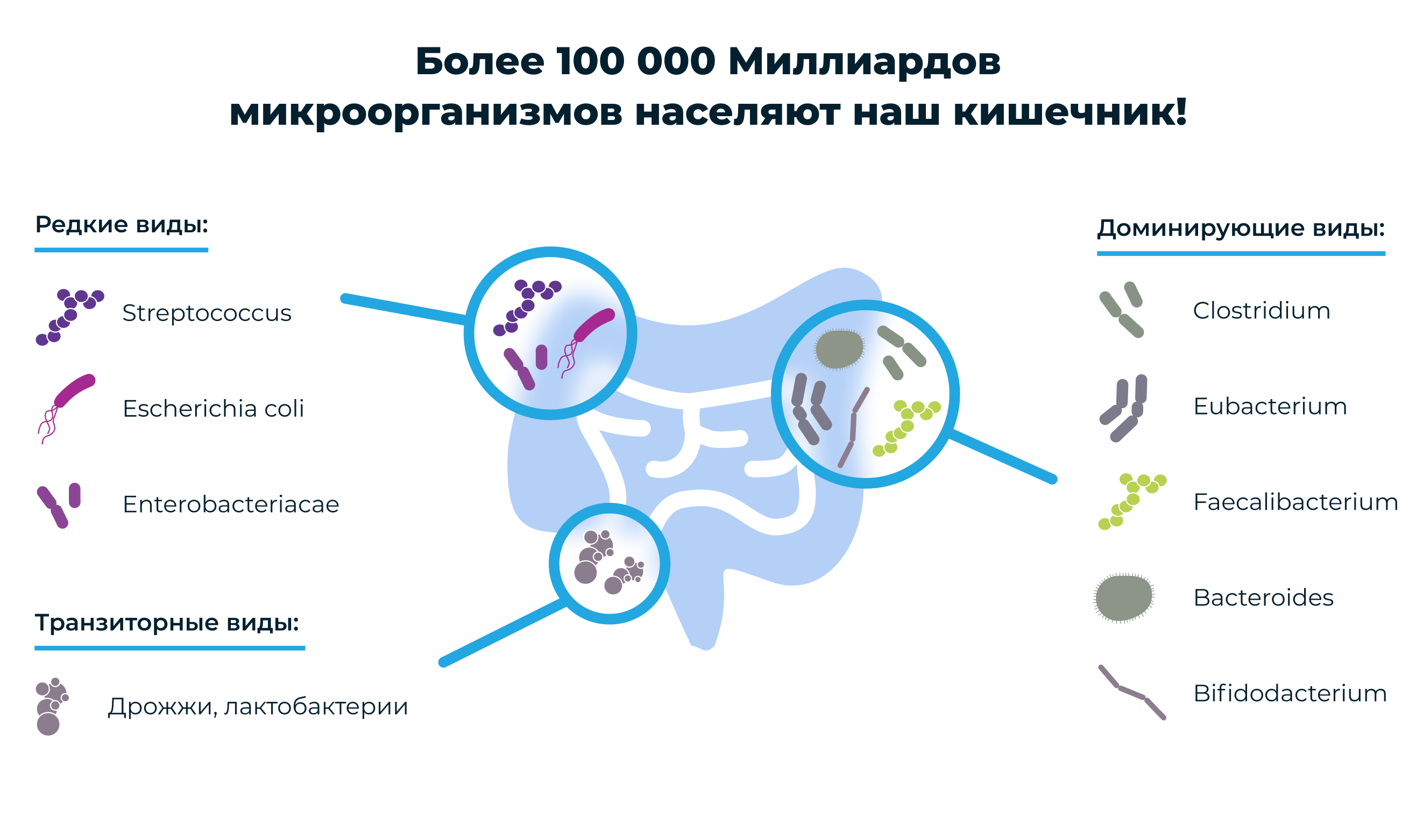
Известно, что в кишечнике здорового человека обитает более 300 видов различных микроорганизмов: бифидобактерии, лактобактерии, непатогенная кишечная палочка и многие другие. Численность этой популяции различается в различных отделах желудочно-кишечного т
Известно, что в кишечнике здорового человека обитает более 300 видов различных микроорганизмов: бифидобактерии, лактобактерии, непатогенная кишечная палочка и многие другие. Численность этой популяции различается в различных отделах желудочно-кишечного тракта (ЖКТ) и достигает максимальных значений в толстой кишке (примерно 1012 микробов в 1 г содержимого) [9]. Состав кишечной микрофлоры достаточно индивидуален и формируется в первые дни жизни ребенка. Важнейшим фактором ее формирования является естественное вскармливание, так как женское молоко содержит ряд веществ (так казываемые «бифидус-факторы»), которые способствуют заселению кишечника отдельными видами микроорганизмов в определенных количествах. Даже незначительные неблагоприятные изменения в организме ребенка в первые дни жизни, особенно патологические состояния ЖКТ, способны вызвать тяжелые, трудно корригируемые в дальнейшем нарушения биоценоза кишечника [6, 8]. В частности, особый ущерб микрофлоре кишечника в этот период могут нанести неправильно выбранное питание и нерациональная антибиотикотерапия [1, 7, 11].
Нарушение микробного равновесия в кишечнике называется дисбактериозом, или дисбиозом, кишечника. Основными причинами дисбактериоза кишечника являются различные заболевания ЖКТ, особенно связанные с нарушением кишечного всасывания, нерациональное питание, антибиотикотерапия (в наибольшей степени — в первые дни жизни) [5, 10].
Дисбактериоз — это не только количественное и качественное изменение кишечной микрофлоры. Согласно отраслевому стандарту, под дисбактериозом кишечника понимают клинико-лабораторный синдром, возникающий при ряде заболеваний и клинических ситуаций и характеризующийся:
В норме избыточному росту бактерий в тонкой кишке препятствуют:
Ведущая роль в формировании дисбактериоза принадлежит нарушению популяционного уровня бифидо- и лактобактерий. Условно-патогенные бактерии, колонизирующие слизистую оболочку кишечника, вызывают нарушение всасывания углеводов, жирных кислот, аминокислот, азота, витаминов, конкурируют с микроорганизмами полезной флоры за участие в ферментации и усвоении питательных веществ, поступающих с пищей. Продукты метаболизма (индол, скатол, сероводород и др.) и токсины, продуцируемые условно-патогенными бактериями, снижают детоксикационную способность печени, усугубляют симптомы интоксикации, подавляют регенерацию слизистой оболочки, способствуют образованию опухолей, угнетают перистальтику и обусловливают развитие диспепсического синдрома [4, 8, 9].
Микрофлора при дисбиозе не способна выполнять в полном объеме физиологические функции, присущие нормальной микрофлоре, и прежде всего противостоять колонизации кишечника экзогенными патогенными микроорганизмами.
Факторы, ведущие к нарушению нормальной флоры кишечника, многочисленны. Дисбактериоз формируется у большинства больных с острыми кишечными инфекциями, вследствие влияния патогенных микроорганизмов на нормальную флору и экологию кишечника, применения антибактериальных препаратов (антибиотиков и сульфаниламидов), подавляющих не только патогенную, но и нормальную микрофлору кишечника [1, 11]. Развитию дисбактериоза способствуют аллергия, воспалительные заболевания пищеварительного тракта (заболевания желудка, протекающие с ахлоргидрией, кишечника, поджелудочной железы, печени, резекция желудка и тонкой кишки, нарушение перистальтики, в частности стаз в толстом кишечнике), стрессы, нерациональное питание и терапия, эндокринные нарушения, ионизирующая радиация. Причинами дисбактериоза могут быть также болезни почек, В12— и фолиеводефицитная анемия, злокачественные новообразования. Дисбактериозы и вторичные иммунодефицитные состояния формируются в условиях возрастающего вредного воздействия окружающей среды на организм человека.
Важно, что дисбактериоз кишечника всегда является вторичным состоянием и, следовательно, требуется поиск первопричины. В свою очередь, дисбактериоз кишечника существенно меняет состав внутренней среды кишки, нарушая пищеварительные процессы, что оказывает повреждающее действие на кишечную стенку. Таким образом, дисбактериоз кишечника нельзя считать безобидным состоянием: он требует к себе пристального внимания [4].
Дисбактериоз кишечника может быть явным (декомпенсированным) и скрытым (компенсированным). Явный дисбактериоз кишечника, как правило, сопровождается нарушениями стула — диареей или запорами. Заподозрить скрытый дисбактериоз кишечника можно у пациента с каким-либо заболеванием ЖКТ, угнетенным состоянием иммунной системы (например, с частыми простудными, инфекционными заболеваниями), а также у больных, получающих массивные курсы антибактериальной терапии.
Устранение дисбактериоза кишечника должно начинаться с лечения первопричины, т. е. того заболевания или состояния, которое вызвало нарушение микробного состава в кишечнике, а также с коррекции питания: в рацион, если позволяет состояние пациента, следует включать достаточное количество пищевых волокон и кисломолочных продуктов. Диета должна быть полноценной по калорийности и содержанию основных ингредиентов. Желательно составить рацион так, чтобы в него входили (конечно, с учетом возраста и состояния больного) изделия из ржи, кукурузы, гречихи, проса, капуста, морковь, кабачки, томаты, огурцы, свежие фрукты, соки без консервантов, орехи, кисломолочные продукты, содержащие живые бифидобактерии и лактобактерии и бифидогенные факторы. В этих продуктах содержатся компоненты питания, обеспечивающие нормальный рост и жизнедеятельность микроорганизмов кишечника, которые называются пребиотиками. Что касается детей первого полугодия жизни, для них крайне важно полноценное грудное вскармливание. При невозможности его обеспечения следует применять адаптированные молочные смеси, содержащие пребиотики [3, 6]. Необходимо также своевременное введение в питание продуктов растительного происхождения.
Этих мер может оказаться достаточно для ликвидации кишечного дисбактериоза, но в ряде случаев приходится назначать специфическую медикаментозную терапию.
В настоящее время для коррекции дисбактериоза наиболее широко применяются препараты, содержащие живые микроорганизмы, положительно влияющие на состав кишечного микробиоценоза, так называемые пробиотики. Собственно probiosis означает сообщество двух организмов, способствующее жизнедеятельности обоих партнеров, probiotic — организм, участвующий в симбиозе. Согласно классическому определению, пробиотики — это живые микроорганизмы, которые благоприятно влияют на здоровье человека, нормализуя его кишечную микрофлору. Пробиотики широко используются в качестве пищевых добавок, в йогуртах и других молочных продуктах, а также в составе лекарственных препаратов. Микроорганизмы, входящие в состав пробиотиков, должны быть непатогенными, нетоксигенными и сохранять жизнеспособность при длительном хранении [9]. Различают следующие основные группы пробиотиков [4]:
С этой целью могут применяться препараты, содержащие микроорганизмы — обычные обитатели кишечника, в том числе бифидо- и лактобактерии, а также микроорганизмы, которые в норме в кишечнике человека не обитают (например, Bacillus cereus IP 5832 или Saccharomyces boulardii). Эти препараты могут быть монокомпонентными, т. е. включать только один вид микроорганизмов, или многокомпонентными. Доказано, что положительный эффект на кишечную микрофлору оказывают следующие микроорганизмы: Lactobacillus (L.) acidophilus, L. GG, L. fermentum, Strepto- (Entero-)coccus faecium SF68, Streptococcus (S.) termophilus, Bifidobacterium (B.) bifidum. В связи с этим для коррекции дисбактериоза кишечника наиболее целесообразно использовать многокомпонентные лекарственные средства, содержащие вышеперечисленные микроорганизмы. Эти препараты обычно назначаются курсами, длительностью не менее 1 мес.
В последние годы все больше используется термин «биотерапевтические агенты» (БТА). БТА представляют собой фармацевтические продукты, состоящие из живых микроорганизмов, обладающих терапевтическими свойствами и использующихся в качестве лекарственных препаратов для профилактики и лечения специфических заболеваний, обусловленных патогенными микробами. Основой для БТА, как правило, являются бактерии — представители нормальной микрофлоры кишечника:B. longum, B. bifidum, B. breve, B. infantis, L. acidophilus, L. plantarum, L. casei, L. bulgaricus, Enterococcus faecium. Использование представителей сапрофитной флоры кишечника в составе БТА обеспечивает положительный и быстрый эффект при приеме препарата, а также гарантирует безопасность для организма ребенка.
Современные бактерийные препараты (бифидумбактерин, лактобактерин, линекс и др.) относятся к категории биотерапевтических, т. е. лечебных препаратов. Механизм действия биотерапевтических препаратов обусловлен наличием у микроорганизмов, входящих в их состав, ряда функциональных свойств: способности выживать в кислой среде, эффективно прикрепляться к эпителиоцитам слизистой стенки кишки и колонизировать ее, продуцировать антимикробные вещества, вызывать стимуляцию иммунной системы, предупреждать избыточный рост и размножение патогенных микробов и восстанавливать нормальную микрофлору кишечника [4].
Продвигаясь по пищеварительному тракту, микроорганизмы сохраняют свою жизнеспособность и обеспечивают временное полезное воздействие на микрофлору кишечника, модифицируя ее состав и метаболическую активность. Пробиотики могут включаться в питание в качестве диетических добавок в виде лиофилизированных порошков, содержащих бифидобактерии, лактобактерии и их комбинации [3].
Эффективность пробиотиков зависит от многих факторов: их состава, состояния микрофлоры организма человека, образа жизни и др. Наиболее часто назначаются и наиболее хорошо изучены пробиотики, изготовленные на основе бифидобактерий и лактобактерий.
Пробиотики должны соответствовать следующим требованиям:
Известно, что соляная кислота и пепсин желудка являются довольно серьезным препятствием для продвижения микроорганизмов. Однако значительная часть бифидо- и лактобактерий, принимаемых перорально, успешно преодолевают этот барьер и в конечном итоге оказываются в толстой кишке. Всего при пероральном приеме сквозь весь пищеварительный тракт проходит от 20 до 40% бифидо- и лактобактерий. Выживаемость бактерий в ЖКТ повышается при одновременном приеме пищи, которая не только снижает кислотность желудочного содержимого и играет роль своеобразного буфера, но и создает благоприятные условия для питания микроорганизмов, выполняя пребиотическую функцию. Несмотря на то, что после приема бактерии обнаруживаются в стуле от 1 до 3 нед, колонизирующая способность бифидо- и лактобактерий в кишечнике невысока. Поэтому для обеспечения постоянного присутствия микроорганизмов в микрофлоре кишечника и достижения стойкого положительного эффекта от применения бифидо- и лактобактерий, содержащие их препараты должны приниматься непрерывно в течение длительного времени и в значительном количестве [3, 9].
Результаты многочисленных исследований подтверждают, что инфекции пищеварительного тракта могут быть предотвращены или излечены при применении бифидо- и лактобактерий. Наибольшие данные накоплены по терапии молочнокислыми бактериями ротавирусных гастроэнтеритов. L. acidophilus быстро устраняет диарею. Этот же штамм показывает высокую эффективность против грибка Candida albicans. Продолжительность диареи, обусловленной вирусной инфекцией, у детей достоверно сокращается после приема L. GG. Также показано угнетающее действие L. acidophilus на сальмонеллы. Подтверждено действие бифидо- и лактобактерий при диарее путешественников [2].
Бифидо- и лактобактерии, применяемые в составе пробиотиков, обеспечивают стабилизацию микрофлоры организма человека, восстанавливают ее нарушенный баланс, а также целостность эпителиальных клеточных образований и стимулируют иммунологические функции слизистой оболочки пищеварительного тракта. Энтерококки и коли-бактерии в большей степени обладают иммуномодулирующим воздействием.
Под синбиотиками понимают комбинацию пробиотиков и пребиотиков, которая оказывает положительный эффект на здоровье организма-хозяина, способствуя выживаемости и колонизирующей способности в кишечнике живых бактериальных добавок и избирательно стимулируя рост и активацию метаболизма лакто- и бифидобактерий.
«Классические» пребиотические препараты содержат живые, но специально обработанные бактерии, представляющие нормальную микрофлору кишечника, которые должны на некоторое время «прижиться» в кишечнике больного ребенка. Это могут быть монопрепараты: содержащие бифидобактерии (бифидумбактерин сухой, биовестин); лактобактерии (лактобактерин, ацилакт); непатогенные эшерихии (колибактерин сухой, ромакол) или их сочетания (линекс, бифиформ, бификол сухой, биовестин-лакто, бифацид, примадофилюс); сенную палочку (споробактерин жидкий, биоспорин); Bacillus cereus (бактисубтил); пропионовокислые бактерии (эвита); лечебные дрожжи Saccharomyces boulardii (энтерол), — или комбинированные — содержащие, кроме живых микроорганизмов, различные добавки в виде сорбентов (бифидумбактерин форте, пробифор), витаминов (нутролин-В), иммунопротекторов (аципол, бифацид, бифилиз сухой, кипацид).
Особую группу составляют препараты, содержащие метаболиты микроорганизмов (дисахариды, органические кислоты) и другие стимуляторы размножения нормальной микрофлоры, к которым относятся парааминометилбензойная кислота (памба, амбен), хилак форте и др.
Важно, что пробиотики назначают не в качестве заместительной терапии, а как средства, обеспечивающие условия для восстановления нормальной микрофлоры. Для лечения дисбактериоза кишечника применяют многочисленные пробиотические препараты.
В последнее время большой интерес вызывают синбиотики, представляющие собой рациональную комбинацию пробиотиков, микробных метаболитов и пребиотиков, которая оказывает положительный эффект на здоровье организма-хозяина, способствуя выживаемости и приживляемости в кишечнике живых бактериальных добавок и избирательно стимулируя рост и активацию метаболизма лакто- и бифидобактерий (нормофлорин-Л, нормофлорин-Б, нормофлорин-Д, гастрофарм, биофлор и др.).
Препараты бифидобактерий — наиболее многочисленная группа пробиотических препаратов, содержащих различные штаммы бифидобактерий (как представителей нормальной микрофлоры кишечника, так и синтетические штаммы). Препараты бифидобактерий применяются для лечения и профилактики дисбиозов, некоторые (бифидумбактерин форте и др.) при лечении антибактериальными препаратами для профилактики антибиотикассоциированного дисбиоза и пр. Бифидобактерии не оказывают токсического действия на организм ребенка, поэтому бифидопрепараты практически не имеют противопоказаний.
Препараты лактобактерий. Действующим началом этих пробиотиков являются живые лактобактерии. Корригирующую терапию лактосодержащими пробиотиками можно назначать совместно или последовательно в течение 2–3 сут после лечения специфическими бактериофагами, предназначенными для элиминации условно-патогенных бактерий, или с химиотерапевтическими препаратами направленного действия.
Нецелесообразно назначать лактосодержащие препараты при средних, выраженных и затяжных формах кандидамикозов, так как продуцируемые лактобактериями кислоты способствуют увеличению количественного состава грибов рода Candida [3].
Колисодержащие препараты изготовлены на основе живых бактерий Escherichia coli штамма М-17, которые обладают антагонистической активностью, иммунокорригирующим действием, оказывают местное и системное протективное действие.
Препараты, содержащие культуры бактерий, обладающих антагонистической активностью. Лечебное действие препаратов из непатогенных представителей рода Bacillus (споробактерин жидкий, бактиспорин, биоспорин, бактисубтил) и лечебных дрожжей Saccharomyces Boulardii (энтерол) обусловлено их выраженными антагонистическими свойствами против широкого спектра патогенных и условно-патогенных микроорганизмов. Эти пробиотики синтезируют комплекс ферментов, стимулирующих пищеварение. Имеются разные точки зрения на применение бактерийных препаратов, содержащих аэробные спорообразующие бактерии. Существуют указания на то, что искусственное введение в кишечник этих бактерий в больших количествах и излишнее размножение бацилл в нехарактерном для них микробиотопе, сопровождающееся распространением бацилл за пределы кишечника, может ухудшить состояние пациента. Поэтому эти препараты рекомендуется назначать кратковременно с последующим применением бифидо- и лактосодержащих пробиотиков.
Комплекс пробиотиков и их метаболитов. Несмотря на довольно широкое использование, бактериальные препараты на основе живых микроорганизмов не всегда оказываются высокоэффективными. Возможно, это связано с быстрой элиминацией вводимых в агрессивную среду штаммов, из-за высокой толерантности иммунной системы к собственной микрофлоре. Высокая себестоимость также ограничивает их применение. Решение проблем коррекции дисбактериозов может заключаться в разработке и во внедрении в клиническую практику принципиально новых препаратов, созданных на основе компонентов микробных клеток или их метаболитов. Такие препараты реализуют свое положительное влияние на физиологические функции и биохимические реакции организма хозяина, либо непосредственно вмешиваясь в метаболическую активность клеток соответствующих органов и тканей, либо опосредованно — через регуляцию функционирования биопленок на слизистых макроорганизма.
Таким образом, коррекция дисбактериоза как у детей, так и у взрослых представляется многогранной проблемой, которая требует учета как первопричины ее возникновения, так и множества сопутствующих факторов. Тем не менее в настоящее время разработаны и внедрены в повседневную практику эффективные средства коррекции состава кишечной микрофлоры, а врач, руководствуясь своими знаниями и опытом, может определить комбинацию, наиболее целесообразную для каждого конкретного пациента.
Литература
С. В. Бельмер, доктор медицинских наук
А. В. Малкоч, кандидат медицинских наук
РГМУ, Москва
Бактисубтил Капсулы, 20 шт
Эубиотик. Бактерии Вacillus cereus IP 5832 выделяют антибакт.
Инструкция
Показания к применению
Противопоказания
Заведомо известная повышенная чувствительность к компонентам препарата.
Инструкция
Состав
Фармакологические свойства
Эубиотик. Бактерии Вacillus cereus IP 5832 выделяют антибактериальные вещества широкого спектра действия, подавляющие развитие патогенных и условно патогенных бактерий, оказывающие противомикробное, противодиарейное действие, восстанавливает кишечную микрофлору. Споры бактерий, содержащиеся в препарате, устойчивы к действию желудочного сока. Их прорастание в вегетативные формы бактерий происходит в кишечнике.
Показания к применению
Противопоказания
Заведомо известная повышенная чувствительность к компонентам препарата.
Применение при беременности и в период грудного вскармливания
Данные о безопасности применения препарата Бактисубтил при беременности не предоставлены.
Способ применения и дозы
Побочное действие
При применении препарата по показаниям в рекомендованных дозах Побочное действиене выявлено.
Передозировка
Случаи передозировки препарата не зарегистрированы. В случае значительного превышения дозы, даже без развития каких-либо симптомов или проявлений необходимо обратиться за медицинской помощью.
Особые указания
Препарат применяется по назначению врача. Пациенты не должны принимать препарат бесконтрольно или по совету третьих лиц.
Что такое пробиотки на самом деле? Интересные факты + полезная таблица
Первое поколение
Монокомпонентные пробиотики, содержащие только один штамм микроорганизмов
Е.coli М-17 ( Колибиктерин )
Bifidobacterium bifidum 791 ( Бифидумбактерин )
Bifidobacterium adolescentis ( Биовестин )
Второе поколение
Bacillus subtilis (Споробактерин)
Bacillus subtilis+Bacillus licheniformis (Биоспорин)
Bacillus cereus IP 5832 (Бактисубтил)
Saccharomyces boulardii (Энтерол)
Третье поколение
Bifidobacterium adolescentis MC-42+ Lactobacillus plantarum (Биовестин лакто)
Bifidobacterium longum + Enterococcus faecium (Бифиформ)
Lactobacillus acidophilus + Bifidobacterium infantis + Enterococcus faecium (Линекс)
Lactobacillus acidophilus + Saccharomyces (Аципол)
Lactobacillus acidophilus LA-5+ Bifidobacterium animalis subs. lactis BB-12 (ФлорОк, ПробиоЛог, Бонолакт)
Lactobacillus plantarum 8Р-А3+ Lactobacillus acidophilus K3Ш24+ Bifidobacterium bifidum 1 (Бифилкт, Бактериобаланс)
Lactobacillus acidophilus + Lactobacillus rhamnosus + Streptococcus thermophiles + Lactobacillus delbrueckii ssp. bulgaricus (Йогулакт)
Четвертое поколение
Bifidobacterium bifidum + активир. уголь (Пробифор, Бифидумбактерин форте)
Bifidobacterium bifidum + Lactobacillus plantarum +активир. уголь (Флорин форте)
Lactobacillus acidophilus LA-5+ Bifidobacterium animalis subs. lactis BB-12 + микрокристаллическая целлюлоза (Линекс форте, ПробиоЛог форте)
Lactobacillus rhamnosus + Lactobacillus acidophilus + гидроксипропилметилцеллюлоза (Примадофилус)
Lactobacillus plantarum CECT 7484+Lactobacillus plantarum CECT 7485+Pediococcus acidilactici CECT 7483 +мальтодекстрим (ПробиоЛог СРК)
Bifidobacterium animalis ssp. Lactis BB-12 + Lactobacillus acidophilus LA-5 + Lactobacillus paracasei LC-01 + Lactococcus lactis R-707-1 (Симбиолакт)
Lactobacillus casei PXN37 + Lactobacillus plantarum PXN47 + Lactobacillus rhamnosus PXN54 + Lactobacillus acidophilus PXN35 + Lactobacillus bulgaricus PXN39 + Lactobacillus helveticus PXN45 + Lactobacillus salivarius PXN57 + Lactobacillus fermentum PXN44 + Bifidobacterium bifidum PXN23 + Bifidobacterium breve PXN25 + Bifidobacterium longum PXN30 + Bifidobacterium infantis PXN27 + Lactococcus lactis ssp. lactis PXN63+ Streptococcus thermophilus PXN66+ целлюлоза микрокристаллическая (Бак-Сет форте)
Lactobacillus paracasei B 21060 или L. rhamnosus GG 10 9 КОЕ, дважды в день;
Lactobacillus acidophilus CL1285 и L. casei LBC80R 5 × 10 10 КОЕ ежедневно 4–10 × 10 10 КОЕ ежедневно
Йогурт с Lactobacillus casei DN114 и L. bulgaricus и Streptococcus thermophilus 10 7 –10 8 КОЕ дважды в день
Saccharomyces boulardii CNCM I-745 5 x 10 9 КОЕ/капсула 250 мг дважды в день
Lactobacillus acidophilus + Bifidobacterium bifidum (штаммы Cultech) 2 × 10 10 КОЕ, один раз в день
Bifidobacterium bifidum MIMBb75 1 × 10 9 КОЕ один раз в день;
Lactobacillus plantarum 299v (DSM 9843) 10 × 10 9 КОЕ один раз в день;
Escherichia coli DSM17252 10 7 КОЕ три раза в день;
Обсудить последние новости со всеми коллегами России вы можете в чатах:
Наш образовательный портал заботится о постоянном повышении квалификации врачей различных специальностей. Перечень дополнительных профессиональных программ повышения квалификации в рамках НМО длительностью 36 часов находится по ссылке. Расписание вебинаров – здесь. Действует удобный поиск по специальностям.
Bacillus cereus ip 5832 что это такое
Биологическая роль цинка многообразна. Он необходим для роста и деления клеток, развития костной ткани, процессов регенерации, репродуктивной функции, развития мозга и поведения. Являясь компонентом более 300 энзимов, цинк принимает участие во всех видах обмена, входит в состав генетического аппарата клетки, представляя около 100 цинксодержащих нуклеопротеидов. Цинк принимает активное участие в процессах регенерации, поскольку необходим для синтеза и стабилизации ДНК.
Как и в случае с медью, несмотря на то что цинк является биогенным (эссенциальным) элементом его избыточное содержание в окружающей среде может приводить к различным патологиям как у человека, так и у животных.
Металлический цинк и его соединения в производственных условиях поступают в организм главным образом через органы дыхания и частично через пищеварительный тракт в результате заглатывания пыли. Более всего изучено токсическое действие паров цинка и мелкодисперсного аэрозоля, которые образуются в процессе плавления металла оксида цинка. При их вдыхании в значительных концентрациях может возникать проф. заболевание – так называемая цинковая, или литейная лихорадка. При хроническом отравлении оксидом цинка могут развиться атрофические и субатрофические изменения слизистой оболочки верхних дыхательных путей, гипохромная анемия, желудочно-кишечные расстройства, нарушения сна, повышенная утомляемость, шум в ушах, снижение остроты слуха. При длительном воздействии пыли оксида цинка на организм человека возможно развитие медленно прогрессирующего пневмокониоза. При длительном вдыхании пыли оксида цинка в значительных концентрациях развиваются умеренные явления пневмосклероза и эмфиземы легких, реже – мелкопятнистая диссеминация в связи с отложением рентгеноконтрастной пыли оксида цинка в легких; возможна уробилинурия и порфиринурия. Раздражающим действием обладают также сульфат и стеарат цинка. Сухой сульфат цинка и его концентрированные растворы вызывают изъязвления кожи кистей рук, особенно их тыльной поверхности, по типу так называемых птичьих глазков. Получены экспериментальные данные об онкогенном действии цинка и его соединений. Острое отравление соединениями цинка отмечали при вдыхании оксида цинка в высоких концентрациях (например, при нагревании металлического цинка выше температуры его плавления). У пострадавших появляется сладковатый привкус во рту, через 1-5 часов возникает сильная жажда, болезненное стеснение в груди, сухой кашель, озноб и другие признаки литейной лихорадки. При вдыхании аэрозоля хлорида цинка может развиться отек легких. При отравлении растворимыми солями цинка через рот у пострадавших также отмечают металлический вкус во рту, наблюдается тошнота, слюнотечение. развивается ожог слизистой оболочки рта, пищевода, желудка, появляются рвота с примесью крови, боль в животе, понос, резкое возбуждение, непроизвольные подергивания отдельных групп мышц, судороги икроножных мышц, возможен коллапс и шок. При более длительном течении отравления развивается острая почечная недостаточность [1, 2, 3].
Значительные концентрации увеличения цинка наблюдаются в восточной части Оренбуржья, что напрямую связано в развитой горнодобывающей и металлургической промышленностью. При этом в ряде районов его содержание превышено в десятки раз по отношению к предельно допустимым концентрациям [4. 5].
Выше изложенное является критерием для изучения влияния свинца на рост микроорганизмов входящих в состав почв и пробиотических препаратов (см. рис.).
Для реализации поставленной задачи в качестве объектов исследования нами были использованы 6 пробиотических препаратов на основе бактерий рода Bacillus: Споробактерин (B. subtilis 534), Бактисубтил (B. cereus IP 5832), Ветом 1.1 (B. subtilis 10641), Ветом 2 (B.licheniformis 7038), Ветом 3 (B. amyloliquefaciens 10642), Ветом 4 (B. amyloliquefaciens 10643). В качестве регулирующих факторов в работе использовались различные соли (нитраты, хлориды, ацетаты и оксиды) свинца.
Влияние Zn(CH3COO)2 на рост исследуемых микроорганизмов: 1 – B. subtilis 534, 2 – B. cereus IP 5832, 3 – B. subtilis 10641
Для выполнения данного этапа работы использовали метод агаровых лунок, выбор данного метода объясняется тем, что он позволяет не только визуально, но и качественно оценить влияние тяжелых металлов на рост исследуемых микроорганизмов.
Методика выполнения заключается в следующем: изучаемый микроорганизм высевали сплошным «газоном» на поверхность агаровой пластинки (1,5% МПА) в чашке Петри. После этого, пробочным сверлом (диаметр 5 мм) вырезали агаровые блочки, при этом на одной чашке Петри можно разместить до 7 агаровых лунок в которые в последующем вносили исследуемые концентрации веществ для оценки их ингибирующего и субингибирующего эффекта. Чашки помещали в термостат на 24 часа при температуре 37 °C (благоприятной для развития исследуемого тест-организма). После инкубирования производили визуальную оценку действия исследуемого металла на рост популяции. Отсутствие зон подавления роста свидетельствовало о отсутствии влияния либо соли в целом (как правило данное явление отмечалось у солей с низки уровнем диссоциации), либо определенной концентрации (именно такие концентрации в дальнейшем использовались в качестве рабочих). В том случае если исследуемое вещество обладало высокой активностью в отношении исследуемого микроорганизма регистрировали значительные зоны подавления роста вокруг лунки.
Данные, представленные на рисунке, свидетельствуют о том, что избыточные концентрации катионов цинка не оказывают выраженного бактерицидного эффекта в отношении исследуемых микроорганизмов, однако по мере удаления от лунки наблюдается отсутствие роста популяции бактерии, что в свою очередь свидетельствует о ингибирующем эффекте низких концентраций цинка. Обобщенные данные по изучению влияния катионов цинка на исследуемые микроорганизмы представлены в таблице.
Оценка влияния солей цинка на рост бактерий рода Bacillus