Таннат железа что это
Новое поколение препаратов железа – бисглицинат (хелат) железа
Распространенность анемии
Значимость анемии как проблемы современного мира не вызывает сомнений. Несмотря на все достижения цивилизации, дефицит железа является основным и наиболее распространенным нарушением питания в мире. Дефицит железа, от которого страдают многие дети и женщины в развивающихся странах, является единственным видом недостаточности питательных веществ, который также в значительных масштабах распространен в экономически развитых странах. Уровни его распространенности поражают: 2 миллиарда человек, то есть более 30% населения мира, страдают от анемии. 1
Среди анемий ведущими являются железодефицитные, составляя в структуре у женщин до 90% и среди мужчин — до 80%. Важным является высокая распространенность среди населения латентного дефицита железа, которая колеблется от 19,5% до 30%, кроме того, от 50% до 86% женщин имеют факторы риска развития анемии.
Железодефицитная анемия (ЖДА) — заболевание системы крови, обусловленное дефицитом железа в организме, сопровождаетcя изменениями параметров его метаболизма, уменьшением концентрации гемоглобина в эритроцитах, количественными и качественными их изменениями и клинически выражается анемической гипоксией и сидеропенией.
Сидеропения и развивающаяся в последующем тканевая и гемическая гипоксия приводят к расстройствам сердечно-сосудистой (миокардиодистрофия и нарушение кровообращения различной степени), нервной системы (вегетативно-сосудистые, вестибулярные нарушения, астенический синдром), снижению детородной функции женщин, а также развитие осложнений во время беременности и родов, изменению интеллекта и поведенческих настроений, хронизацию различных заболеваний и как следствие снижение работоспособности и ухудшение качества жизни. 4
Эволюция синтетических лекарственных средств терапии железодефицитной анемии
Фармакотерапия ЖДА базируется на введение в организм железа из состава железосодержащих лекарственных средств. Выбору препарата для коррекции сидеропении придается особое значение, так как важна не только эффективность, но и отсутствие побочных реакций и осложнений при их применении.
Существует условное деление препаратов железа на двух- и трёхвалентные. Однако, сама по себе валентность железа не представляет какой-либо ценности.
Известно, что всасывание железа в кишечнике возможно лишь тогда, когда микроэлемент находится в двухвалентной форме, которая способна проходить через клеточную мембрану слизистой оболочки кишечника. Низкое значение рН желудочного содержимого способствует растворению алиментарного железа и переходу трехвалентного железа (окисное) в двухвалентную форму (закисное). 17
При поступлении желудочного содержимого в кишечник рН пищевого комка повышается и в отличие от ферро-иона (Fe2+), ферри-ион (Fe3+) образует нерастворимые соли. В этих условиях только муцин, хелатируя железо, способен поддержать ферри-ион в растворимом состоянии. 4
Таким образом, соединения железа в составе препаратов должны обладать хорошей растворимостью, высокой биодоступностью, достаточным содержанием элементарного железа и малой токсичностью. Рассмотрим особенности абсорбции каждой из трёх известных групп препаратов железа.
Первое поколение препаратов железа
Одной из первых групп препаратов железа стали применять ионные соли двухвалентного железа. Эта группа характеризуется довольно быстрым наступлением эффекта в плане повышения гемоглобина и улучшения гемодинамических показателей в периферической крови.
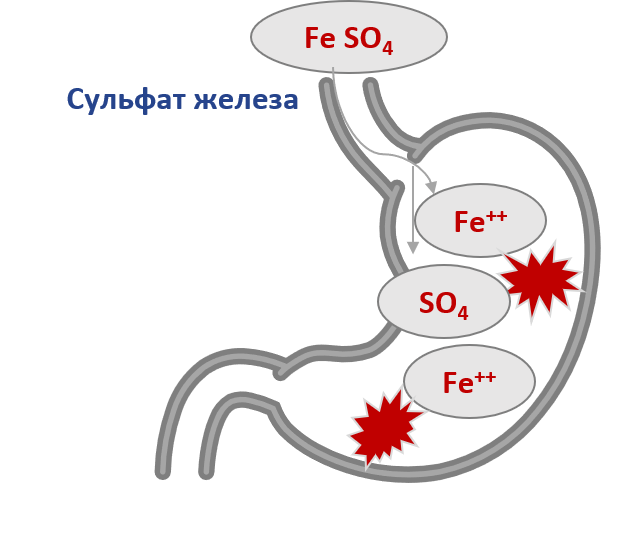
Тем не менее, лечение ионными препаратами железа, в частности сульфатом железа, вызывает побочные реакции у 44,7% пациентов. Чаще всего страдает желудочно-кишечный тракт (ЖКТ). Симптомы дисфункции его верхних отделов обычно проявляются в течение часа после приема лекарства и могут протекать как в легкой (тошнота, дискомфорт в эпигастрии), так и в тяжелой форме — с болью в животе и/ или рвотой. Кроме того, ферротерапия солевыми препаратами железа нередко сопровождается появлением металлического привкуса в течение первых дней лечения, потемнением зубной эмали и десен, возможны также диарея или запор. хорошо известно, что солевые препараты железа в просвете кишечника взаимодействуют с компонентами пищи, лекарствами, затрудняя абсорбцию в том числе и железа. В связи с этим, их рекомендуют назначать за 1 час до приема пищи, однако это усиливает повреждающее действие соединений Fe2+ на слизистую кишечника, вплоть до развития ее некроза. 5
Причиной возникновения данных побочных явлений является гидролиз солей железа в желудке. Под действием желудочного сока ионные соли железа подвергаются гидролизу(диссоциации) в желудке, в результате чего свободные молекулы железа негативно воздействуют на слизистую оболочку ЖКТ и провоцируют возникновение побочных эффектов: тошнота, боль в животе, металлический привкус во рту, диарея/запор.
Второе поколение препаратов железа
Абсорбция железа в виде гидроксид-полимальтозного комплекса (ГПК) железа-III имеет принципиально иную схему по сравнению с его ионными соединениями и осуществляется путем активного всасывания при конкурентном обмене лигандами, уровень которых определяет скорость абсорбции железа Fe3+. Неионная структура, обеспечивающая стабильность комплекса и перенос железа с помощью транспортного белка, предотвращает в организме свободную диффузию ионов железа, то есть прооксидантные реакции. Однако биодоступность полимальтозного комплекса железа-III самая низкая среди всех препаратов железа, всего 10–15%.
В связи с большим размером молекулы (55 kDa), ее пассивная диффузия примерно в 40 раз медленнее, чем у ионов железа. 6 Такую низкую биодоступность приходится компенсировать большими суточными дозами ГПК.
Новое поколение препаратов железа — новое решение проблемы анемии
С конца 90-х начала 2000-х годов начали активно внедрять применение хелатных комплексов железа для терапии дефицита железа и анемии у людей. Хотя данная группа препаратов появилась гораздо раньше, и использовалась изначально в качестве пищевых добавок и в ветеринарии.
В 1893 году Альфред Вернер выдвинул постулат о новой молекулярной структуре, характеризующей эти стабильные молекулы. Спустя несколько лет, в 1920 году Морган и Дрю применили термин «хелат» к молекулярной структуре, постулированной Вернером. 7
Хелаты металлов представляют собой комплексные соединения металла с аминокислотой.
В отличие от солей металлов, лиганд в хелатном комплексе отдает электроны катиону, делая тем самым молекулу ионно-нейтральной, устойчивой к разным факторам, действующим в желудочно-кишечном тракте (рН, пища), а низкая молекулярная масса способствует максимальному усвоению железа при пероральном приеме. 8
Хелатные комплексы легче проникают через стенку кишечника и лучше усваиваются, не нарушая ионный и минеральный баланс клетки. 10
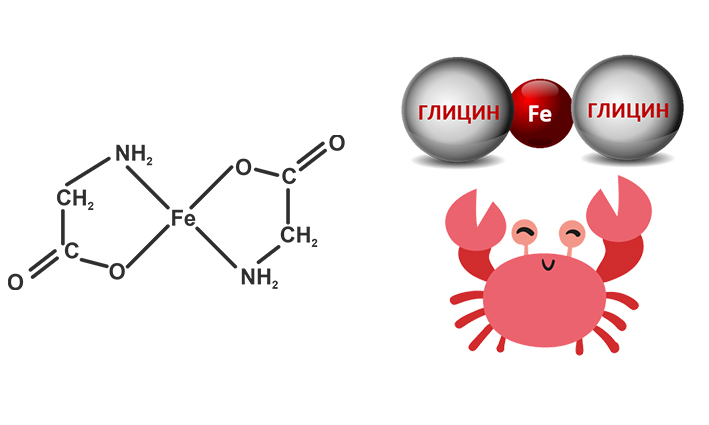
Бисглицинат железа состоит из одной молекулы железа, которая соединена с карбоксильными группами двух молекул глицина при помощи ковалентных связей.
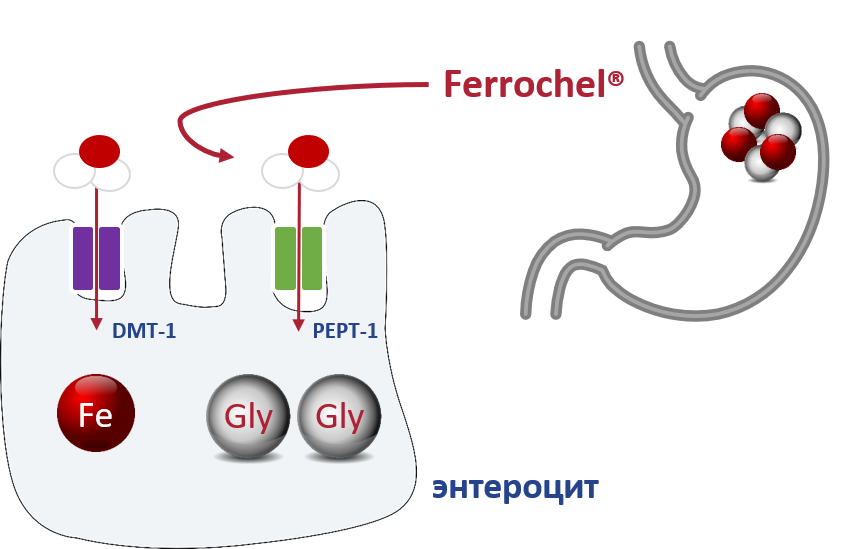
Соотношение железа к лиганду 1:2 нейтрализует валентность железа, что обеспечивает его стойкость к разным факторам, действующим в желудочно-кишечном тракте (рН, пища). Поэтому соединение хелата не поддается гидролизации в желудке, полностью абсорбируется в тонком кишечнике и в неизмененном виде попадает внутрь энтероцитов, где и происходит высвобождение молекулы железа. 8
Бисглицинат железа — это источник негемированного железа. После перорального применения соединение в неизмененном виде попадает в энтероциты, где гидролизируется на железо и глицин. Стабильность соединения бисглицината железа объясняется тем, что оно не гидролизируется при разных значениях рН, а низкая молекулярная масса (204 г/моль) способствует максимальному усвоению железа при пероральном приеме. 8
В составе Multizan ® Феррум бисглицинат железа представлен запатентованным комплексом Ferrochel ® компании Albion Minerals — мировым лидером и новатором в области минерального аминокислотного хелатного питания.
Уникальная гамма хелатных минералов Albion ® :
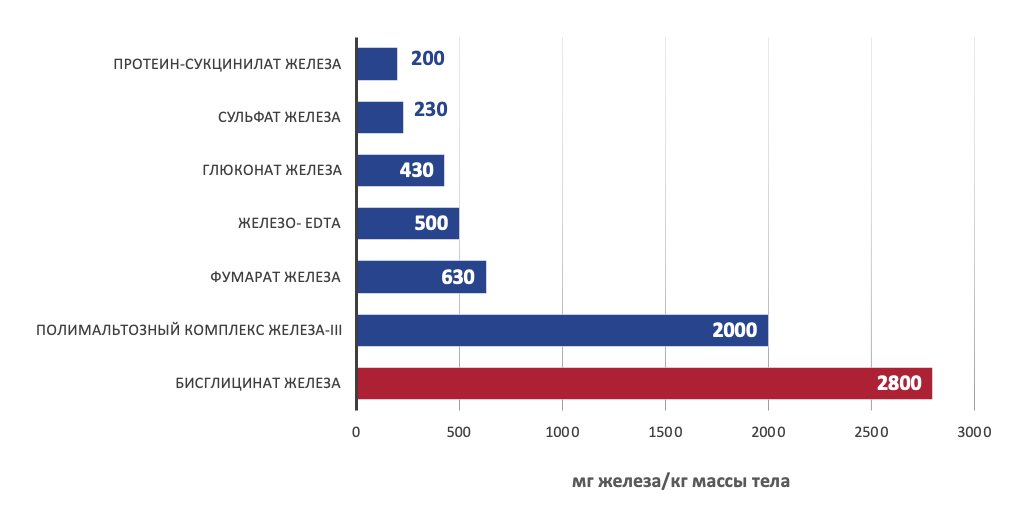
Даже с повышенной биодоступностью бисглицинат железа безопасен. Всасывание контролируется запасами железа в организме, при этом большие количества обычно усваиваются людьми с более низким статусом железа. Организм, страдающий железодефицитной анемией, может потреблять 90% железа, в то время как организм, не страдающий железодефицитной анемией, может потреблять всего 10%, или ровно столько, сколько необходимо организму для компенсации потерь в метаболизме. Было обнаружено, что бисглицинат железа Ferrochel ® в 2,6 раза безопаснее, чем сульфат железа, и безопаснее, чем обычное неорганическое железо, содержащееся в пищевых продуктах и пищевых добавках. 13
Сравнительная таблица доз LD50 (cредняя доза вещества, вызывающая гибель половины членов испытуемой группы) различных препаратов железа при пероральном введении белым мышам. 14, 15, 16
Сывороточное железо (венозная кровь) в Сортобе
Лабораторное исследование для определения уровня сывороточного железа. Железо — один из самых важных микроэлементов, дефицит или переизбыток которого представляют угрозу для организма человека.
Приём и исследование биоматериала
Комплексы с этим исследованием
Когда нужно сдавать анализ Сывороточное железо?
Подробное описание исследования
Сывороточное железо — это микроэлемент, который не вырабатывается в организме человека самостоятельно, а поступает только извне с пищей.
Железо входит в состав:
Также железо участвует в клеточном обмене, в работе иммунной системы, входит в состав некоторых ферментов, обеспечивая нормальное протекание в них метаболических реакций, а также участвует в синтезе ДНК.
Всего в организме находится не более 5г железа. Оно поступает с пищей из животных и растительных источников. Это так называемое гемовое (содержится в мясных продуктах, в составе гемоглобина) и негемовое (ферменты и белки растительной пищи) железо. Из общего количества железа, которое поступило в организм, всасывается всего около 10%. Процесс всасывания происходит в двенадцатиперстной кишке.
В плазме крови человека большая часть железа находится в окисленном трехвалентном состоянии в связке с белком трансферрином. Трансферрин переносит железо к тканям и органам. Большая часть поступающего железа уходит на образование гемоглобина, а оставшаяся часть депонируется (запасается). Основное депо железа в организме — это специальные белковые комплексы «ферритин» и «гемосидерин». Отсюда железо расходуется в случае его снижения в сыворотке крови. Восстановление железа сыворотки крови зависит от степени наполнения депо. При длительной нехватке железа его запасы истощаются, что может привести к анемии. Данный механизм регуляции обеспечивает самосохранение.
Концентрация сывороточного железа — важный биохимический показатель, изменение которого может указывать на возможные проблемы обмена этого микроэлемента.
Дефицит железа встречается чаще, чем его переизбыток. Как правило, человек не замечает, что у него развивается анемия — патологическое снижение концентрации гемоглобина крови. Обычно это становится заметно, когда концентрация гемоглобина становится ниже 100 г/л. Тогда человек может жаловаться на повышенную утомляемость, головокружение, выпадение волос, бледность кожи и ломкость ногтей. В некоторых случаях люди отмечают ощущение покалывания и жжения кончика языка.
Если не предпринимать никаких действий, направленных на восстановление депо железа, дальше развивается одышка, рассеянность внимания, учащенное сердцебиение (тахикардия).
Подобные состояния наблюдаются при онкологических заболеваниях (особенно если поражен кишечник), железодефицитных анемиях, желтухе, острых и хронических инфекциях, язвенной болезни и язвенном колите. Дефицит железа часто может быть вызван хронической кровопотерей при геморрое. При целиакии, болезни Крона и в послеоперационном периоде также диагностируют анемию. Концентрация железа у женщин изменяется в зависимости от фазы менструального цикла.
Также встречается так называемая «анемия беременных» — состояние при котором снижается концентрация сывороточного железа у беременных женщин. Как правило, во втором триместре, когда формируется депо железа у плода. Это состояние также требует особого наблюдения.
Переизбыток железа встречается реже и характеризуется следующими симптомами: боли в животе и суставах, нарушение сердечного ритма, а также, схожая с анемией, усталость.
Для нормальной работы всех органов и систем необходимо, чтобы с пищей в день поступало не менее 1 мг железа. Продукты питания богатые этим микроэлементом: мясо и субпродукты (свиная печень), бобовые (чечевица, фасоль), зелень (шпинат, сельдерей), фрукты (гранат, яблоки). Аскорбиновая кислота улучшает процесс всасывания железа, поэтому рекомендуется употреблять ее вместе с железосодержащими продуктами. Помешать усвоению железа могут молочные продукты и кофеин.
Диета при низком уровне железа и ферритина
Железо и железное здоровье: какую роль микроэлемент играет в нашем организме
Железо входит в состав гемоглобина. В свою очередь, белок гемоглобин является строительным материалом для эритроцитов — красных кровяных клеток, которые переносят кислород от легких к органам, а на обратном пути избавляют их от углекислого газа. Собственно, этот процесс и называется клеточным дыханием. Без железа он невозможен. А поскольку каждая клетка нашего тела нуждается в кислороде, железо можно назвать одним из самых важных элементов.
На синтез гемоглобина уходит 60–70% всего поступающего в организм железа. Оставшиеся 30–40% депонируются в тканях и тратятся на решение других задач — на обменные процессы, регуляцию работы щитовидной железы, поддержание защитной системы организма и синтеза соединительной ткани.
Как видите, функции железа разнообразны и многочисленны, однако транспорт кислорода — самая главная из них.
Железо плохо усваивается даже при идеальном здоровье и правильном рационе — человеческий организм способен усвоить до 10% железа, поступающего с пищей.
Суточная потребность в железе у здоровых людей
Потребность в железе меняется в зависимости от возраста и состояния здоровья.
У младенцев до полугода потребность в железе невелика, так как они рождаются с изрядным запасом этого элемента. Новорожденным нужно только 0,27 мг железа в сутки. Детям от полугода до года требуется 11 мг, малышам от 1–3 лет — 7 мг, детям в возрасте 4–8 лет — 10 мг, 9–13 лет — 8 мг.
Подростки 14–18 лет должны получать 11–15 мг ежедневно, причем у девушек потребность в железе выше — это связано с ежемесячными кровопотерями во время менструаций.
Мужчинам требуется около 10 мг железа в сутки, женщинам — 15–18 мг. Во время беременности норма повышается до 25–35 мг, а при грудном вскармливании — до 25 мг.
Примерно после 50 лет норма содержания железа для мужчин и женщин становится одинаковой — около 10 мг в сутки.
Это усредненные цифры, однако в некоторых случаях потребность в железе может быть немного выше среднестатистической. Больше железа требуется спортсменам, а также людям, занятым тяжелым физическим трудом. Потребность в железе возрастает и во время восстановления после операций и травм (особенно если они сопровождались кровопотерей), инфекционных болезней, а также для тех, кто страдает постоянными кровотечениями (при геморрое, язве желудка, носовых кровотечениях, обильных менструациях и пр.).
Продукты с высоким содержанием железа
Наш организм не может синтезировать железо, он лишь перерабатывает этот элемент, извлекая его из отслуживших свое эритроцитов. «Свежее» железо поступает с едой. Однако даже если вы употребляете продукты, содержащие железо, это еще не значит, что вам его хватает. Все дело в том, что существует два вида железа.
Железо может быть гемовым (двухвалентным) и негемовым (трехвалентным). Первое содержится в продуктах животного происхождения и легко усваивается (примерно на 25%), второе входит в состав растений и усваивается всего на 8–10% максимум[3]. Именно поэтому веганы и вегетарианцы часто испытывают нехватку этого элемента, даже если едят продукты, богатые железом.
И все же именно правильная диета считается основным способом профилактики железодефицита. Железо в значимых дозах содержится в следующих продуктах:
Продукты животного происхождения:
Продукты растительного происхождения:
Несмотря на то, что содержание железа в некоторых растительных продуктах высоко, негемовая форма железа усваивается плохо. Потому тем, кто придерживается растительной диеты, важно проверять уровень железа и при необходимости принимать пищевые добавки, которые содержат этот элемент.
Лучше всего наш организм воспринимает железо, полученное из мяса (в среднем усваивается 20%), чуть хуже — из рыбы и морепродуктов (около 11%), бобовых (7%) и орехов (6%). Из фруктов, овощей и круп усваивается лишь 1-3% железа.
Для улучшения усвоения железа важно также получать в нужном количестве витамины и минералы, которые играют роль катализаторов и помогают этому элементу всасываться. К ним относятся:
Правила рационального питания
Чем больше разнообразных продуктов вы будете использовать в приготовлении пищи, тем меньше шансы заработать себе дефицит железа или какого-либо другого микроэлемента или витамина. Однако диета при нехватке железа содержит в себе и некоторые ограничения. Дело в том, что некоторые элементы могут ухудшать всасывание этого минерала. Это не значит, что от них нужно совсем отказываться. Но лучше не есть продукты, содержащие железо, одновременно с:
Если ваша задача — повысить содержание железа в крови, ешьте все вышеуказанные продукты только через 3–4 часа после продуктов с высоким содержанием железа. А вот от жирного и жареного, готовых масляных соусов, таких как майонез, острых специй и маринадов следует отказаться — все это раздражает слизистые оболочки ЖКТ и мешает железу усваиваться.
Пример рациона на сутки: «железный» день у меня сегодня…
Как составить меню, которое поможет справиться с железодефицитом? На самом деле это не сложно. Продукты, богатые железом и витаминами, необходимыми для его всасывания, не являются ни редкими, ни особенно дорогими. Вот пример «железного» рациона на один день:
Завтрак: 2 яйца всмятку или омлет, салат из свежей капусты, ломтик черного хлеба с маслом и твердым сыром, апельсиновый сок.:
Второй завтрак: творожный мусс с курагой и черносливом или овсянка с сухофруктами, отвар шиповника. :
Обед: куриный суп или борщ с грибами, тушеная печень с луком или запеченная индейка с овощным рагу, фруктовый салат и компот из сухофруктов. :
Ужин: паровые биточки из говядины или запеченная в фольге скумбрия, гороховое пюре или тушеная морковь, успокаивающий травяной чай.:
Такое меню не только богато железом, витаминами C, B9 и медью, оно еще и вполне подходит под определение диетического, содержит достаточное количество клетчатки и не повредит вашей фигуре.
Нормы потребления железа пациентами с анемией
Иногда анализы выявляют не просто нехватку железа, но более серьезную ситуацию — железодефицитную анемию. Обычно такое состояние развивается на фоне заболеваний ЖКТ, опухолевых процессов, глистных инвазий, постоянных кровотечений. Оно часто диагностируется у людей, переживших значительную кровопотерю во время травмы или операции.
Железодефицитную анемию диагностируют в том случае, если уровень гемоглобина падает до 100–70 г/л, а сывороточный ферритин понижается до 15 нг/мл.
При диагностированной железодефицитной анемии назначать себе лечение самостоятельно нельзя. Терапию подбирает врач. Возможно, он назначит поливитаминные комплексы и биодобавки с железом, а в самых тяжелых случаях он может выписать даже препараты железа — довольно сильные средства с многочисленными побочными эффектами. Принимать такие лекарства можно только под контролем лечащего врача.
ОЖСС (Сывороточное железо, ЛЖСС) (венозная кровь) в Москве
Лабораторное исследование для определения общей железосвязывающей способности сыворотки (ОЖСС) с целью определения количества железа, которое может переносить кровь. Используется в дифференциальной диагностике анемий, а также состояний, связанных с нарушением метаболизма железа в организме.
Приём и исследование биоматериала
Комплексы с этим исследованием
Когда нужно сдавать анализ ОЖСС (Сывороточное железо, ЛЖСС)?
Подробное описание исследования
Гемоглобин, миоглобин, а также некоторые важные ферменты содержат микроэлемент железо (Fe). Человек получает железо из продуктов животного и растительного происхождения. Далее микроэлемент всасывается в кишечнике и транспортируется с помощью специального белка трансферрина, вырабатываемого клетками печени. Этот белок имеет особую структуру — на его поверхности существуют центры связывания железа. Fe заполняет треть связующих центров трансферрина, свободная часть остается в резерве. Уровень трансферрина связан с состоянием печени и особенностями рациона питания, присутствия в нем железосодержащих продуктов.
Общая железосвязывающая способность сыворотки крови (ОЖСС) отражает количество железа, способного связаться с трансферрином. Показатель используется для ранней диагностики железодефицита. Для проведения исследования к анализируемой сыворотке крови добавляют железо до того момента, пока все связующие центры трансферрина не будут заполнены микроэлементом. Далее оценивают количество железа, которое связалось с трансферрином. Это количество характеризует степень дефицита железа и отражает количество трансферрина в крови.
ОЖСС — сумма сывороточного железа и латентной железосвязывающей способности сыворотки. ЛЖСС характеризует трансферрин, не связанный с железом. Данные показатели используются в диагностике анемий, т.е. состояний, связанных с уменьшением количества эритроцитов и снижением содержания гемоглобина в единице объема крови.
Если железа в организме недостаточно, концентрация трансферрина увеличивается, также увеличивается и ЛЖСС. Тогда как при избытке железа трансферрин практически полностью заполнен микроэлементом, а значит, ЛЖСС снижается.
Дефицит железа может возникнуть в результате:
На ранней стадии дефицита железа клинические симптомы, как правило, не выражены. Однако по мере прогрессирования дефицита начинают появляться:
В случае анемии данные исследования помогают определить причины развития патологии: недостаточное поступление железа в составе пищи, недостаток витаминов, наличие хронических заболеваний и пр.
Избыток железа опасен не меньше, чем его дефицит, потому как в больших концентрациях микроэлемент токсичен для организма. Избыточное количество железа может накапливаться по причине:
1. Длительного приема неадекватных доз препаратов, содержащих железо;
2. Множественных переливаний крови;
3. Наличия поражений печени, вызванных хроническим злоупотреблением алкоголя или инфекционными заболеваниями.
Также возможно наличие наследственной патологии, ассоциированной с избыточным накоплением железа в организме и его последующим токсическим действием (гемохроматоз). Если в организме накапливается избыточное количество железа, его сывороточная концентрация увеличивается. Показатель ОЖСС при этом находится в пределах нормы или уменьшается.
Клинические симптомы избыточного накопления микроэлемента включают:
1. Суставные и мышечные боли;
2. Потерю веса;
3. Слабость;
4. Нарушение сердечного ритма.
Как правило, исследование назначается для оценки обмена железа в комплексе с другими анализами крови с целью установления диагноза и проведения адекватной терапии.
Железодефицитная анемия
Дефицит железа представляет собой наиболее частую причину анемии и чаще всего связан с хронической кровопотерей. Мальабсорбция, развивающаяся на фоне операций на ЖКТ, воспалительных заболеваний кишечника и целиакии, вызывает железодефицит намного реже. Симптомы железодефицитной анемии являются очень неспецифичными, и изменения лабораторных показателей является главным маркером развивающегося заболевания.
Метаболизм железа в организме
Железо представляет собой один из важнейших микроэлементов организма человека в связи с его участием в широком спектре метаболических процессов, включая транспорт кислорода, синтез молекул ДНК и транспорт электронов через мембрану клетки. Гомеостаз железа в организме поддерживается путем тщательного регулирования адсорбции железа в проксимальном отделе тонкого кишечника для компенсации его потерь в ходе метаболических процессов. Длительное нарушение баланса железа в организме ведет к развитию либо гемосидероза (повышение концентрации железы), либо железодефицитной анемии.
Железодефицитную анемию может вызывать как снижение адсорбции железа в кишечнике, так и повышенная скорость потери микроэлемента. Снижение адсорбции чаще возникает в связи с уменьшением количества потребляемого усваиваемого железа. Кровопотеря (геморрагия) является наиболее частой причиной повышенной потери железа организмом, однако гемоглобинурия с интраваскулярным гемолизом также может быть причиной железодефицитной анемии. Мальабсорбция железа представляет собой относительно редкую причину анемии, связанную с тяжелым поражением тонкого кишечника (целиакия, воспалительные заболевания кишечника, региональный энтерит) или с постоперационными осложнениями операций на ЖКТ.
Для захвата железа в проксимальном отделе кишечника существует 3 различных механизма. Первый механизм предназначен для железа, входящего в состав гема, второй – для трехвалентного железа, третий – для двухвалентного. В Российской Федерации и Европе треть всего потребляемого организмом железа приходится на железо в составе гема, однако остальные две трети попадают в организм через потребляемый гемоглобин. Железо в составе гема находится в нехелатированном состоянии и преципитируется множеством других соединений (фосфатами, таннатами, оксалатами), содержащихся в продуктах питания, что нарушает его всасывание в кишечнике. Растворимость и доступность гема для всасывания поддерживается продуктами деградации глобина, который разрушается ферментами поджелудочной железы. Гемовое и негемовое железо всасывается энтероцитами неконкурентно.
Гем попадает в клетку в виде интактного металлопорфирина, вероятнее всего везикулярным механизмом транспорта. Гем разрушается внутри энтероцита гемовой оксигеназой с последующим выделением железа. Образовавшееся свободное гемовое железо проникает конкурентно с негемовым через базолатеральную стенку энтероцита для связывания с трансферрином в плазме крови.
Трехвалентное железо использует отличный от двухвалентного механизм проникновения в клетку. Это было доказано путем исследования с конкурентным ингибированием, при котором использовались блокирующие антитела против дивалетного транспортера-1 металлов (DMT-1) и против бета3-интегрина, а также в экспериментах с трансфекционными моделями. Данные исследования показали, что трехвалентное железо использует бета3-интегрин и мобилферрин для проникновения в клетку, а двухвалентное железо – белок DMT-1.
Каким путем транспортируется большее количество негемового железа в организм неизвестно. Большая часть негемового железа в рационе человека представлена трехвалентным железом.
Существует также ряд вспомогательных белков, которые также участвуют в адсорбции железа. Стимулятор транспорта железа, гепсидин, увеличивает абсорбцию трехвалентного и двухвалентного железа и играет важную роль в переносе железа из энтероцита в плазму крови. Однако, взаимосвязь и точный механизм действия данных белков до сих пор до конца не ясен.
Концентрация железа внутри энтероцитов находится в прямой зависимости от потребности организма в железе. При специфической окраске эпителия тонкой кишки пациентов с железодефицитом в энтероцитах железо не визуализировалось. Однако у людей с достаточным уровнем железа окраска энтероцитов происходила очень выражено. Изменение концентрации ионов железа внутри энтероцитов может вызывать повышение синтеза рецепторов или сатурацию железо-связывающих белков.
В отличие от железодефицита, при повышенном эритропоэзе (например, при гипоксии) железо быстро адсорбируется без изменения его концентрации в энтероците. Эндотоксины и цитокины изменяют адсорбцию иным механизмом, что, возможно, объясняется балансом активности гепсидина и эритропоэтина.
Большая часть железа, которая доставляет к клеткам организма, связана с трансферрином. Трансферрин использует два механизма проникновения через мембраны: классический путь через рецепторы трансферрина (высокая афинность, низкая эффективность) и независимый от рецептора путь (низкая афинность, высокая эффективность).
В классическом трансферриновом пути комплекс железа с трансферрином попадает в клетки вместе с эндосомой. Последующее закисление эндосомы приводит к высвобождению железа из белкового комплекса и его попадание в цитоплазму клетки. После этого апотрансферрин доставляется из эндосомы в плазму для реутилизации. Точный механизм доставки железа в клетки с помощью независимого от рецептора пути до конца неизвестен. Клетки организма также могут доставлять железо посредством мобилферрина и белка DMT-1. Их функции в отсутствии трансферрина, сатурированного железом, не до конца ясны. Однако их присутствие в данных клетках предполагает, что они могут участвовать во внутриклеточном регулировании гомеостаза железа.
Этиология железодефицитной анемии
Факторы диеты
Мясо является главным источником гемового железа, который менее подвержен ингибирующему эффекту других соединений, находящихся в пище, по сравнению с негемовым железом. Распространенность железодефицитной анемии значительно ниже в регионах, где мясо является главным составляющим диеты, по сравнению с областями, где мясо не является превалирующим в рационе.
Без искусственных добавок железа у вегетарианцев чаще развивается железодефицитная анемия, чем у людей, принимающих в пищу мясные продукты. Национальные программы по увеличению в рационе питания железа активно внедряются во многих странах, где потребление мяса очень низкое и железодефицитная анемия широко распространена. Однако фундаментальная идея заключается в том, что в большинстве случаев после 1 года жизни одного лишь снижения потребления железа с пищей недостаточно для развития железодефицитной анемии, поэтому обязательным является поиск причин хронической кровопотери. Новорожденные и младенцы представляют собой главную группу риска для развития железодефицитной анемии на фоне снижения потребления железа.
Геморрагия
Хроническая потеря крови, независимо от причины, вызывает выраженный недостаток железа, что, в свою очередь, приводит к железодефицитной анемии. Острая потеря крови ведет к постгеморрагической анемии, которая является нормоцитарной, в отличие от железодефицитной. При хронической геморрагии костный мозг гиперстимулируется для повышенной продукции гемоглобина, что вызывает уменьшение концентрации железа в организме. При уменьшении запасов железа происходит нарушение синтеза гемоглобина, и развивается микроцитарная гипохромная анемия.
Максимальное изменение клеточных индексов эритроцитов происходит приблизительно через 120 дней в связи с полной заменой ранее синтезировавшихся нормальных красных кровяных клеток микроцитами. До этого в мазке периферической крови обнаруживается диморфная популяция эритроцитов: нормоцитов, синтезированных до геморрагии, и микроцитов. Данная ситуация отражается увеличением показателя распределения эритроцитов по величине (RDW), изменение которого является наиболее ранним показателем железодефицитной анемии.
Гемоглобинурия
Железодефицитная анемия может развиваться из-за потери железа с мочой. Гемоглобинурию стоит подозревать, если свежеполученная моча имеет красный или красно-бурый цвет, но при микроскопии не обнаруживаются эритроциты. Дифференциальный диагноз гемоглобинурии и миоглобинурии проводится с использованием 80% сульфата аммония, который преципитирует только гемоглобин, но не миоглобин. Гемоглобинурия может возникать как при любой интраваскулярной гемолитической анемии, так и при достаточно редком состоянии, таком как пароксизмальная ночная гемоглобинурия. На ранних этапах развития сердечно-сосудистой хирургии искусственные клапаны сердца являлись одной из основных причин гемолитической анемии и гемоглобинурии, однако в последнее время с развитием технологий производства клапанов данное осложнение встречается все реже.
Мальабсорбция железа
Длительная ахлоргидрия может вызвать железодефицит, так как низкий уровень pH в желудке требуется для отщепления ионов железа, которые хелатируются с помощью муцина и других субстанций (аминокислот, сахаров) для сохранения растворимости и всасываются в щелочных условиях двенадцатиперстной кишки. Также нужно отметить, что большое потребление крахмала также может привести к мальабсорбции железа и железодефицитной анемии.
Операции по хирургическому удалению проксимального отдела тонкого кишечника или хронические заболевания этого отдела кишки (целиакия, воспалительные заболевания кишечника) могут снизить адсорбцию железа. У пациентов, которые перенесли бариатрическую хирургию, постоперативная желудочная гипохлоргидрия нарушает адсорбцию железа. В то же время, у пациентов, перенесших желудочное шунтирование, наблюдается нарушение восстановления железа в двухвалентное состояние, в форме которого ионы могут всасываться в кишечном тракте. Ухудшает ситуацию общее снижение потребления пищи данными пациентами и часто снижение потребления мяса.
Железодефицит рефрактерный к лечению
Железодефицит рефрактерный к лечению представляет собой наследственное заболевание, характеризующееся железодефицитной анемий резистентной к пероральным препаратам железа, но имеющей частичный ответ на парентеральное лечение. Данное состояние развивается в результате мутаций в гене TMPRSS6, которые ведут к гиперпродукции гепсидина. Заболевание характеризуется микроцитарной гипохромной анемией и повышенными значениями сывороточного гепсидина.
Пациенты с железодефицитом рефрактерным к лечению в большинстве случаев женского пола. Существует высокий уровень вариации возраста манифестации болезни, тяжести заболевания, ответа на проводимую терапию даже внутри одной семьи. Наиболее редкая форма железодефицита рефрактерного к лечению наблюдается у женщин в постменопаузе с дефицитом андрогенов. В этом случае клинический ответ на лечение наблюдается только при дополнительной гормон-заместительной терапии.
Эпидемиология
В соответствии с данными министерства здравоохранения Италии, Бельгии, Германии и Испании, ежегодная встречаемость железодефицитной анемии составляет 7.2-13.9 на 1000 жителей в год. Повышенная встречаемость наблюдается у женщин, молодых и престарелых людей, пациентов с поражением желудочно-кишечного тракта, беременных и женщин с менометроррагией, а также людей, принимающих аспирин или антациды. В странах, где мясо не является основной частью рациона, железодефицитная анемия наблюдается в 6-8 раз чаще, чем в странах Европы. Это происходит даже несмотря на эквивалентное общее содержания железа в рационе, так как гемовое железо из мясных продуктов всасывается лучше, чем негемовое железо. В исследовании, проведенном у детей и подростков из Судана и Непала, железодефицитная анемия обнаруживалась у 2/3 включенных в исследование. Более того, в некоторых регионах кишечные паразиты значительно ухудшают течение железодефицитной анемии в связи с постоянной кровопотерей в ЖКТ.
Клинические проявления и симптомы
Основными симптомами и жалобами при железодефицитной анемии являются:
Несмотря на то, что диагностика железодефицитной анемии проводится на основании результатов лабораторного обследования, тщательно собранный клинический анамнез может значительно упростить раннее выявление данного состояния, помочь в подтверждении этиологии анемии, а также оценить длительность ее существования. Железодефицитная анемия развивается постепенно, и пациенты чаще всего остаются асимптомными до момента, пока запасы железа в организме полностью не иссякнут, что приведет к нарушению синтеза эритроцитов, работы других клеток и, как следствие, появления усталости и других симптомов.
У половины пациентов с железодефицитной анемией средней тяжести наблюдается пагофагия. Обычно главным проявлением данного состояния является желание пациентов живать или сосать лед, а также замороженные овощи. Судороги мышц, возникающие при подъеме по лестнице, также являются частым ранним проявлением железодефицитной анемии. Чаще всего пациенты точно могут назвать дату, когда данные симптомы появились, что позволяет оценить, сколько времени пациент находится в состоянии железодефицита.
Усталость и снижение толерантности к тяжелым физическим нагрузкам при железодефицитной анемии связаны с уменьшением количества гемоглобина в эритроцитах. Однако тяжесть этих симптомов часто не коррелирует с уровнем анемии, что может объясняться нарушением работы других белков, в которых железо является основным коферментом или структурным компонентом. Большое количество новых данных подтверждают идею того, железодефицит приводит к недостаточности и дисфункции не только гемоглобина, но и других ферментов и структурных белков, что ведет к развитию мышечной дисфункции, пагофагии, дисфагии, снижению умственных способностей, ослаблению иммунного ответа на инфекционные агенты и изменению поведения.
Две трети железа в организме содержится в гемоглобине эритроцитов. Каждый грамм гемоглобина содержит 3,47 мг железа. Таким образом, потеря миллилитра крови приводит к потере 0,5 мг железа. Хроническая кровопотеря, связанная с паразитарной инвазией, онкологическими заболеваниями и другими состояниями, представляет собой наиболее частую причину железодефицита. Кровотечение из желудочно-кишечного тракта трудно заметить, и часто пациенты не понимают значимости дегтеобразного стула (мелена). Также чрезмерная менструальная кровопотеря часто не озвучивается пациентками в качестве жалобы, только в случае нарушения цикла. В этом случае наличие сгустков, болей внизу живота, а также использования нескольких тампонов или прокладок может навести доктора на мысль о возможной менометроррагии.
При анемии наблюдается неспецифическая бледность слизистых оболочек. Для железодефицитной анемии также характерно изменения эпителиальных структур: поражение слизистой пищевода, койлонихии, глоссит, ангулярный стоматит и атрофический гастрит. Точная связь между этими состояниями и железодефицитом до сих пор не ясна. Предполагается, что эти состояния могут вызываться другими сопутствующими факторами. Так, было показано, что у 15% пациентов с железодефицитной анемией из стран Европы наблюдаются перечисленные ранее симптомы. В то же время у пациентов из США данные проявления железодефицитной анемии были крайне редки.
Спленомегалия может развиваться в случаях тяжелой персистирующей железодефицитной анемии без лечения.
Прогноз
В большинстве случаев железодефицитной анемии проводимая терапия имеет отличные результаты. Однако ситуация значительно усложняется частым наличием тяжелого первичного заболевания, вызвавшего анемию (чаще всего онкологической патологией). Кроме этого, прогноз пациентов с железодефицитной анемией значительно ухудшается заболеваниями сердечно-сосудистой системы.
Железодефицитная анемия редко является причиной летальных случаев, однако тяжелые случаи и случаи средней тяжести могут вызвать достаточную гипоксию для усугубления хронических заболеваний легких и сердца.
У детей железодефицит может являться причиной сниженного темпа роста, пониженного уровня IQ и способности к обучению.
Стадии железодефицитной анемии
Лабораторное обследование позволяет определить стадию железодефицитной анемии.
Стадия 1 характеризуется снижением железа в костном мозге; гемоглобин и сывороточное железо остается в пределах нормальных значений, но уровень ферритина падает ниже 20 нг/мл. Компенсаторное повышение всасывания железа приводит к повышению железосвязывающей способности сыворотки.
Во время стадии 2 происходит нарушение эритропоэза, и снижение концентрации железа в сыворотке ниже 9 мкмоль/л. Происходит повышение концентрации рецептора трансферрина.
На стадии 3 наблюдается анемия с нормальными значениями индексов эритроцитов и отсутствием изменений на мазке.
На стадии 4 развивается микроцитоз и гипохромия.
На стадии 5 недостаток железа приводит к нарушению работы тканей, развиваются симптомы и жалобы.
Дифференциальный диагноз железодефицитной анемии:
Лабораторная диагностика железодефицитной анемии
Несмотря на то, что симптомы и жалобы пациента могут помочь в ранней диагностике железодефицитной анемии, данное заболевание подтверждается с использованием различных лабораторных тестов.
Тесты для диагностики железодефицитной анемии:
Общий анализ крови
Общий анализ крови позволяет заподозрить железодефицитную анемию и оценить тяжесть заболевания. При хронической железодефицитной анемии наблюдается микроцитоз и гипохромия эритроцитов, характеризующаяся снижением среднего объема эритроцита (MCV) и средней концентрации гемоглобина в эритроците (MCHC). Нужно отметить, что до 40% пациентов с железодефицитной анемией имеют нормоцитарные эритроциты, так что нормальные значения среднего объема эритроцита не исключает железодефицитную анемию. Индекс распределения эритроцитов по величине (RDW) показывает уровень вариации размеров эритроцитов и помогает подтвердить наличие как нормоцитов, так и микроцитов на ранних этапах развития железодефицитной анемии, а также подтвердить комбинированную этиологию анемии при наличии микроцитов и макроцитов (железо-, В12— и фолатдефицитная анемия). Увеличение RDW обозначается как анизоцитоз.
Нужно отметить, что при железодефицитной анемии индексы эритроцитов изменяются только через несколько месяц после начала развития заболевания.
Часто наблюдается повышение количества тромбоцитов (более 450000/мкд), которое нормализуется при проведении терапии. Количество лейкоцитов обычно находится в пределах норм, однако редко может наблюдаться лейкоцитоз.
Мазок периферической крови
Исследование мазка периферической крови является важным этапом диагностики пациентов с анемиями. Для железодефицита характерна микроцитарная (уменьшение размера эритроцита) и гипохромная (уменьшение концентрации гемоглобина в эритроците, приводит к более «бледной» окраске эритроцитов) анемия. Нужно отметить, что микроцитоз определяется раньше, чем изменение показателя MCV.
При железодефицитной анемии не наблюдается кодоциты (клетки-мишени), в отличие от талассемии, и анизоцитоз и пойкилоцитоз чаще всего не выражен. Кроме того, при железодефицитной анемии не наблюдаются внутриэритроцитарные включения.
В регионах со сниженным потреблением мяса частым является сосуществование дефицита фолатов и железодефицита. При таком состоянии в мазке могут наблюдаться макроциты с гипохромными микроцитами. В этом случае значение MCV будет находиться в пределах нормальных значений.
Ферритин, железо, железосвязывающая способность
Для оценки концентрации железа в организме проводятся исследования на сывороточную концентрацию железа, общую железосвязывающую способность и концентрацию ферритина.
Для железодефицитной анемии характерно снижение концентрации железа и ферритина и повышения общей железосвязывающей способности. Однако полная положительная «триада» лабораторных маркеров встречается на более поздних этапах развития анемии. Раньше всего на снижение концентрации железа отвечает ферритин.
Молекула ферритина способна связывать 4000-5000 атомов железа единовременно, что делает его главным белковым хранилищем железа в организме. Ферритин находится в основном в цитоплазме клеток ретикулоэндотелиальной системы, а также в свободном виде в сыворотке крови.
Концентрация ферритина прямо отражает общее содержание железа в организме. Таким образом, сывороточная концентрация ферритина является диагностическим инструментом для анализа содержания железа. Концентрация ферритина сильно варьирует у пациентов разного возраста и пола.
При железодефицитной анемии концентрация ферритина в сыворотке составляет одну десятую нормального значения. Ряд исследований показали, что ферритин является одним из самых чувствительных маркеров железодефицитной анемии на ранних этапах развития заболевания, однако результаты исследования следует интерпретировать с осторожностью, так как в некоторых случаях он не отражает реальной картины общего содержания железа в организме. Чаще всего это связано с тем, что ферритин является острофазным белком и может значительно повышаться при остром и хроническом воспалении, а также при хронических заболеваниях печени, хронической болезни почек. В связи с этим нормальные значения ферритина могут наблюдаться при сосуществовании железодефицитной анемии с другой хронической патологией.
Ферритин также является маркером ответа и мониторинга проводимой терапии препаратами железа.
Тесты для подтверждения этиологии железодефицитной анемии:
Дифференциальный диагноз с анемией хронического заболевания
Ферритин является белком острой фазы, и его концентрация значительно повышается при воспалительных процессах, что делает невозможным его использования в качестве маркера дифференциальной диагностики анемии хронического заболевания и железодефицитной анемии в некоторых клинических случаях. В конце 90-х годов был описан чувствительный и ранний маркер дефицита железа – растворимый рецептор трансферрина, который увеличивается пропорционально дефициту тканевого железа. Главным преимуществом данного маркера является то, что его концентрация не изменяется при воспалительной реакции, что делает его идеальным маркером для дифференциальной диагностики анемии хронического заболевания и железодефицитной анемии. Дополнительно для увеличения точности исследования рекомендуется использовать индекс растворимого рецептора трансферрина/Logферритин (рТФР-Ф). Положительный результат исследования рТФР-Ф с высокой вероятностью диагностирует железодефицит. Чувствительность метода — 89,19%, специфичность — 92,86%.
Электрофорез гемоглобина
Электрофорез гемоглобина помогает подтвердить бета-талассемию и другие гемоглобинопатии в качестве причины развития микроцитарной анемии.
Исследование гемоглобина в стуле
Исследование гемоглобина в стуле позволяет подтвердить, что хроническое желудочно-кишечное кровотечение является причиной развития железодефицитной анемии. Современные методы позволяют с высокой точностью и специфично детектировать человеческий гемоглобин в стуле. Данные методы позволяют проводить исследования даже у пациентов, которые предварительно не исключили из рациона мясные продукты. Для повышения точности исследования может быть рекомендовано одновременное проведение исследование фекального кальпротектина в кале.
Главной причиной появления гемоглобина в стуле являются злокачественные образования толстого кишечника, поэтому подтверждение железодефицитной анемии и детекция гемоглобина в кале является показанием к проведению колоноскопии.
Определение осмотической стойкости эритроцитов
Тест на осмотическую стойкость эритроцитов является классическим исследованием для диагностики наследственного сфероцитоза. При микросфероцитозе может наблюдаться микроцитоз и снижение MCV, однако нормохромия и нормальные значения MCHC помогают отличить это состояние от железодефицитной анемии. В редких случаях исследование осмотической стойкости эритроцитов помогает точно определить этиологию заболевания.
Исследование концентрации свинца
Хроническое отравление свинцом может приводить к развитию микроцитарной анемии. Встречаемость отравления свинцом намного выше у пациентов с железодефицитом, чем у здоровых людей, так как понижение концентрации железа в крови приводит к повышенному всасыванию свинца.