Синдром уставших надпочечников что это такое
Дисфункция надпочечников. Человек Уставший, продолжение.
Дисфункция – это как предболезнь. Заболевание еще не развилось, а жалобы есть, но они стертые, поэтому человеку плохо, но он не может понять, что с ним и с каким органом это состояние связать.
В современном обществе формируется неправильная тенденция социального поведения. Тебя постоянно подгоняют «еще, еще. больше работай, будь успешным, делай карьеру, но не забудь про семью, роди 2-3 детей (надо поднимать демографию страны), имей хобби, выучи языки, имей 2 образования, занимайся спортом, путешествуй, не забывай посещать театр (для кого-то ночной клуб, дискотеку), води машину и т.д.»
И как, скажите мне, человеку выдержать такой прессинг? Ни малейшего времени на передышку, на созерцание. Резервы организма ИМЕЮТ ПРЕДЕЛ, и у каждого свой срок «до срыва». И этим пределом часто является истощение функции надпочечников, одного из важнейших эндокринных органов.
Какими же симптомами дисфункция надпочечников может выражаться: (симптомы могут быть разной степени выраженности от минимальных до максимальных)
Как проверить работу надпочечников?
До 2015 года основным способом были: анализ крови на кортизол, АКТГ по часам 8:00- 24:00 (или еще промежуточно 13:00) и сбор суточной мочи на кортизол, кровь на ДГА-С. Это было крайне неудобно. Ни одна лаборатория, кроме расположенных в стационаре, кортизол в 24:00 не брала. А без этого показателя оценить функцию надпочечников правильно не возможно. Собирать суточную мочу не все соглашались, очень трудоемко и может быть не так достоверно.
С 2015-2016 года появился метод оценки кортизола слюны.
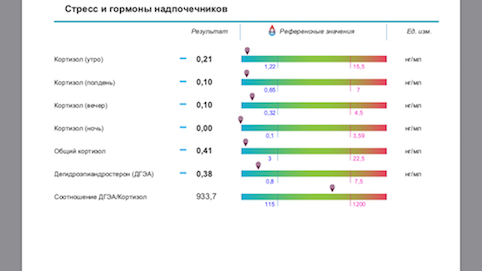
Собирается суточный профиль слюны на кортизол по 4 точкам 8:00- 13:00 и 17:00- 24:00.
Ниже привожу материал лаборатории «CHROMOLAB» по исследованию состояния надпочечников и его интерпретации.
«Организм человека постоянно подвергается воздействию различных факторов внешней и внутренней среды. Это могут быть абиотические факторы, такие как холод, жара, атмосферное давление, влажность, недостаток кислорода. Избыток или дефицит поступающих в организм веществ (белков, углеводов, липидов), недостаток витаминов и микроэлементов, вирусная или микробная инфекция, токсины также оказывают определенное влияние. Негативные последствия имеют вредные привычки, физическая перегрузка, переедание, гиподинамия, нарушение ритма сна и бодрствования. Кроме того, к серьезным стрессорам относят техногенные и психологические воздействия: переизбыток компьютерной и телевизионной информации, монотонный труд, конфликты, чрезмерную рабочую нагрузку, эмоциональное истощение, завышенный уровень ответственности, общую неудовлетворенность и прочее. Все эти и многие другие причины ведут к постоянному напряжению физиологических резервов организма, который вынужден приспосабливаться (адаптироваться) к этим факторам или защищаться. Если воздействия носят интенсивный, внезапный или незнакомый («новый») характер, то организм отвечает на них универсальной (в формате «скорой помощи») физиологической реакцией, называемой СТРЕССОМ (стрессорной реакцией). Стрессорная реакция не связана с положительным или отрицательным восприятием внешних раздражителей, с которыми сталкивается человек. Она необходима для скорейшей адаптации организма с целью его защиты от гибели. Стресс – это защитная реакция организма. Однако длительная стрессорная реакция приводит к избыточному нерегулируемому ответу организма на повреждающий фактор и обратному эффекту. Вместо защитных процессов активируются деструктивные, что может стать пусковым механизмом для развития патологических состояний: сахарного диабета, тромбозов, инсультов, инфарктов, аритмии, бесплодия, эректильной дисфункции, аллергии, онкологических заболеваний, иммунодефицитов, ранней менопаузы, остеопороза, гипотиреоза, бессонницы, депрессии, ожирения, анорексии и многого другого. Стресс инициирует различные патологические состояния, и это зависит от провоцирующих факторов внешней и внутренней среды.»
Стадийность стрессорных реакций. Выделяют три стадии стресса (согласно Г. Селье):
Глубокое понимание механизмов регуляции стресса стало возможным благодаря исследованию процессов синтеза, обмена и метаболизма стероидных гормонов коры надпочечников: кортизола и дегидроэпиандростерона (ДГЭА), которые регулируют реализацию стрессорной реакции.
Согласно современным исследованиям, физиологический смысл этого феномена заключается в том, что ДГЭА – это мощный естественный антиглюкокортикоид, противостоящий кортизолу, уровень которого резко повышается при любом стрессе. Известно, что отношение ДГЭА к кортизолу следует рассматривать как ключевой маркер устойчивости организма к любому стрессу, для обеспечения которой в целях адекватной защиты в организме всегда должен превалировать уровень ДГЭА.
Оценку суточного ритма секреции кортизола по его концентрации в слюне (4-кратное определение в течение дня в разных порциях слюны) применяют для отличия стрессорной реакции от иных патологических состояний, связанных с дисфункцией секреции стероидных гормонов.
Оценка проводится только врачом.
Известно, что уровень кортизола – величина непостоянная, и он подвержен колебаниям в течение суток.
С 7 до 9 часов утра концентрация кортизола максимальна, в связи с чем утренний уровень этого гормона считается хорошим индикатором для определения функционального состояния надпочечников.
С 11 часов утра до 13 часов дня концентрация кортизола возвращается к среднему значению, что служит показателем адаптивной функции надпочечников.
С 15 до 17 часов дня уровень кортизола постепенно опускается.
С 22 часов вечера до полуночи концентрация гормона находится на самом низком уровне, что отражает нормальную надпочечниковую функцию.
Такое развернутое исследование надпочечников поможет определиться с диагнозом, нет ли здесь дебюта надпочечниковой недостаточности или это просто дисфункция и определиться с лечебной тактикой. Ведь кому-то надо будет отдохнуть и правильно питаться. А кому-то понадобится подобрать препараты гормонов надпочечников сроком от 1,5-3-х месяцев до пожизненной терапии при выявленной надпочечниковой недостаточности. Радует то, что надпочечниковая недостаточность встречается очень редко.
НО очень часто встречается дисфункция.
Особенную благодарность в идее составления этой статьи выражаю своему учителю Гострому Андрею Владимировичу.
Что вызывает истощение надпочечников, как это предотвратить?
Признаки истощения организма в целом хорошо известны всем. Однако подобное может происходить и с отдельными системами и органами. Особенно склонны к этому эндокринные железы. Сегодня мы сосредоточимся на надпочечниках — парных органах, функции которых для многих остаются загадкой. Расскажем, как они работают, почему переутомляются, как это влияет на организм.
Почему органы устают?
Прежде чем знакомиться с надпочечниками и выявлять причины их истощения, разберемся, как вообще органы могут переутомляться. Ведь они трудятся на протяжении всей жизни человека и, казалось бы, уставать не должны.
Но у любого органа есть пределы нормальной работы. Когда его активность усиливается, наблюдается гиперфункция. Это может быть реакцией:
• защиты от интенсивного раздражителя;
• приспособления к изменившимся условиям;
• компенсации недостаточности других органов (что особенно присуще элементам эндокринной системы).
Однако длительная работа на пределе возможностей приводит к усталости и появлению признаков истощения. Сначала они вызывают дискомфорт, а в дальнейшем оборачиваются серьезными заболеваниями. Поэтому так важно прислушиваться к сигналам организма.
Что такое надпочечники, какие функции они выполняют?
Это парные эндокринные железы, расположенные над верхними полюсами почек. Каждая из них состоит из двух элементов, выполняющих разные функции.
Кора надпочечников вырабатывает:
• глюкокортикоиды, борющиеся с воспалением и стимулирующие образование глюкозы в печени;
• андрогены, регулирующие работу основных половых гормонов;
• минералокортикоиды, которые отвечают за транспортировку электролитов.
Второй элемент — мозговое вещество — вырабатывает катехоламины, регулирующие основные реакции симпатической нервной системы. Наиболее очевидное проявление работы этих желез — выделение адреналина.
Как появляется состояние надпочечниковой усталости?
Нарушения в деятельности надпочечников могут выражаться по двум направлениям. При гипофункции орган со своей задачей не справляется, а при гиперфункции — работает на пределе возможностей. В последнем случае и возникает переутомление.
Эндокринологи не признают усталость надпочечников как самостоятельную патологию. Однако существование ее признаков отрицать сложно.
Пытаясь найти истоки такого состояния, нужно сосредоточиться на синдромах, сопровождающихся гиперфункцией желез. Они характеризуются высокими показателями гормонов, выделяемых этими железами (преимущественно кортизола — индикатора стресса).
Однако в результате их длительного воздействия на организм появляются симптомы, которые часто приписывают переутомлению надпочечников. Это неправильно, поскольку истинное истощение органа проявляется, когда после длительной гиперфункции он перестает справляться со своими задачами.
Основные виды заболеваний надпочечников
Гиперфункция надпочечников бывает компенсаторной. Если их кора изначально гиперплазирована (увеличена от рождения), железа вырабатывает избыточное количество гормонов. Но поскольку интенсивность работы объясняется патологическим размером органа, о переутомлении речи не идет.
В этом аспекте более интересны синдромы, сопровождаемые приобретенной гиперфункцией эндокринных желез:
• Синдром Кушинга. Характеризуется избыточной выработкой кортизола под действием избытка адренокортикотропного гомона, медикаментозной терапии или опухоли.
• Синдром Конна. Железы активно выделяют альдостерон, что чаще вызывается аденомой клубочковой зоны коры.
• Адреногенитальный синдром. Основной признак — избыточная секреция надпочечниковых андрогенов. Наблюдается при врожденной гиперплазии желез или под действием злокачественной опухоли.
От гиперфункции надпочечников важно отличать феохромоцитому. Хотя в организме повышается уровень катехоламинов, вырабатывает их не эндокринная железа, а ее опухоль.
Симптомы заболеваний
Поскольку перечисленные патологии связаны с нарушением нормальной работы одного и того же элемента эндокринной системы, многие их проявления совпадают. Поэтому особенно важна дифференциальная диагностика.
Кроме повышения уровня определенного гормона, эти заболевания проявляются и другими характерными симптомами.
Синдром Кушинга:
Синдром Конна:
Адреногенитальный синдром:
Методы диагностики заболеваний надпочечников
Основной метод диагностики патологий в этой области — анализ крови на гормоны. Однако не менее важным является ультразвуковое исследование. Оно отвечает на вопросы о наличии гиперплазии органа и новообразований.
Использование этих методов в совокупности исключает ошибку. Например, катехоламины могут вырабатываться как самим органом, так и опухолью. Поэтому единственный анализ крови не даст полной картины.
В зависимости от того, на какое заболевание указывают результаты анализов и УЗИ, возможно направление пациента на дополнительные обследования. При подозрении на синдром Конна важно оценить активность ренина плазмы и концентрацию электролитов, на синдром Кушинга — состояние гипофиза, при признаках надпочечниковой вирилизации — уровень других половых гормонов.
Методы лечения
Они зависят от заболевания, спровоцировавшего гиперфункцию надпочечников. Для подбора правильной тактики лечения важно определить причину выявленного синдрома. В целом используются медикаментозные и хирургические методы, но в отдельных случаях некоторые из них могут не сработать.
Лечение адреногенитального синдрома
Если АГС связан с гиперплазией, используется медикаментозная терапия. Пациенту назначаются глюкокортикоиды:
• гидрокортизон;
• дексаметазон;
• кортизона ацетат.
Дексаметазон назначается только в случаях, если два других препарата не дают нужного эффекта. Его избегают, поскольку побочной реакцией может стать развитие синдрома Кушинга.
Если причиной заболевания послужила гормонопродуцирующая опухоль, ее удаляют. Но даже при благополучном исходе ткани коры оказываются атрофированными. Поэтому требуется дополнительная поддержка глюкокортикоидами до полного восстановления нормальной работы желез.
Лечение синдрома Конна
Причиной этой патологии обычно выступает опухоль. Удаляют ее с лапароскопического доступа. В 70% случаев после операции симптомы исчезают.
Однако иногда избыток альдостерона обусловливается гиперплазией надпочечника. Резекция части органа не влечет нормализации давления, поэтому эндокринологи предпочитают медикаментозную терапию.
Для лечения обычно используются блокаторы альдостерона — спиронолактон, эплеренон. Оба являются калийсберегающими диуретиками. При этом спиронолактон блокирует андрогенное действие, что делает его более предпочтительным для женщин. Эплеренон же чаще назначают мужчинам во избежание феминизации.
Лечение синдрома Кушинга
Для нормализации состояния пациента назначают блокаторы кортизола. Если заболевание развивается стремительно, существует угроза жизни, предпочтение отдается внутривенной инфузии (капельнице) этомидата. В домашних условиях подойдет кетоконазол, однако его назначают с осторожностью из-за его гепатотоксичности.
К хирургическим методам прибегают, если болезнь вызвана АКГТ-продуцирующей опухолью. Она может располагаться в:
• гипофизе (чаще всего);
• надпочечниках;
• тканях, для которых нехарактерна выработка адренокортикотропного гомона (эктопическая опухоль).
Повышение кортизола всегда нарушает калий-натриевый баланс. Поэтому больному необходима диета, богатая калием. Если через питание быстро восстановить его уровень не удается, назначают калийсберегающие диуретики.
Как заподозрить усталость надпочечников?
Усталость надпочечников — это результат их работы в усиленном режиме. Поэтому невозможно обнаружить ее внезапно, не замечая симптомов описанных синдромов. Поэтому эндокринологи и относятся к этому явлению со скепсисом.
Заподозрить переутомление органа можно по таким состояниям:
• общая слабость;
• скачки давления;
• выраженные вегетативные реакции на стресс;
• нарушение репродуктивной функции;
• маскулинизация у женщин (появление мужских черт).
Если после гиперфункции железы перешли в состояние гипофункции, возможны проявления минералокортикоидной или глюкокортикоидной недостаточности.
Первая характеризуется преимущественно нарушением электролитного баланса на фоне обезвоживания. Человек теряет соли с мочой и даже слюной. Также у него ощутимо снижается давление.
При дефиците глюкокортикоидов нарушается обмен нутриентов. Это проявляется гипогликемией (снижением уровня сахара в крови). Человек ощущает слабость, спутанность сознания, тошноту, теряет вес (вплоть до анорексии). Все эти симптомы как раз приписывают усталости надпочечников.
Что вызывает истощение надпочечников, как это предотвратить?
Признаки истощения организма в целом хорошо известны всем. Однако подобное может происходить и с отдельными системами и органами. Особенно склонны к этому эндокринные железы. Сегодня мы сосредоточимся на надпочечниках — парных органах, функции которых для многих остаются загадкой. Расскажем, как они работают, почему переутомляются, как это влияет на организм.
Почему органы устают?
Прежде чем знакомиться с надпочечниками и выявлять причины их истощения, разберемся, как вообще органы могут переутомляться. Ведь они трудятся на протяжении всей жизни человека и, казалось бы, уставать не должны.
Но у любого органа есть пределы нормальной работы. Когда его активность усиливается, наблюдается гиперфункция. Это может быть реакцией:
• защиты от интенсивного раздражителя;
• приспособления к изменившимся условиям;
• компенсации недостаточности других органов (что особенно присуще элементам эндокринной системы).
Однако длительная работа на пределе возможностей приводит к усталости и появлению признаков истощения. Сначала они вызывают дискомфорт, а в дальнейшем оборачиваются серьезными заболеваниями. Поэтому так важно прислушиваться к сигналам организма.
Что такое надпочечники, какие функции они выполняют?
Это парные эндокринные железы, расположенные над верхними полюсами почек. Каждая из них состоит из двух элементов, выполняющих разные функции.
Кора надпочечников вырабатывает:
• глюкокортикоиды, борющиеся с воспалением и стимулирующие образование глюкозы в печени;
• андрогены, регулирующие работу основных половых гормонов;
• минералокортикоиды, которые отвечают за транспортировку электролитов.
Второй элемент — мозговое вещество — вырабатывает катехоламины, регулирующие основные реакции симпатической нервной системы. Наиболее очевидное проявление работы этих желез — выделение адреналина.
Как появляется состояние надпочечниковой усталости?
Нарушения в деятельности надпочечников могут выражаться по двум направлениям. При гипофункции орган со своей задачей не справляется, а при гиперфункции — работает на пределе возможностей. В последнем случае и возникает переутомление.
Эндокринологи не признают усталость надпочечников как самостоятельную патологию. Однако существование ее признаков отрицать сложно.
Пытаясь найти истоки такого состояния, нужно сосредоточиться на синдромах, сопровождающихся гиперфункцией желез. Они характеризуются высокими показателями гормонов, выделяемых этими железами (преимущественно кортизола — индикатора стресса).
Однако в результате их длительного воздействия на организм появляются симптомы, которые часто приписывают переутомлению надпочечников. Это неправильно, поскольку истинное истощение органа проявляется, когда после длительной гиперфункции он перестает справляться со своими задачами.
Основные виды заболеваний надпочечников
Гиперфункция надпочечников бывает компенсаторной. Если их кора изначально гиперплазирована (увеличена от рождения), железа вырабатывает избыточное количество гормонов. Но поскольку интенсивность работы объясняется патологическим размером органа, о переутомлении речи не идет.
В этом аспекте более интересны синдромы, сопровождаемые приобретенной гиперфункцией эндокринных желез:
• Синдром Кушинга. Характеризуется избыточной выработкой кортизола под действием избытка адренокортикотропного гомона, медикаментозной терапии или опухоли.
• Синдром Конна. Железы активно выделяют альдостерон, что чаще вызывается аденомой клубочковой зоны коры.
• Адреногенитальный синдром. Основной признак — избыточная секреция надпочечниковых андрогенов. Наблюдается при врожденной гиперплазии желез или под действием злокачественной опухоли.
От гиперфункции надпочечников важно отличать феохромоцитому. Хотя в организме повышается уровень катехоламинов, вырабатывает их не эндокринная железа, а ее опухоль.
Симптомы заболеваний
Поскольку перечисленные патологии связаны с нарушением нормальной работы одного и того же элемента эндокринной системы, многие их проявления совпадают. Поэтому особенно важна дифференциальная диагностика.
Кроме повышения уровня определенного гормона, эти заболевания проявляются и другими характерными симптомами.
Синдром Кушинга:
Синдром Конна:
Адреногенитальный синдром:
Методы диагностики заболеваний надпочечников
Основной метод диагностики патологий в этой области — анализ крови на гормоны. Однако не менее важным является ультразвуковое исследование. Оно отвечает на вопросы о наличии гиперплазии органа и новообразований.
Использование этих методов в совокупности исключает ошибку. Например, катехоламины могут вырабатываться как самим органом, так и опухолью. Поэтому единственный анализ крови не даст полной картины.
В зависимости от того, на какое заболевание указывают результаты анализов и УЗИ, возможно направление пациента на дополнительные обследования. При подозрении на синдром Конна важно оценить активность ренина плазмы и концентрацию электролитов, на синдром Кушинга — состояние гипофиза, при признаках надпочечниковой вирилизации — уровень других половых гормонов.
Методы лечения
Они зависят от заболевания, спровоцировавшего гиперфункцию надпочечников. Для подбора правильной тактики лечения важно определить причину выявленного синдрома. В целом используются медикаментозные и хирургические методы, но в отдельных случаях некоторые из них могут не сработать.
Лечение адреногенитального синдрома
Если АГС связан с гиперплазией, используется медикаментозная терапия. Пациенту назначаются глюкокортикоиды:
• гидрокортизон;
• дексаметазон;
• кортизона ацетат.
Дексаметазон назначается только в случаях, если два других препарата не дают нужного эффекта. Его избегают, поскольку побочной реакцией может стать развитие синдрома Кушинга.
Если причиной заболевания послужила гормонопродуцирующая опухоль, ее удаляют. Но даже при благополучном исходе ткани коры оказываются атрофированными. Поэтому требуется дополнительная поддержка глюкокортикоидами до полного восстановления нормальной работы желез.
Лечение синдрома Конна
Причиной этой патологии обычно выступает опухоль. Удаляют ее с лапароскопического доступа. В 70% случаев после операции симптомы исчезают.
Однако иногда избыток альдостерона обусловливается гиперплазией надпочечника. Резекция части органа не влечет нормализации давления, поэтому эндокринологи предпочитают медикаментозную терапию.
Для лечения обычно используются блокаторы альдостерона — спиронолактон, эплеренон. Оба являются калийсберегающими диуретиками. При этом спиронолактон блокирует андрогенное действие, что делает его более предпочтительным для женщин. Эплеренон же чаще назначают мужчинам во избежание феминизации.
Лечение синдрома Кушинга
Для нормализации состояния пациента назначают блокаторы кортизола. Если заболевание развивается стремительно, существует угроза жизни, предпочтение отдается внутривенной инфузии (капельнице) этомидата. В домашних условиях подойдет кетоконазол, однако его назначают с осторожностью из-за его гепатотоксичности.
К хирургическим методам прибегают, если болезнь вызвана АКГТ-продуцирующей опухолью. Она может располагаться в:
• гипофизе (чаще всего);
• надпочечниках;
• тканях, для которых нехарактерна выработка адренокортикотропного гомона (эктопическая опухоль).
Повышение кортизола всегда нарушает калий-натриевый баланс. Поэтому больному необходима диета, богатая калием. Если через питание быстро восстановить его уровень не удается, назначают калийсберегающие диуретики.
Как заподозрить усталость надпочечников?
Усталость надпочечников — это результат их работы в усиленном режиме. Поэтому невозможно обнаружить ее внезапно, не замечая симптомов описанных синдромов. Поэтому эндокринологи и относятся к этому явлению со скепсисом.
Заподозрить переутомление органа можно по таким состояниям:
• общая слабость;
• скачки давления;
• выраженные вегетативные реакции на стресс;
• нарушение репродуктивной функции;
• маскулинизация у женщин (появление мужских черт).
Если после гиперфункции железы перешли в состояние гипофункции, возможны проявления минералокортикоидной или глюкокортикоидной недостаточности.
Первая характеризуется преимущественно нарушением электролитного баланса на фоне обезвоживания. Человек теряет соли с мочой и даже слюной. Также у него ощутимо снижается давление.
При дефиците глюкокортикоидов нарушается обмен нутриентов. Это проявляется гипогликемией (снижением уровня сахара в крови). Человек ощущает слабость, спутанность сознания, тошноту, теряет вес (вплоть до анорексии). Все эти симптомы как раз приписывают усталости надпочечников.