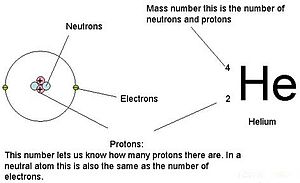
С чем совпадает зарядовое число
Зарядовое число
Зарядовое число атомного ядра (синонимы: атомный номер, атомное число, порядковый номер химического элемента) — количество протонов в атомном ядре. Зарядовое число равно заряду ядра в единицах элементарного заряда и одновременно равно порядковому номеру соответствующего ядру химического элемента в таблице Менделеева.
Термин «атомный» или «порядковый» номер обычно используется в атомной физике и в химии, тогда как эквивалентный термин «зарядовое число» — в ядерной физике. В неионизированном атоме количество электронов в электронных оболочках совпадает с зарядовым числом.
Зарядовое число обычно обозначается буквой Z. Ядра с одинаковым зарядовым числом, но различным массовым числом A (которое равно сумме числа протонов Z и числа нейтронов N) являются различными изотопами одного и того же химического элемента, поскольку именно заряд ядра определяет структуру электронной оболочки атома и, следовательно, его химические свойства.
Полезное
Смотреть что такое «Зарядовое число» в других словарях:
зарядовое число — atominis skaičius statusas T sritis Standartizacija ir metrologija apibrėžtis Cheminio elemento eilės numeris periodinėje elementų sistemoje. Apibūdina atomo branduolio protonų skaičių, taip pat atitinkamo neutraliojo atomo elektronų skaičių.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
зарядовое число — atominis skaičius statusas T sritis Standartizacija ir metrologija apibrėžtis Protonų skaičius atomo branduolyje. atitikmenys: angl. atomic number; charge number; ordinal number; proton number vok. Atomnummer, f; Atomzahl, f; Kernladungszahl, f;… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
зарядовое число — atominis skaičius statusas T sritis chemija apibrėžtis Protonų skaičius atomo branduolyje. santrumpa( os) Z atitikmenys: angl. atomic number; charge number; ordinal number; proton number rus. атомное число; атомный номер; зарядовое число;… … Chemijos terminų aiškinamasis žodynas
зарядовое число — atominis skaičius statusas T sritis fizika atitikmenys: angl. atomic number; charge number; ordinal number vok. Atomnummer, f; Atomzahl, f; Kernladungszahl, f; Ordnungszahl, f rus. атомное число, n; атомный номер, m; зарядовое число, n;… … Fizikos terminų žodynas
ЗАРЯДОВОЕ ЧИСЛО — атомный номе р, порядковый номер Z хим. элемента в периодической системе элементов Менделеева. Определяет число протонов в атомном ядре и его электрич. заряд, равный Ze, где е заряд протона (численно равный заряду электрона), а также число… … Большой энциклопедический политехнический словарь
Число (значения) — Число Число (лингвистика) Число система налогообложения, действовавшая в XIII XV веках на территориях, захваченных Золотой Ордой. Название связано с сутью налога его размер зависел от «числа» людей, подчиненных плательщику[1][2] … Википедия
ЗАРЯДОВОЕ СОПРЯЖЕНИЕ — (С), операция замены всех ч ц, участвующих в к. л. вз ствии, на соответствующие им античастицы. Опыт показывает, что сильное и эл. магн. вз ствия не меняются при З. с., то есть сильные и эл. магн. вз ствия ч ц и античастиц, находящихся в тех же… … Физическая энциклопедия
Массовое число — Для улучшения этой статьи желательно?: Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное. Дополнить статью (статья слишком короткая либо содержит лишь словарное определение) … Википедия
атомное число — atominis skaičius statusas T sritis Standartizacija ir metrologija apibrėžtis Cheminio elemento eilės numeris periodinėje elementų sistemoje. Apibūdina atomo branduolio protonų skaičių, taip pat atitinkamo neutraliojo atomo elektronų skaičių.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
С чем совпадает зарядовое число
1. Как называются протоны и нейтроны вместе?
Протоны и нейтроны называются нуклонами.
То есть атомные ядра состоят из нуклонов.
В 1932 году Д.Д. Иваненко и В. Гейзенберг предложили протонно-нейтронную модель строения ядер.
2. Что называется массовым числом и какой буквой оно обозначается?
Массовым числом называется общее число нуклонов в ядре атома.
Массовое число численно равно массе ядра, выраженной в атомных единицах массы и округлённой до целых чисел.
Массовое число обозначается буквой А.
3. Что можно сказать о числовом значении массы атома (в а.е.м.) и его массовом числе?
Массовое число равно с точностью до целых (поскольку масса каждого нуклона примерно равна 1 а.е.м.) числу атомных единиц массы, содержащихся в массе атома.
2. Что называется зарядовым числом и какой буквой оно обозначается?
Зарядовым числом называется число протонов в ядре.
Зарядовое число численно равно заряду ядра, выраженному в элементарных электрических зарядах.
(Заряд каждого протона равен элементарному электрическому заряду. )
Зарядовое число обозначается буквой Z.
Для каждого химического элемента зарядовое число равно атомному (порядковому) номеру в таблице Д. И. Менделеева.
4. Как называется и какой буквой обозначается число протонов в ядре?
Число протонов в атоме обозначается буквой Z и называется зарядовым числом.
5. Что можно сказать о зарядовом числе, заряде ядра (выраженном в элементарных электрических зарядах) и порядковом номере в таблице Д. И. Менделеева для любого химического элемента?
Зарядовое число равно заряду ядра, выраженному в элементарных электрических зарядах.
Зарядовое число атома равно его порядковому номеру в таблице Менделеева.
6. Как в общем виде принято обозначать ядро любого химического элемента?
Ядро любого химического элемента в общем виде обозначается 
7. Какой буквой обозначают число нейтронов в ядре?
Число нейтронов в ядре обозначают буквой N.
8. Какой формулой связаны между собой массовое число, зарядовое число и число нейтронов в ядре?
A = Z + N
9. Как с точки зрения протонно нейтронной модели ядра объясняется существование ядер с одинаковыми зарядами и различными массами?
У одного и того же химического элемента встречаются атомы с различными по массе ядрами.
Такие атомы называются изотопами.
Атомы изотопов имеют одинаковый заряд и поэтому один и тот же порядковый номер в таблице Д. И. Менделеева.
Изотопы — это разновидности одного химического элемента, различающиеся по массе атомных ядер
Ядра изотопов содержат одинаковое число протонов, но различное число нейтронов.
Зарядовое число
Зарядовое число атомного ядра (синонимы: атомный номер, атомное число, порядковый номер химического элемента) — количество протонов в атомном ядре. Зарядовое число равно заряду ядра в единицах элементарного заряда и одновременно равно порядковому номеру соответствующего ядра химического элемента в таблице Менделеева.
Термин «атомный» или «порядковый» номер обычно используется в атомной физике и в химии, тогда как эквивалентный термин «зарядовое число» — в ядерной физике. В неионизированном атоме количество электронов в электронных оболочках совпадает с зарядовым числом.
Ядра с одинаковым зарядовым числом, но различным массовым числом A (которое равно сумме числа протонов Z и числа нейтронов N) являются различными изотопами одного и того же химического элемента, поскольку именно заряд ядра определяет структуру электронной оболочки атома и, следовательно, его химические свойства. Поскольку протоны и нейтроны имеют приблизительно одинаковую массу (а масса электронов пренебрежимо мала для многих целей), а дефект массы нуклонного связывания всегда мал по сравнению с массой нуклона, атомная масса любого атома, если выразиться в объединённом атомном атоме Массовые единицы (составляющие величину, называемую «относительной изотопной массой»), находятся в пределах 1 % от целого числа А.
Атомы с одинаковым атомным номером, но с разными нейтронными числами и, следовательно, с разными массовыми числами, известны как изотопы. Чуть более трех четвертей естественных элементов существует в виде смеси изотопов (см. Моноизотопный элемент), и средняя изотопная масса изотопной смеси для элемента (называемого относительной атомной массой) в определённой среде на Земле определяет стандартный атомный вес элемента. Исторически именно эти атомные веса элементов (по сравнению с водородом) были величинами, измеряемыми химиками в XIX веке.
Периодическая таблица и порядковые номера для каждого элемента
Существование или создание периодической таблицы элементов создает упорядочение элементов, и поэтому они могут быть пронумерованы по порядку.
Однако простая нумерация, основанная на позиции периодической таблицы, никогда не была полностью удовлетворительной. Помимо случая йода и теллура, позднее было известно, что несколько других пар элементов (таких как аргон и калий, кобальт и никель) имеют почти одинаковые или обратные атомные веса, поэтому их размещение в периодической таблице определяется их химическим составом. свойства. Однако постепенная идентификация все более и более сходных по химическому составу элементов лантаноидов, атомный номер которых не был очевиден, привела к несогласованности и неопределенности в периодической нумерации элементов, по крайней мере, начиная с лютеция (элемент 71) и далее (гафний не был известен в настоящее время).
Модели атома Резерфорда-Бора и Ван ден Брука
В 1911 году британский физик Эрнест Резерфорд предложил модель атома, в которой центральное ядро содержало большую часть массы атома и положительный заряд, который в единицах заряда электрона должен был быть примерно равен половине атомного веса атома, выраженного в числа атомов водорода. Таким образом, этот центральный заряд должен был быть примерно вдвое меньше атомного веса (хотя он почти на 25 % отличается от атомного номера золота (Z = 79, A = 197), единственного элемента, из которого Резерфорд сделал свое предположение). Тем не менее, несмотря на оценку Резерфорда, что у золота был центральный заряд около 100 (но был элемент Z = 79 в периодической таблице), через месяц после появления статьи Резерфорда, голландский физик-любитель Антониус ван ден Брук впервые предположил, что центральный заряд и число электронов в атоме были точно равны его месту в периодической таблице (также известной как номер элемента, атомный номер и символизированный Z). Эта гипотеза в конечном счете подтвердилась.
Эксперименты Мозли 1913 года
Отсутствующие элементы
Протон и гипотеза ядерных электронов
Открытие нейтрона и его значение
Каждый элемент обладает определённым набором химических свойств как следствие количества электронов, присутствующих в нейтральном атоме, которое представляет собой Z (атомный номер). Конфигурация этих электронов следует из принципов квантовой механики. Количество электронов в электронных оболочках каждого элемента, особенно в самой внешней валентной оболочке, является основным фактором, определяющим его химическую связь. Следовательно, только атомный номер определяет химические свойства элемента; и именно по этой причине элемент может быть определён как состоящий из любой смеси атомов с данным атомным номером.
Поиски новых элементов обычно описываются с использованием атомных номеров. По состоянию на 2019 год были обнаружены все элементы с атомными номерами от 1 до 118. Синтез новых элементов осуществляется путем бомбардировки атомами-мишенями тяжелых элементов ионами, так что сумма атомных номеров целевого и ионного элементов равна атомному номеру создаваемого элемента. Как правило, период полураспада становится короче с увеличением атомного номера, хотя для неизученных изотопов с определённым числом протонов и нейтронов может существовать «островок стабильности».
С чем совпадает зарядовое число
Учебник Физика 7 класс Кривченко И.В., размещённый в этой рубрике, включён в федеральный перечень учебников в соответствии с ФГОС. Учебник в цветном полиграфическом исполнении с твёрдым переплетом объёмом 150 страниц вышел из печати в июле 2015 г. в пятом издании. Учебник физики 7 класса рассчитан на 2 урока в неделю и содержит 6 тем курса физики, которые перечислены ниже.

Физика. Физическая величина. Измерение физических величин.
Цена делений шкалы прибора. Погрешность прямых и косвенных измерений.
Формулы и вычисления по ним. Единицы физических величин.
Метод построения графика.

Явление тяготения и масса тела. Свойство инертности и масса тела.
Плотность вещества. Таблицы плотностей некоторых веществ.
Средняя плотность тел и их плавание.
Метод научного познания.

Сила и динамометр. Виды сил.
Уравновешенные силы и равнодействующая.
Сила тяжести и вес тела. Сила упругости и сила трения.
Закон Архимеда. Вычисление силы Архимеда.
Простые механизмы. Правило равновесия рычага.

Определение давления. Давление жидкости. Закон Паскаля. Давление газа.
Атмосферное давление. Барометр Торричелли. Барометр-анероид.
Вакуумметры. Манометры: жидкостные и деформационные.
Пневматические и гидравлические механизмы.

Механическая работа. Коэффициент полезного действия. Мощность.
Энергия. Кинетическая и потенциальная энергия.
Механическая энергия. Внутренняя энергия.
Взаимные превращения энергии.

Температура и термометры. Количество теплоты и калориметр.
Теплота плавления/кристаллизации и парообразования/конденсации.
Первый закон термодинамики. Двигатель внутреннего сгорания.
Теплота сгорания топлива и КПД тепловых двигателей.
Теплообмен. Второй закон термодинамики.
 |
Учебник Физика 8 класс Кривченко И.В., размещённый в этой рубрике, включён в федеральный перечень учебников в соответствии с ФГОС. Учебник в цветном полиграфическом исполнении с твёрдым переплетом объёмом 150 стр. вышел из печати в июле 2015 г. в четвёртом издании. Учебник физики 8 класса рассчитан на 2 урока в неделю и содержит 5 тем курса физики, которые перечислены ниже.

Из истории МКТ. Частицы вещества. Движение частиц вещества.
Взаимодействие частиц вещества. Систематизирующая роль МКТ.
Кристаллические тела. Аморфные тела. Жидкие тела. Газообразные тела.
Агрегатные превращения. Насыщенный пар. Влажность воздуха.

Строение атомов и ионов. Электризация тел и заряд.
Объяснение электризации. Закон сохранения электрического заряда.
Электрическое поле. Электрический конденсатор. Электрический ток.
Электропроводность жидкостей, газов и полупроводников.

Электрическая цепь. Сила тока. Электрическое напряжение. Работа тока.
Закон Ома для участка цепи. Сопротивление соединений проводников.
Закон Джоуля-Ленца. Электронагревательные приборы.
Полупроводниковые приборы. Переменный ток.

Магнитное поле. Соленоид и электромагнит. Постоянные магниты.
Действие магнитного поля на ток. Электродвигатель на постоянном токе.
Электромагнитная индукция. Электротрансформатор. Передача электроэнергии.
Электродвигатель на переменном токе.

Период, частота и амплитуда колебаний. Нитяной и пружинный маятники.
Механические волны. Свойства механических волн. Звук.
Электромагнитные колебания. Излучение и прием электромагнитных волн.
Свойства электромагнитных волн. Принципы радиосвязи и телевидения.
 |
Учебник Физика 9 класс Кривченко И.В., размещённый в этой рубрике, включён в федеральный перечень учебников в соответствии с ФГОС. Учебник в цветном полиграфическом исполнении с твёрдым переплетом объёмом 150 стр. вышел из печати в июле 2015 г. в третьем издании. Учебник физики 9 класса рассчитан на 2 урока в неделю и содержит 4 темы курса физики, которые перечислены ниже.
Для перехода к параграфам кликайте нумерацию 01 02 03 04 05 и т.д. вверху страницы. Параграфы каждой темы курса физики снабжены интерактивными вопросами и заданиями.