рандомизированное исследование что это значит
Доказательная медицина: как это работает?
Поделиться:
В последние годы этот термин все чаще звучит с экранов телевизоров. Из контекста зрителю ясно, что соответствие принципам доказательной медицины — это хорошо, а несоответствие — плохо.
Но вот в чем, собственно, заключается кардинальное различие между двумя этими полюсами? И какие преимущества предлагает доказательная медицина для конкретного пациента? Давайте разбираться.
Под одной гребенкой
Врачи всегда принимали решения, основываясь на доказательствах. Однако вплоть до второй половины XX века доказательства для каждого доктора могли быть свои.
Для одних ими были смутные воспоминания об изучаемых когда-то дисциплинах, для других — советы коллег и собственный опыт, для третьих — общее впечатление о том, как следует лечить «правильно». Такая практика приводила к серьезным различиям в стратегиях диагностики, подборе терапии и эффективности лечения.
Поставить точку в череде случайностей, которые определяли шансы больного на выздоровление, и позволила доказательная медицина. Ее концепцию предложил британский исследователь Арчи Кокрейн в 1972 году.
Читайте также:
Грипп и простуда: почувствуйте разницу
В своей книге «Действенность и Эффективность: Случайные размышления о медицинской службе» он подчеркивал: поскольку врач не в состоянии изучить все необходимые информационные ресурсы, чтобы принять верное решение, медицинская помощь должна базироваться на правильно спланированных исследованиях, соответствующих четким критериям эффективности.
Проще говоря, Кокрейн предложил некий стандарт, который позволял врачу уверенно двигаться в верном направлении.
Опираясь на выводы Кокрейна, ученые из Северной Каролины и Торонто в конце 80-х-начале 90-х годов прошлого века предложили термин доказательной медицины и сформулировали ее критерии, которые остались неизменными до сегодняшнего дня.
Принципы доказательной медицины
Доказательная медицина гласит: лечить нужно только тогда, когда есть доказательства выгоды для пациента и, наоборот — лечить нельзя, если есть доказательства бесполезности или вреда для больного.
Способы лечения и препараты должны пройти проверку на эффективность и безопасность в клинических исследованиях, проведенных по четким, строгим правилам.
Исследования могут иметь различный план, от которого зависит их качество и результат.
В основу доказательной медицины положены рандомизированные контролируемые исследования (РКИ), которые в идеале должны быть еще и двойными слепыми — именно такой дизайн позволяет получить максимально точные, непредвзятые результаты.
Рандомизированное исследование — эксперимент, в котором участники случайным образом разделяются на несколько групп. Одна из них принимает исследуемый препарат или метод лечения, а вторая — получает плацебо, то есть пустышку или стандартную методику.
Слепое исследование подразумевает, что либо его участник, либо исследователь не знает, какое лечение получает пациент.
В двойном слепом исследовании в неведении остаются обе стороны: ни участник, ни исследователь не знают, что принимает пациент — исследуемое лекарство или пустышку.
В таком случае вероятность преднамеренных искажений сводится к минимуму, а риск непреднамеренных ошибок распределяется равномерно между группами участников.
Самыми «доказательными» считаются двойные слепые плацебоконтролируемые исследования, проведенные на большом количестве пациентов.
Им присвоен I уровень доказательности (класс А). Остальные исследования априори менее «доказательные»:
Очевидно, что чем выше класс доказательности, тем более высокое качество имеет исследование, а, значит, его результаты более точные.
Доказательная медицина на практике
Итак, теория в общих чертах ясна, но как применять ее на «живых» пациентах? Доказательная медицина предусматривает и это. Использование ее принципов на практике включает несколько последовательных шагов:
• Формулировка клинического вопроса, например: о каком заболевании, скорее всего, идет речь? Каковы его причины? Как его диагностировать? Каков прогноз?
• Сбор доказательств, которые позволят дать ответы на поставленные вопросы. Идеальный источник информации должен содержать высококачественные данные, быть применимым в клинической практике, содержать данные обо всех преимуществах и о вреде всех вмешательств и препаратов, а также быть удобным в использовании. Сегодня в качестве самых достоверных источников информации используются протоколы лечения (на западе их называют гайдлайнами), а также данные РКИ класса I.
• Критическая оценка качества информации. Мало отыскать исследование или рекомендации по интересующему врача вопросу — нужно еще и уметь его адекватно оценить. Ключевой вопрос, на который необходимо ответить доктору: «Достаточно ли я верю результатам этого исследования, чтобы использовать его принципы для своих пациентов?»
• Принятие решения о том, как использовать результаты исследования или рекомендации в конкретном случае. Это — один из самых сложных шагов, требующих от врача и знаний, и опыта. Именно на этом этапе доктор взвешивает соотношение пользы лечения и риска неблагоприятных реакций и делает выбор в пользу метода терапии или препарата.
На первый взгляд, алгоритм прост, но на самом деле доказательная медицина не предлагает легких путей. Это сложный, но чрезвычайно эффективный инструмент. Им можно воспользоваться и предоставить пациенту качественную медицинскую помощь, а можно и положить на пыльную полку и забыть о его существовании.
И хотя сегодня еще далеко не все врачи используют современные инструменты по назначению, будущее за теми, кто ищет и находит истину. А, значит, победа доказательной медицины неизбежна. Во всяком случае, в это хочется верить.
Мнение автора может не совпадать с мнением редакции
Научная электронная библиотека
Наумова Е. А., Шварц Ю. Г., Семенова О. Н.,
Рандомизированные клинические исследования
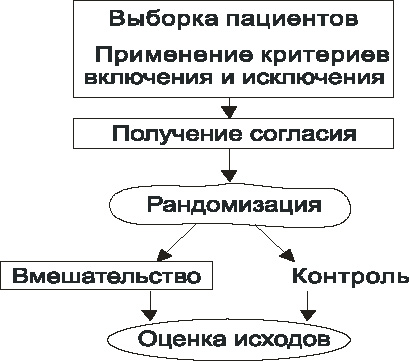
Общая схема РКИ приведена на рис. 8.
Рандомизация – это процесс случайного распределения испытуемых в группу вмешательства и группу контроля. Именно она является основным моментом в проведении РКИ. Однако обратите внимание, что это не первый этап исследования. Первым этапом происходит формирование выборки пациентов: определяется круг лиц, максимально похожих друг на друга (насколько это возможно), и происходит это на основании критериев включения и исключения, описанных в протоколе исследования.
Это основной документ, в котором подробнейшим образом описываются обоснование исследования, его цели, задачи, дизайн, критерии включения и исключения, все процедуры исследования. Четко описываются все манипуляции с пациентом: когда, на какие сутки/или минуты, будет забираться кровь, выполняться электрокардиография (ЭКГ), биопсия или какие-либо иные действия. Протокол пишется разработчиками – экспертами, одобряется регуляторными органами, и именно по данному документу в дальнейшем работают все врачи-исследователи, принимающие участие в эксперименте. Благодаря этому врачи разных исследовательских центров выполняют одинаковые действия, строго следуя протоколу исследования. Отклонения от протокола исследования не допустимы, но если они случаются, то это документируется и сообщается и организаторам, и регуляторным органам. Если по ходу исследования было допущено множество отклонений от протокола, то его результаты могут быть поставлены под сомнение, и разработчикам может быть отказано в регистрации препарата.
Критерии включения и исключения
Это подробное описание тех симптомов, признаков, показателей, которые обязательно должны быть у пациента (критерии включения), и которых не должно быть ни в коем случае (критерии исключения). Например, в исследование включаются пациенты старше 40 лет, но не старше 71 года, поступившие не позднее 2 часов от появления клинических симптомов острого коронарного синдрома (ОКС), обязательно имеющие элевацию сегмента ST не менее 1 мм в не менее чем 2 смежных стандартных отведениях и/или не менее 2 мм в 2 смежных грудных отведениях. При этом у них не должно быть острой сердечной недостаточности Killip 3-4, не должно быть онкологических заболеваний, почечной, печеночной недостаточности. Это делается для того, чтобы группа пациентов, которые могут участвовать в исследовании была максимально однородной. Если пациент соответствует основным критериям включения и не имеет критериев исключения, то ему предлагают участвовать в данном клиническом исследовании. Врач-исследователь проводит с пациентом беседу, в ходе которой он объясняет суть исследования, риски и пользу от участия в исследовании, и предлагает для ознакомления документ, под названием ИС.
Информированное согласие (ИС)
Основополагающим документом, определяющим этические принципы проведения биомедицинских исследований с участием людей, является Хельсинкская Декларация Всемирной Медицинской Ассоциации. Хельсинкская Декларация гласит: «При проведении любого исследования с участием людей в качестве субъектов каждый потенциальный субъект исследования должен быть надлежащим образом проинформирован о целях, методах, ожидаемой пользе и возможном риске исследования, а также о неудобствах, которые могут быть вызваны экспериментом. Участники исследования должны быть проинформированы о том, что они имеют неограниченное право отказаться от участия в исследовании и в любое время взять назад согласие на участие. Врач должен получить такое согласие – свободное и информированное – от субъекта исследования, желательно в письменном виде».
Пациенты могут включаться в научное исследование только после того, как они получили полную информацию о нём и дали осознанное и добровольное согласие на участие.
Получение ИС – важнейший элемент надлежащего проведения любого исследования на человеке. Этот процесс строго регламентирован. Письменную форму ИС (сейчас в России Информационный листок пациента и Форма ИС) для КИ составляет фирма-спонсор или сам врач-исследователь (если он проводит свое, менее масштабное, например диссертационное исследование).
ИС обязательно должно содержать следующую информацию:
1. Кто проводит данное исследование?
3. Какой препарат (метод) исследуется, что он из себя представляет. Используется ли плацебо или какая-либо контрольная терапия?
4. Подробнейшее описание всех процедур исследования (сколько раз пациент посещает исследовательский центр, какие исследования выполняются и когда (максимально детально, вплоть до количества миллилитров крови, которое будет забрано).
5. Что потребуется от пациента (например, регулярное посещение центра)?
6. Каковы возможные риски и неудобства от участия в программе?
7. Какую пользу может получить пациент от своего участия в эксперименте?
8. Какая компенсация предусмотрена в случае нанесения вреда здоровью?
9. Предусмотрена ли оплата за участие в эксперименте (характерно для 1 фазы КИ)?
10. В обязательном порядке подчеркивается добровольность участия в исследовании (указывается, что в случае отказа – никакого влияния на стандартную помощь и терапию это не окажет) и возможность отказа от участия в нем в любой момент (и даже без объяснения причин).
11. Гарантируется конфиденциальность всей информации о пациенте (никто, кроме самого врача-исследователя не будет знать, что вся информация о данном участнике исследования – это данные, в том числе и персональные, принадлежащие именно данному человеку, все остальные участники процесса будут получать данные пациента только в обезличенном виде).
12. Оговаривается возможность проведения проверок (при соблюдении конфиденциальности) представителями официальных инстанций.
13. Указываются имена и телефоны контактных лиц (врача-исследователя, этического комитета).
14. Обязательно вносится предупреждение о том, что одномоментно пациент может участвовать только в одном клиническом исследовании.
ИС обязательно предоставляется на родном языке пациента (если необходим перевод, то он осуществляется сертифицировано) Форма согласия должна быть удобна для чтения (не мелкий шрифт, четкость и последовательность изложения информации). Документ утверждается официальными инстанциями страны, где проходит КИ и Комитетом по Этике.
Важно помнить, что ИС получается ДО выполнения любых действий с пациентом в рамках исследования, а не только до непосредственного назначения исследуемого препарата. Что это означает? Ни одно обследование, измерение, назначение в рамках протокола (а не стандартной практики) не может происходить без подписанного ИС, даже если это безболезненная и безопасная процедура, например обычный осмотр пациента или ультразвуковое исследование почек. Если данные процедуры выполняются только по причине участия в протоколе, то это уже эксперимент, и требуется согласие пациента. С другой стороны, если, например проводится исследование среди стационарных пациентов с пневмонией, то выполнение рентгенологического исследования легких является процедурой, обязательной для всех, не зависимо от участия в исследовании. В этом случае, подписывать дополнительное согласие на рентген нет необходимости, оно включено в стандартное согласие пациента на предложенный план лечения в стационаре. Если в протокол исследования вносятся какие-либо изменения, так или иначе связанные с пациентом (появляется новая информация о лекарственном средстве, изменяются процедуры исследования), то должна быть подготовлена, затем одобрена соответствующими инстанциями, а затем и подписана пациентом новая версия ИС, содержащая все внесенные изменения.
При получении ИС пациент не может быть как-либо ограничен во времени. Он может забирать форму для ознакомления домой. Может показывать форму согласия любому другом врачу, родственнику, адвокату, т. е. любому лицу, с которым захочет посоветоваться.
Форма ИС собственноручно подписывается и датируется пациентом в двух оригинальных экземплярах. Затем форму подписывает и датирует врач-исследователь, проводивший разъяснительные беседы с пациентом. Один оригинал согласия остается в исследовательском центре, а второй оригинал – забирает пациент. В истории болезни пациента обо всем этом делается соответствующая запись.
Если пациент не может сам подписать ИС (это несовершеннолетний ребенок, лицо, признанное в законном порядке недееспособным), то согласие за него может подписать его законный представитель или официально назначенный опекун.
Если пациент не может сам прочесть форму ИС (например, вследствие проблем со зрением), то в процессе чтения, и обсуждения принимает участие Свидетель (независимое лицо, не связанное с персоналом клиники). Он помогает пациенту, и в этом случае также подписывается в специальных строках формы согласия (после подписания формы пациентом).
В редких случаях возможно включение пациента в исследование без подписания ИС. Это относится к исследованиям, в реанимационной практике, когда велика вероятность поступления пациента без сознания, и без сопровождающих официальных лиц. Это подробно описывается в протоколе исследования. Такие испытания нуждаются в очень весомых обоснованиях и также проходят одобрение официальных инстанций и Этического комитета. После того, как пациент пришел в себя, с ним проводится беседа, описывается суть произошедшего, и пациент знакомится с информационным листком пациента и формой ИС. Если пациент их подписывает, то он продолжает участие в эксперименте, если пациент отказывается (а он имеет на это полное право), то его участие в научном исследовании завершено, он продолжает только стандартное лечение.
Как мы уже обсуждали выше, рандомизация – это процесс случайного распределения заранее отобранных, имеющих максимально сходные характеристики испытуемых в основную и контрольную группы. Сам термин «рандомизация» произошел от англ. слова random, т. е. случайный выбор.
Рандомизация – наиболее оптимальный способ распределения испытуемых в группы, так как именно он позволяет минимизировать возможность систематической ошибки.
Систематическая ошибка (bias) – это «систематическое (неслучайное, однонаправленное) отклонение результатов от истинных значений». Она может быть связана с отбором пациентов (selection bias), с процедурами измерения (measurements bias) и с вмешивающимися факторами (confounding bias).
Почему так важен отбор пациентов? Достаточно очевидно, что при сравнении двух групп, существенно отличающихся друг от друга (например, по возрасту или тяжести заболевания), невозможно сравнивать их исходы (как при наличии медицинского вмешательства, так и нет). То есть, у кого тяжесть заболевания выше, всегда будут иметь больше негативных исходов, чем пациенты с более легкой формой болезни. Отбор пациентов по строгим критериям включения и исключения с последующим случайным распределением в основную группу и группу контроля и направлен на предотвращение данной ошибки.
Ошибка, обусловленная измерением, связана с различными способами оценки каких-либо параметров в двух исследуемых группах. Это могут быть погрешности измерения в различных лабораториях (и поэтому очень часто в КИ используют единую центральную лабораторию), различия в измерениях какого-либо интервала на ЭКГ, различия в опросе пациента, и акцентирование или нет при разговоре с ним на какие-либо факторы. Для нивелирования этих факторов в КИ и используют унифицированные процедуры работы с пациентами, строго прописанные в протоколе, очень часто – в различные центры для измерений поставляются одинаковые измерительные приборы, как уже отмечалось выше, используется центральная лаборатория.
Ошибка, связанная с действием вмешивающихся факторов. Очень часто два каких-либо фактора сильно взаимосвязаны между собой, и возможна ситуация, когда из-за этого неверно оценивается эффект каждого из факторов.
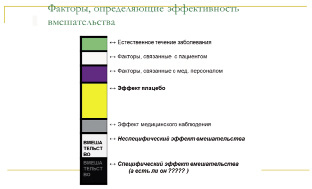
Если рассматривать КИ эффективности вмешательств, то условно все факторы, так или иначе влияющие на эту самую эффективность (т. е. на исходы) можно представить рис. 9.
Во-первых, у любого заболевания есть свое определенное течение, и очень часто это чередование обострений и ремиссий. Если вы набираете пациентов в фазу обострения, а затем фиксируете выздоровление, то как определить связано это выздоровление с применимым вмешательством (например, лекарственным средством), или с естественным течением заболевания (выздоровление наступило самостоятельно, независимо от вашего лечения). Задумайтесь, ведь не случайно имеется такое количество «эффективных» средств от простуды? Большинство простудных заболеваний всегда заканчиваются выздоровлением, независимо от использованных средств (помните поговорку, насморк без лечения проходит за неделю, а с лечением – за 7 дней). Именно этим и пользуются недобросовестные производители, которые проводят нерандомизированные исследования своих «чудо – препаратов», фиксируют выздоровление пациентов, и даже не пытаются обосновывать реальную взаимосвязь между улучшением самочувствия пациента и применением «чудо-средства».
Рис. 9. Факторы, определяющие эффективность вмешательства
Факторов, связанных с пациентом и с его врачом также немало. К сожалению, все люди имеют особенности, которые могут влиять не только на течение заболевания, на оказание помощи пациенту, но и на восприятие каждого фактора, в том числе и тех, оценка которых является целью исследования.
Эффект плацебо также существует, также, как и эффект самого вмешательства, т. е. так называемый эффект Хортона. Эффект Хортона в данном случае проявляется тем, что повышенное внимание к испытуемому, дополнительные обследования и вмешательства повышают положительное восприятие пациентом своего участия в эксперименте и того лечения, которое он получает, и тем самым искажает результаты исследования. Все это в итоге крайне затрудняет оценку эффективности именно изучаемого вмешательства. Только правильно организованные КИ с отбором схожих пациентов и случайным делением на группы, в каждой из которых и будут действовать все описанные факторы, позволяют делать вывод об эффекте изучаемого препарата/прибора/процедуры: если все другие факторы одинаково действовали в двух группах, то разница в исходах как раз и связана с проводимым лечением.
Типы рандомизации представлены на рис. 10.
Рис. 10. Типы рандомизации (Р. Флетчер Клиническая эпидемиология)
Фиксированная рандомизация – пациент попадает в группу вмешательства или контроля строго на основании заранее сгенерированных/запрограмированных таблиц, последовательностей чисел и т. п. Изменений в данных последовательностях по ходу исследования не происходит.
Простая рандомизация – для каждого участника пациента вероятность попадания в группу вмешательства или контроля 50/50 %. Типичный пример – подбрасывание монетки: орел или решка. При таком подходе группы могут различаться, а иногда и существенно и по числу испытуемых в группе, и по некоторым характеристикам (пол, возраст и т. п.)
Блоковая рандомизация – для достижения большей сбалансированности между группами, все участники делятся на блоки, в каждом из которых всегда равное число участников группы контроля или вмешательства, однако последовательность участников в каждом блоке случайна и неизвестна (рис. 11). Пациент рандомизируется в определенный блок, и занимает в нем порядковое место. При таком подходе группы получаются более сбалансированными, но если исследователю будет известен размер блока, то он может повлиять на распределение пациентов в группы.
Рис. 11. Метод блоковой рандомизации
Стратифицированная (послойная) рандомизация – при распределении в группы учитывается ряд факторов (например пол, возраст, ключевые особенности заболевания). Таким образом опять же достигается большая сбалансированность исследуемых групп.
Динамическая рандомизация – распределение пациентов по группам «балансируется» по ходу исследования.
Метод «несимметричной монеты» – применяется для достижения более равномерного распределения участников в группы по определенному критерию. Например, нам важно, чтобы по возрасту группы были максимально идентичны. В этом случае, если при рандомизации в какой-либо из групп участников молодого возраста меньше, то очередной участник молодого возраста будет иметь больше шансов (обычно 66,6 %, но не более!) попасть именно в эту группу. Если же на данном этапе набора участников исследования по возраст группы сопоставимы, то новый испытуемый имеет шансы оказаться в группе вмешательства/контроля 50/50.
При адаптивной рандомизации – распределение участников в группы динамически меняется так, чтобы к концу исследования наибольшее число испытуемых получило более эффективный способ терапии (это определяется после промежуточных анализов же, собранных по ходу данного исследования баз данных). Минусом такой рандомизации является необходимость частичного раскрытия данных для определенной группы аналитиков, и сложность контроля за этим.
Как на практике выглядит рандомизация? В многоцентровых клинических исследованиях она может быть локальной (на территории самой клинической базы), либо централизованной. В первом случае это как правило метод конвертов: исследователь центра получает ряд запечатанных, пронумерованных конвертов, в каждом из которых указан вид лечения/препарата. Согласно определенным процедурам протокола пациенту назначается один из конвертов, и препарат с номером, указанным внутри.
В настоящее время наиболее часто используется централизованная рандомизация. Врач-исследователь вводит определенные обезличенные данные пациента (пол, возраст, тяжесть заболевания и др.) через специальную телефонную линию или интернет в специальную единую компьютерную систему, в которой и происходит рандомизация, т. е. распределение пациента в одну из двух групп, и в ответ врач получает номер упаковки с ИП. Все упаковки имеют одинаковый внешний вид, а препарат в них в идеале должен иметь не только одинаковый внешний вид, но и одинаковый запах, вес, вкус, и для исследователя и пациента отличаются только номером. Упаковка с указанным номером выдается пациенту.
Что такое РКИ? Рандомизированные контролируемые клинические исследования
РАНДОМИЗИРОВАННЫЕ КОНТРОЛИРУЕМЫЕ
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Что такое РКИ? Рандомизированныеконтролируемые клинические исследования (РКИ) проводятся с серединыпрошлого века. Их гуманистическая направленность стала ответом научногосообщества на проведение экспериментов на людях во время Второй мировойвойны в фашистских концлагерях. РКИ являются фундаментом доказательноймедицины, так как на их основе происходит принятие научно-обоснованныхрешений и проводится мета-анализ. Поэтому целесообразно более подробноостановиться на особенностях их планирования и проведения. РКИпредполагают использование тонких и чувствительных операционных истатистических методов во время проспективного исследования, в которомсопоставляемые группы получают различные виды анализируемыхвмешательств, лица контрольной группы — стандартное по современнымпредставлениям лечение.
Отличительной особенностьюсовременных РКИ является неукоснительное следование этическим нормам.Перед началом любого РКИ его протокол должен быть одобрен национальнымили региональным этическим комитетом (часто и тем, и другим). Вдальнейшем этический комитет в обязательном порядке информируется осерьезных побочных эффектах, возникших в ходе РКИ и всех изменениях впротоколе. До включения в исследование его потенциальный участник долженна добровольной основе подписать информированное согласие, где вдоступной форме должна быть изложена цель исследования, возможныеосложнения или неудобства, преимущества, связанные с участием больного висследовании, и альтернативные методы лечения. Пациент должен бытьпроинформирован о том, что решение о его участии или неучастии в данномклиническом исследовании на любом этапе выполнения никак не отразится надальнейшей тактике его ведения, и он в любой момент может прекратитьсвое участие в РКИ. Только после получения информированного согласияпациент может принимать участие в исследовании. Если РКИ предполагаетпроведение суб-исследований,требующих дополнительного обследования, то на них тоже необходимополучить информированное согласие пациента. В ряде случаев, например припроведении РКИ у детей, информированное согласие подписывают родителиили опекуны.
ЦЕЛИ И ЗАДАЧИ ИССЛЕДОВАНИЯ
Дляоценки новых методов лечения и диагностики могут применяться дваосновных вида исследования — контролируемые и неконтролируемые.Неконтролируемое клиническое испытание (без сравнения с ужеприменяющимся способом терапии или плацебо) новых методов лечениядопустимо только в исключительных случаях, когда новый метод позволяетспасти жизнь или радикально улучшить прогноз у пациентов, страдающихнеизлечимым заболеванием (в настоящее время большинство такихисследований связано с ВИЧ-инфекцией). Необходимо подчеркнуть, что даже вэтом случае предполагаемая польза нового метода должна бытьубедительной и сопоставимой, например, с эффектом инсулина при сахарномдиабете I типа.
Особняком стоят неконтролируемыеклинические испытания при изучении новых лекарственных препаратов наэтапе фазы I и II их клинического исследования, когда на здоровыхдобровольцах и ограниченном числе пациентов определяютсяфармакокинетические и фармакодинамические характеристики нового методалечения.
Актуальность проведения контролируемыхклинических исследований в настоящее время существенно возросла, так какони необходимы не только для доказательной медицины, но и привыполнении рутинной научной работы, в том числе и диссертационныхисследований клинической направленности.
ПланированиеРКИ начинается с формулирования цели и задач исследования, которыеотличаются новизной и практической значимостью. Цель исследования должнаотличаться как научной новизной, так и практической значимостью.Например, именно таким исследованием было SYST-EUR, результаты которого взначительной степени реабилитировали антагонисты кальция в леченииартериальной гипертензии, когда на них обрушилась волна критики порезультатам не совсем корректного мета-анализа.
Поэтому,как правило, крупные многоцентровые РКИ планируют известные в своейобласти специалисты. Каждое новое РКИ оригинально по дизайну и популяциипациентов, участвующих в нем (определяется критериями включения иисключения), поэтому уже существующие протоколы не могут быть полностьювоспроизведены вновь, хотя и могут служить некой базой для адаптации. Вкачестве примера решения сходной задачи можно привести два сильноразличающихся как по дизайну, так по итоговым результатам протоколаисследований ALLHAT и ASCOT. Точная формулировка основной цели имеетрешающее значение. Так, можно в качестве примера привести исследованиеELITE I, в котором сравнивалась эффективность ингибитора АПФ каптоприла иантагониста рецепторов ангиотензина II лозартана у пациентов схронической сердечной недостаточностью. Достоверных различий между этимидвумя режимами терапии не выявлено, но цель исследования была «доказатьпреимущества лозартана», и она не была достигнута. Однако новый класспрепаратов, оказавшийся не хуже эталонных ингибиторов АПФ, стал важнымсобытием для кардиологов. Если бы целью исследования было доказательстворавнозначной эффективности лозартана и каптоприла при хроническойсердечной недостаточности, никакой последующей полемики попросту невозникло.
Задачи, решаемые в РКИ, не должны бытьмногочисленными, поскольку это может привести к ложноположительнымрезультатам и затруднить интерпретацию полученных данных для практики.
критерияоценки, вызываемые лечением, должны отражать изменения клиническизначимого критерия (исхода)». Необходимость использования суррогатныхконечных точек обусловлена тем, что для получения статистическидостоверного влияния вмешательства на жесткие точки необходимообследовать большое число пациентов и наблюдать их на протяжениидлительного времени. Суррогатные конечные точки (типичные для каждойнозологии) позволяют существенно уменьшить длительность исследования иколичество больных, участвующих в нем. Однако обязательно нужно помнить:выбранные суррогатные точки должны иметь доказанное влияние на прогнозисследуемого заболевания. Безусловно, выбранным конечным точкамнеобходимо иметь не только научное, но и клиническое значение.Предпочтение отдается объективным (например, развитие инсульта,подтвержденное компьютерной томографией), стандартизованным критериям(индекс массы миокарда левого желудочка по данным эхокардиографии) идискретным показателям эффективности (показатели типа да/нет, жив/умер,госпитализация/отсутствие госпитализации, улучшение/ухудшение), покоторым рассчитывается абсолютный и относительный эффект вмешательства иих легко интерпретировать практическому врачу.
Вмногих РКИ выделяют основные конечные точки, по которым оцениваетсяэффективность вмешательства, и второстепенные конечные точки,учитывающие другие аспекты этого вмешательства (например, побочныеэффекты, качество жизни, когнитивные нарушения, лабораторные показатели ит.д.). Хотя в ряде случаев последние сами могут становиться основнойконечной точкой (например, когнитивные изменения в исследовании SCOPE,холестерин — в исследованиях по атеросклерозу, уровень креатинина — висследованиях по почечной недостаточности, артериальной гипертензии исахарному диабету).
Существеннооблегчить задачу по выбору оптимальных конечных точек при планированииисследований может использование существующих баз данных о клиническихисходах (табл. 7.1).
Таблица 7.1. Источники информации рекомендуемых для оценки клинических показателях при проведении исследований
Ещеодной особенностью современных РКИ является проведение суб-исследований(суб-протоколов) в рамках основного РКИ, которые используютдополнительные методы обследования и позволяют ответить надополнительные вопросы, остававшиеся за рамками основного РКИ.
Длительность исследования (интервал времени от момента рандомизации больного и осуществления вмешательства до момента
оценкиконечного исхода заболевания) определяется целью и задачамиисследования, зависит от характера патологии, особенностей естественноготечения заболевания, риска развития исследуемых осложнений и времени,необходимого вмешательству для оказания потенциального влияния навыбранные конечные точки.
Вторымпо значимости разделом РКИ (после формулирования цели и задачисследования) является определение критериев включения и исключения изисследования. Критерии включения предопределяются целью исследования,более широкие из них облегчают набор пациентов и позволяютэкстраполировать полученные результаты на большую популяцию больных.Однако в этом случае существует опасность формирования разнородныхисследуемых групп больных как по исходным клинико-демографическимпоказателям, так и по эффективности тестируемого вмешательства. Обычно вРКИ включают пациентов со средней тяжестью заболевания, хотя упациентов с исходно более высоким риском осложнений можно в болеекороткие сроки оценить эффект вмешательства на жесткие конечные точки.Группа пациентов с низким риском и легким течением заболевания требуетдлительного наблюдения и потенциально опасна в получении статистическидостоверного эффекта вмешательства, тогда как на самом деле оно можетоказаться эффективным.
Критерииисключения должны минимизировать возможность ошибок при проведенииисследования (например, исключение из исследования больных стерминальной стадией заболевания, сниженной функцией печени и почек).Если данный контингент пациентов не является предметом РКИ, в негообычно не включают несовершеннолетних, женщин в период беременности илактации или не использующих контрацепцию, онкологических и психическихбольных. Важной задачей критериев исключения является обеспечениеодинакового лечения и ведение пациентов в исследуемой и контрольнойгруппах, а также исключение применения в них во время исследованияпрепаратов, сходных с испытуемым.
В целом чем крупнееРКИ и чем быстрее его планируют закончить, шире должны быть критериивключения и тем меньше критериев исключения.
Никакихнормативов, кроме получения необходимой статистической достоверностипри определении числа пациентов, участвующих в исследовании, несуществует. Небольшое количество пациентов не позволяет добитьсяоднородности сравниваемых групп и статистически достоверного эффектавмешательства. Размер РКИ зависит от ожидаемого клинически значимогоэффекта вмешательства.
Типичным исходным показателем,необходимым для расчета размера РКИ, является ожидаемый исходзаболевания при стандартном общепринятом лечении на момент планированияисследования. Кроме этого, весьма полезными оказываются данныезакончившихся РКИ по аналогичной тематике.
Принятосчитать, что снижение относительного риска исхода заболевания на 20%является клинически значимым. При этом степень достоверности полученияложноположительного обычно устанавливается на уровне 0,05 («а» или «Iтип ошибки»). В свою очередь степень достоверности ложноотрицательногорезультата обычно устанавливается на уровне 0,1 («b» или «II типошибки»).
РазмерРКИ, в котором в качестве критериев эффективности вмешательстваиспользуются дискретные показатели исхода заболевания, всегда больше,чем размер такого же РКИ, но в котором критерием эффективностивмешательства являются продолженные показатели исхода заболевания(средние величины показателя или функционального исхода).
Достаточностьгрупп наблюдения зависит от степени предполагаемых различий в эффектевмешательства в опытной и контрольной группах, видом статистическогопоказателя эффекта вмешательства (частоты, средние величины).Естественно, чем больше ожидаемое различие в эффекте между ними, темменьше окажется необходимое число наблюдений.
Приодинаковой степени точности необходимое число наблюдений будетзначительно меньше, когда для оценки эффекта вмешательства используютсясредние величины, а не частотные показатели.
Припроведении исследования очень важно получить достоверную информацию обэффективности вмешательства в возможно более сжатые сроки. Для этогоиспользуют многоцентровые РКИ. В них происходит кооперирование (частомеждународное) и стандартизация исследовательских центров по единойпрограмме и методам наблюдения, что позволяет получить сопоставимыеданные разных учреждений.
Надежностьданных РКИ прямо зависит от сопоставимости сравниваемых групп.Категорически нельзя сравнивать группы, в одну из которых были включеныпациенты с анализируемым вмешательством, а в другую — отказавшиеся отучастия в РКИ и получавшие «традиционную» терапию. Также нельзясопоставлять результаты нового метода лечения в разных клиниках, еслиони не проводили его оценку по одному общему протоколу (различий втехнической оснащенности, квалификации кадров и принятых стандартахлечения). Аналогичные недостатки имеет и метод «исторического контроля».
Рандомизация является ключевым моментом при проведении РКИ. Она должна обеспечить случайное распределение больных, независящее от желания врача или каких-либо других факторов, исопоставимость сравниваемых групп по клинико-демографическимхарактеристикам пациентов, тяжести основного исследуемого заболевания,сопутствующей патологии и проводимой терапии.
Принебольшом числе пациентов в группах даже правильно проведеннаярандомизация не может обеспечить их однородность. В этом случаеиспользуется предварительная стратификация (stratum — слой,пласт), при которой распределение вариантов вмешательства происходит вболее однородных группах больных, изначально сформированных по одномуили нескольким важным признакам. Различия пациентов по этим ключевымпризнакам должны быть минимальными. Такой подход практически гарантируетполучение надежных результатов и отсутствие систематической ошибки.Отсутствие систематической ошибки в РКИ называют обоснованностью(validity).
Наиболее частой причиной несопоставимостисравниваемых групп после рандомизации может быть включение в анализ невсех участвовавших в исследовании пациентов.
Существуетбольшое количество методов рандомизации: метод непрозрачныхзапечатанных и последовательно пронумерованных конвертов, компьютерныйметод (процедура рандомизации на основе метода генерации случайных чиселпроводится специалистом, непосредственно не участвующим в лечении),метод пронумерованных идентичных контейнеров, подготовленныхфармацевтической фирмой (код и истинное содержание контейнеров неизвестны ни пациентам, ни врачам, участвующим в исследовании),централизованная рандомизация по телефону (IVRS) специалистомфармацевтической фирмы. Наиболее объективным считается последний из них,а наименее объективным — метод конвертов.
Прирандомизации необходимо соблюсти одно важное условие — непредсказуемыйхарактер распределения больных на группы (нельзя предугадать, в группувмешательства или контроля попадет пациент). Ни пациент, ниисследователь не должны знать, в какие группы попадают пациенты. Этодостигается при использовании «слепого», «двойного слепого» и даже«тройного слепого» отбора. Если о назначаемом вмешательстве известнотолько врачу, такая организация РКИ называется «простым слепымиспытанием» (single-blind trial). Если все лица исследовательскогоцентра, общающиесяи работающие с пациентами, не знают, кто из них какое лечение получает,то это «двойное слепое испытание» (double-blind trial). Подобнаяорганизация РКИ абсолютно необходима в тех случаях, когда велика рольсопутствующего лечения, например при антибиотико- и химиотерапии.
Частопроцесс «ослепления» достаточно сложен, например традиционная терапияпредполагает применение таблетированных форм, а новое вмешательствоиспользует инъекции. В этом случае в первой группе лечение придетсядополнить введением физиологического раствора, а во втором — приемомплацебо per os. Нелишне отметить, что вид, органолептические свойства и кратность назначения сравниваемых препаратов должны быть одинаковыми.
В настоящее время существует несколько причин, по которым в научных исследованиях рандомизация не используется:
• незнание врачами-исследователями основ доказательной медицины;
• слепое следование традиционной практике и боязнь получить результаты, отличные от общепринятых и мнения авторитетов;
• боязнь применить у пациента менее эффективный метод вмешательства, ноименно ради выявления его реальной эффективности проводится РКИ;
• существующее негативное общественное мнение, отождествляющее РКИ с испытаниями на людях.
Втоже время в последние годы термин «рандомизация» стал использоватьсяавторами публикаций как «магическое заклинание», гарантирующее авторамотсутствие критики и повышающее их научный рейтинг самооценки. Истиннаярандомизация подменяется ее декларированием, проявляетсянесопоставимостью сравниваемых групп и «информационным шумом» от выводовпо некачественно сделанным исследованиям. Так, K.F. Schultz et al.считают, что только 9-15% статей в медицинских журналах имели истиннуюрандомизацию.
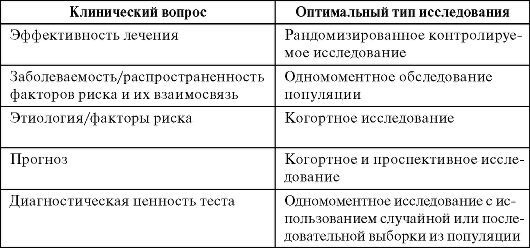
Сегоднядля решения конкретного клинического вопроса идентифицированыоптимальные типы (табл. 7.2) и дизайны (рис. 7.1) исследований. Каждыйиз видов исследований имеет свои достоинства и недостатки (табл. 7.4).
Таблица 7.2. Клинические вопросы и оптимальные типы исследований для их решения
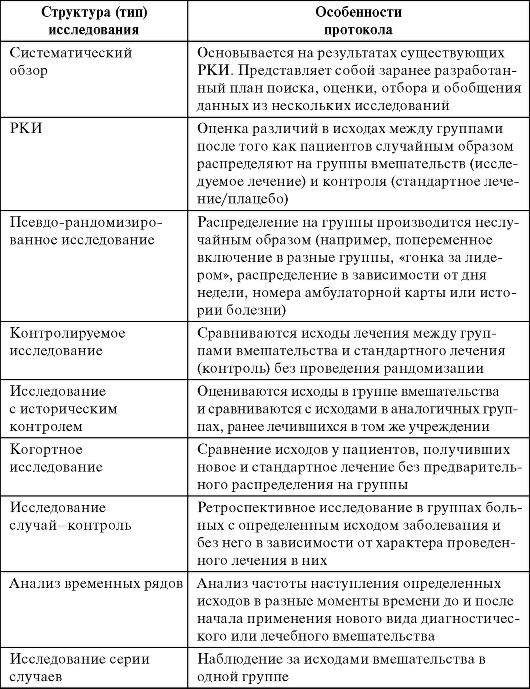
Важнопонять, что структура исследования, в существенной мерепредопределяемая поставленным клиническим вопросом, прямо влияет настепень доказательности полученных данных (табл. 7.3).
Рис. 7.1. Наиболее часто используемые дизайны проведения клинических исследований
Таблица 7.3. Уровень доказательности исследований в зависимости от их структуры при оценке эффективности вмешательства
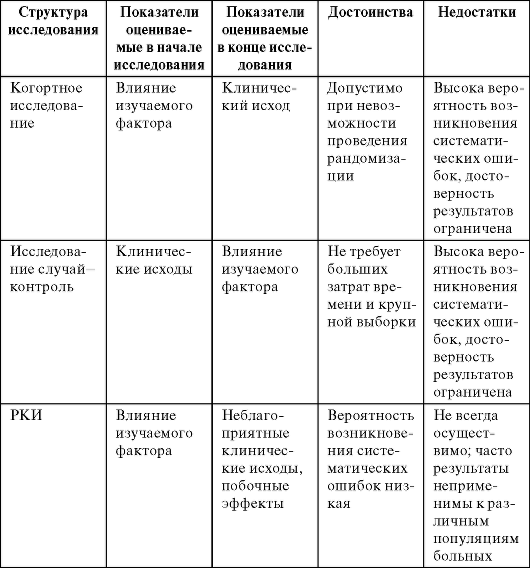
Таблица 7.4. Достоинства и недостатки исследований с различной структурой
АНАЛИЗ И ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ
Главной задачей статистического анализа РКИ является установление разницы и степени ее достоверности по исходам (конечным
точкам)между группой с анализируемым вмешательством и контрольной группой. Внастоящее время существует много пакетов статических программ дляанализа полученных результатов (BMDP, SOLO, Statistica и другие). Дляполучения объективной информации об эффективности вмешательства в анализнеобходимо включать всех первоначально рандомизированных больных(intention-to-treat analysis), а не только тех, которым лечениепроведено в строгом соответствии с протоколом исследования (on protocolanalysis). Это один из основных способов минимизировать возможныеошибки, когда при intention-to-treat analysis исходят из допущения, чтовсе пациенты получили лечение, предписанное при рандомизации.
Выбываниепациентов из исследования по разным причинам (отказ от дальнейшегоучастия, побочные эффекты и плохая переносимость лечения, нарушенияпротокола пациентами или исследователями) не должно превышать 15% отисходного числа рандомизированных больных. Если процент выше, результатыисследования некорректны. Такой подход существенно снижает вероятностьполучения ложноположительного результата, когда на самом деле онотсутствует. Считается: если более 80% из включенных больных наблюдалисьдо конца исследования, его результаты могут быть достаточно надежными.
Длястатистического анализа большого массива дискретных конечных точеквычисляют c-квадрат. При малой выборке (число пациентов менее 30 вкаждой из групп вмешательства) используют методы непараметрическойстатистики (тесты Фишера или Йетса).
Результатыисследования представляются с использованием следующих показателей:число больных, которых необходимо пролечить для того, чтобыпредотвратить один нежелательный исход заболевания,абсолютного/относительного риска нежелательного исхода и их снижения суказанием статистической достоверности.
Частостатью с итогами РКИ предваряет опубликование его наиболее значимыхрезультатов и выводов в материалах крупных международных конференций исъездов. Структура статьи имеет обычный характер. Обязательнымтребованием является максимально широкое представление дизайна истатистических аспектов РКИ. Особый интерес может представлятьобсуждение результатов, так как они
могут дать дополнительную информацию о спорных моментах при его проведении.
Внастоящее время для проведения РКИ разработаны этические иметодологические стандарты. Необходимо помнить о том, чтоплацебо-контролируемые исследования оправданы, когда не существуетальтернативного способа лечения, эффективность которого не вызываетсомнений.
Сегодня врачам, исследователям иорганизаторам исследований необходимо непрерывно повышать не толькопрофессионализм, но и уровень знаний в области доказательной медицины,правоведения и GCP. При этом само проведение РКИ — не только наука, но иособый (и достаточно прибыльный) медицинский бизнес, что предъявляетеще более высокие этические требования ко всем его участникам.
1. Pocock S.J. Clinical trials. A practical approach. — John Wiley & Sons
2. Guyatt G.H. etal. Users’ guides to the medical literature. II. How to use an articleabout therapy or prevention. A. Are the results of the study valid //JAMA. — 1993. — Vol. 270. — Р. 2598-2601.
3. Guyatt G.H. etal. Users’ guides to the medical literature. II. How to use an articleabout therapy or prevention. B. What were the results and will they helpme in caring for my patients // JAMA. — 1994. — Vol. 271. — P. 59-63.
4. Begg C. et al. Improving the quality of reporting of randomized controlled trials. The CONSORT statement // JAMA. — 1996. — Vol. 276 —
 Читайте также:
Читайте также: