появление резистентных штаммов микроорганизмов что это такое
Антибиотикорезистентность: аргументы и факты
Устойчивость к антимикробным препаратам создает угрозу для проведения эффективной профилактики и лечения постоянно возрастающего числа инфекций. Все более необходимым становится рациональное использование имеющихся антимикробных препаратов с учетом спектра их активности и профиля антибиотикорезистентности основных возбудителей. В связи с этим чрезвычайно актуально проведение научных и общественных мероприятий, направленных на обсуждение целого ряда вопросов, касающихся распространенности бактериальных инфекций, трудностей микробиологической диагностики, текущей ситуации с антибиотикорезистентностью и перспектив использования разных классов антимикробных препаратов при лечении инфекций различной локализации.
За последние 100 лет врачам удалось справиться со многими болезнями и значительно увеличить среднюю продолжительность жизни людей. Ряд открытий и изобретений в области медицины по праву можно отнести к числу наиболее значимых в прошлом столетии. Примерами могут служить появление первых кровезаменителей и расшифровка ДНК. Но, по мнению многих экспертов, именно изобретение пенициллина, внедрение его в клиническую практику и последующее бурное развитие антимикробной терапии (АМТ) сыграли наиболее существенную роль в увеличении продолжительности жизни людей в XX веке. Сегодня невозможно представить нашу жизнь без антимикробных препаратов (АМП), помогающих бороться с большинством инфекционных заболеваний [1].
Вместе с тем, в настоящее время во всем мире наблюдается совершенно объективный процесс глобальный рост антибиотикорезистентности микроорганизмов к АМП. Проблема резистентности во многом обусловлена широким и часто нерациональным использованием данных препаратов. Инфекции, вызванные резистентными штаммами микроорганизмов, характеризуются более тяжелым течением, чаще требуют госпитализации больного, увеличивают продолжительность пребывания его в стационаре, предполагают применение комбинированной АМТ с использованием резервных препаратов. Все это приводит к увеличению затрат на лечение, ухудшает прогноз для здоровья и жизни пациентов, а также создает условия для возникновения эпидемий. По данным Центра по контролю и профилактике заболеваний, в США ежегодно не менее 2 миллонов человек инфицируются бактериями, устойчивыми к антибиотикам, из которых примерно 23 тысячи умирают вследствие этих инфекций [2,3].
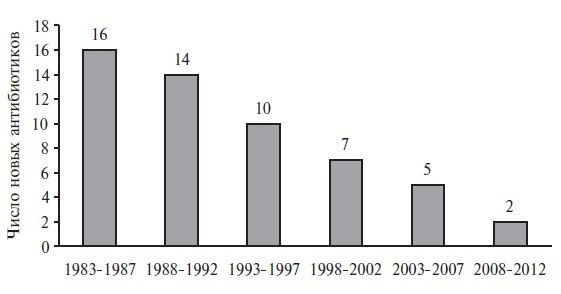
Несмотря на значительный прогресс в медицине, интенсивность разработки новых АМП за последние 30 лет значительно снизилась. Американское общество по борьбе с инфекционными болезнями в 2004 году сообщило, что за период 1998–2002 гг. количество одобренных Управлением по контролю за пищевыми продуктами и лекарственными средствами (FDA) новых антибиотиков уменьшилось на 56% по сравнению с периодом 1983–1987 г.
Во втором квартале 2014 года Всемирная организация здравоохранения опубликовала отчет об антибиотикорезистентности в мире. Это один из первых детальных докладов за последние 30 лет, касающийся столь актуальной глобальной проблемы. В нем проанализированы данные из 114 стран, в том числе России, на основании которых сделан вывод о том, что резистентность к антибиотикам на сегодняшний день отмечается уже во всех странах независимо от уровня их благосостояния и экономического развития. Российская Федерация в 2014 году со своей стороны стала инициатором подписания документа, в котором закреплено, что оценка ситуации с антибиотикорезистентностью в стране является национальным приоритетом. Сложившаяся ситуация имеет большое социально-экономическое значениеи рассматривается как угроза национальной безопасности. При неэффективности стартовой терапии клиницисты вынуждены использовать альтернативные АМП, которые часто характеризуются более высокой стоимостью и худшим профилем безопасности.
Все более необходимым становится рациональное использование имеющихся АМП с учетом спектра их активности и профиля антибиотикорезистентности основных возбудителей. В связи с этим чрезвычайно актуально проведение научных и общественных мероприятий, направленных на обсуждение целого ряда вопросов, касающихся распространенности бактериальных инфекций, трудностей микробиологической диагностики, текущей ситуации с антибиотикорезистентностью и перспектив использования разных классов АМП при лечении инфекций различной локализации [3,4].
Проблема антибиотикорезистентности
Значение проблемы антибиотикорезистентности подтверждается многими исследованиями. Согласно данным, опубликованным в 2014 году, при сохраняющихся темпах роста антибиотикорезистентности суммарные потери общемирового ВВП к 2050 году составят более 100 триллионов долларов, а количество случаев преждевременной смерти людей в два раза превысит численность населения России [5].
Монорезистентные организмы становятся полирезистентными, а затем и панрезистентными. Появилось понятие так называемых “проблемных” микроорганизмов, среди которых особенно часто, особенно в условиях стационара, где широко применяются АМП и дезинфектанты, встречаются штаммы, резистентные к тем или иным (ко всем известным) АМП. К таким микроорганизмам относятся Staphylococcus spp., Enterococcus spp., Pseudomonas aeruginosa, Acinetobacter spp., ряд штаммов бактерий семейства Enterobacteriaceae.
Одной из наиболее важных причин сложившейся ситуации является доступность АМП населению во многих странах мира и высокая частота самолечения, которое очень часто является неадекватным. Так, по данным Европейского центра по профилактике и контролю заболеваний, около 40% европейцев уверены в том, что антибиотики эффективны при простуде и гриппе.
Свой вклад в усугубление проблемы, к сожалению, вносят и врачи. Недостаточная осведомленность клиницистов относительно правил рациональной АМТ, а иногда и неспособность устоять перед настойчивыми просьбами пациентов и их родителей приводят к неоправданному или неадекватному назначению АМП. Отсутствие просветительской работы с пациентами, в частности о необходимости завершения полного курса АМТ, становится причиной досрочного прекращения лечения. Все это способствует формированию и распространению устойчивых штаммов микроорганизмов.
Многими экспертами не раз уже отмечено, что хотя генерические препараты являются важным инструментом снижения общих затрат здравоохранения, по целому ряду из них отсутствуют адекватные исследования эффективности и безопасности по сравнению с оригинальными препаратами. Несколько исследований, проведенных в Российской Федерации, продемонстрировали наличие более низких концентраций активных субстанций в ряде “псевдогенериков”, что потенциально может приводить не только к снижению эффективности терапииу конкретного пациента, но и более быстрому росту резистентности к целому классу антибиотиков. В настоящее время рассматривается возможность внесения поправок к Федеральному закону №61. Согласно предложенным поправкам для регистрации новых генериков необходимо будет проводить исследование биоэквивалентности регистрируемого генерика по сравнению с оригинальным препаратом, а не любым уже зарегистрированным генериком.
Одной из основных проблем получения достоверных данных в бактериологических лабораториях России является недостаточно хорошее оснащение. Использование нестандартизированных сред и дисков с антибиотиками приводит к получению ложных результатов. В связи с этим значительное количество данных о чувствительности различных микроорганизмов к АМП не может быть использовано для проведения рациональной эмпирической АМТ. Следует также с осторожностью относиться к публикациям в отечественных и зарубежных источниках, в которых отсутствует информация о методах определения чувствительности и критериях интерпретации результатов. Необходимо помнить о том, что данные, полученные в зарубежных странах, могут существенно отличаться от российских, поэтому их нельзя использовать для выбора АМП.
Ситуацию также усугубляет недостаточный контроль за использованием АМП в ветеринарии и сельском хозяйстве. Применение антибиотиков в животноводстве в качестве добавки в корм для скота в малых дозах для стимулирования роста является общепринятой практикой во многих промышленно развитых странах и, как известно, приводит к повышению уровня резистентности микроорганизмов. Сельскохозяйственные животные могут служить резервуаром антибиотикорезистентных бактерий Salmonella spp., Campylobacter spp., Escherichia coli, Clostridium difficile, Staphylococcus aureus (MRSA), Enterococcus faecium (VRE) [7,8].
В настоящее время учитывая потенциальное развитие антибиотикорезистентности, АМП теряют коммерческую привлекательность, что находит подтверждение в отрицательной динамике появления новых системных антибиотиков (рис. 1).
Сдерживание распространения антибиотикорезистентности
Антибиотики на сегодняшний день являются одной из самых часто применяющихся групп лекарственных средств. По данным Ассоциации международных фармацевтических производителей и ГК Ремедиум в 2014 году системные антибиотики в России занимали 4-е место в структуре амбулаторных и 2-е место в структуре госпитальных продаж готовых лекарственных средств.
В настоящее время во всем мире идет поиск альтернативных подходов к терапии инфекционных заболеваний. Одним из перспективных направлений в борьбе с инфекциями является применение бактериофагов и их компонентов. Бактериофаги природных штаммов и искусственно синтезированные генетически модифицированные фаги с новыми свойствами инфицируют и обезвреживают бактериальные клетки. Фаголизины – это ферменты, которые используются бактериофагами для разрушения клеточной стенки бактерий. Ожидается, что препараты на основе бактериофагов и фаголизинов позволят справиться с устойчивыми к АМП микроорганизмами, однако эти препараты появятся не ранее 2022-2023 гг. Параллельно с этим идет разработка препаратов на основе антибактериальных пептидов и вакцин для лечения инфекций, вызванных C. difficile, S. aureus, P. aeruginosa [9].
В последние годы резко возросла поддержка со стороны органов исполнительной и законодательной власти, а также Министерства здравоохранения Российской Федерации исследований, направленных на сдерживание антибиотикорезистентности. Так, например, Межрегиональная ассоциация по клинической микробиологии и антимикробной химиотерапии (МАКМАХ) и Федеральный научно-методический центр мониторинга резистентности к антимикробным препаратам активно занимаются разработкой страте гических направлений по данной проблеме.
На международный уровень обсуждение данной проблемы вышло на рубеже веков. В 2001 году ВОЗ опубликовала Глобальную стратегию по сдерживанию устойчивости к противомикробным препаратам, а в 2016 году вопрос борьбы с растущей угрозой антибиотикорезистентности был вынесен на повестку дня Генеральной Ассамблеи ООН.
Входящие в ООН государства в совместном заявлении обязались разработать национальные планы мер по противодействию устойчивости микроорганизмов к АМП. Это подразумевает усиление мониторинга лекарственноустойчивых инфекций и контроля за применением АМП в медицине, ветеринарии и сельском хозяйстве, а также укрепление международного сотрудничества и финансирования. Также члены организации взяли на себя обязательства ужесточить законодательное регулирование применения АМП, заниматься поиском рационального их использования (улучшение диагностики инфекций с учетом их чувствительности к препаратам) и широко внедрять меры профилактики инфекционных заболеваний (вакцинация, очистка воды, санитария, должный уровень гигиены в стационарах и на фермах) [10].
Еще одним знаменательным событием 2016 года стало подписание ведущими международными фармацевтическими, диагностическими и биотехнологическими компаниями совместной декларации о принятии всеобъемлющих мер против инфекций, устойчивых к лекарственной терапии. Декларация была оглашена на Всемирном экономическом форуме в г. Давосе и подписана на сегодняшний день почти 100 фармацевтическими компаниями. Представители индустрии призывают правительства всех стран мира выйти за рамки заявлений о намерениях и в сотрудничестве с компаниями принять конкретные меры для поддержки инвестиций в разработку антибиотиков, средств диагностики, вакцин и других продуктов, имеющих жизненно важное значение для предотвращения и лечения лекарственно устойчивых инфекций. Одновременно с этим в Декларации устанавливаются обязательства подписавших сторон по дальнейшим действиям в области проблем лекарственной устойчивости. Компании обязуются уменьшить воздействие производства АМП на окружающую среду; содействовать надлежащему применению новых и существующих АМП, в том числе за счет поддержки рекомендаций по применению АМП; продолжать и расширять научноисследовательские разработки по созданию новых АМП; поддерживать инициативы, направленные на обеспечение доступа к АМП во всех частях света при любых уровнях доходов.
Заключение
Современная медицина немыслима без АМТ. Антибиотики во много раз сократили смертность от инфекционных заболеваний, смягчили тяжесть их течения, уменьшили количество постинфекционных осложнений. Однако, несмотря на появление в арсенале врачей значительного перечня лекарственных препаратов, активных в отношении практически всех патогенных микроорганизмов, существует значительное количество проблем и нерешенных вопросов в области АМТ [1].
В течение последних десятилетий АМТ инфекционных заболеваний существенно осложняется резистентностью возбудителей к АМП. Постоянный рост резистентности к АМП отмечен среди возбудителей как нозокомиальных, так и внебольничных инфекций. Возникновение резистентности и распространение ее среди микроорганизмов является естественным процессом, возникшим в ответ на широкое использование АМП в клинической практике, однако имеет большое социально-экономическое значение и в развитых странах рассматривается как угроза национальной безопасности. Инфекции, вызванные резистентными штаммами микроорганизмов, отличаются более тяжелым течением, чаще требуют госпитализации и увеличивают продолжительность пребывания в стационаре, ухудшают прогноз для пациентов.
Специалисты в области АМТ выделяют несколько уровней резистентности к АМП глобальный, региональный и локальный. Прежде всего, необходимо учитывать глобальные тенденции в развитии резистентности. Примерами микроорганизмов, у которых во всем мире стремительно распространяется резистентность к АМП, являются Staphylococcus spp., Enterococcus spp, Streptococcus pneumoniae, Neisseria gonorrhoeae, Pseudomonas aeruginosa, Acinetobacter spp., бактерии семейства Enterobacteriaceae и другие. При этом следует помнить, что резистентность не является тотальной. Так, например, Streptococcus pyogenes сохраняет чувствительность к пенициллину.
При планировании политики АМТ внебольничных инфекций следует более рационально опираться на локальные (региональные) данные, полученные в конкретной стране или регионе страны. В Российской Федерации существуют значительные территориальные вариации частоты резистентности возбудителей вне больничных инфекций к АМП. Вот почему необходимы постоянный мониторинг резистентности и информирование врачей различных специальностей. Наряду с региональными данными по резистентности к АМП внебольничных возбудителей в каждом ЛПУ необходимо иметь данные по резистентности нозокомиальных возбудителей, особенно в отделениях с интенсивным использованием АМП: ОРИТ, отделения хирургической инфекции, травматологии и ортопедии [4].
Хотя от адекватных назначений врачей и отказа пациентов от самолечения во многом зависит успех борьбы с проблемой антибиотикорезистентности, этих шагов, к сожалению, недостаточно. Очень многие решения должны быть приняты на национальном уровне, например, запрет на безрецептурный отпуск антибиотиков, усиление законодательства в отношении предотвращения производства и продажи фальсифицированных АМП, снижение применения антибактериальных средств в продовольственном животноводстве. Следует также отметить, что современные тенденции развития фармацевтической промышленности таковы, что гарантий появления новых групп АМП нет [11,12].
Без сомнения, эра АМП сыграла существенную роль в жизни современного общества. Однако только трезвый подход как к проблеме лечения АМП и ее принципам, так и к роли антибиотикотерапии в современном обществе способен обеспечить правильное планирование выпуска АМП и прогнозирование их эффективности в будущем.
Резистентность микроорганизмов
Под резистентностью (устойчивостью) понимают способность микроорганизма переносить значительно большие концентрации препарата, чем остальные микроорганизмы данного штамма (вида), или развиваться при таких концентрациях, которые превышают достигаемые в макроорганизме при введении антибиотиков, сульфаниламидов и нитрофуранов в терапевтических дозах.
Резистентные штаммы микроорганизмов возникают при изменении генома бактериальной клетки в результате спонтанных мутаций. Последние не связаны с направленным действием на ДНК бактерии антибактериальных препаратов, которые играют роль лишь селективных агентов. В процессе селекции в результате воздействия химиотерапевтических соединений чувствительные микроорганизмы погибают, а резистентные сохраняются, размножаются и распространяются в окружающей среде. Приобретенная резистентность закрепляется и передается по наследству последующим генерациям бактерий.
Спонтанные мутации происходят с низкой частотой, примерно одна мутация на 10 8 — 10 9 микробных клеток в течение одной клеточной генерации. Однако при огромном числе клеток в бактериальной популяции вероятность возникновения в каком-либо гене мутации, приводящей к превращению чувствительных к данному лекарственному препарату клеток в резистентные, достаточно велика. В отдельных случаях в результате мутации только в одном локусе генома бактериальная клетка после первого контакта с химиотерапевтическим соединением приобретает устойчивость к высоким концентрациям препарата. Типичный пример такой мутационной резистентности — одноступенчатое возникновение устойчивости к стрептомицину вследствие изменения гена str А. В результате мутации нарушается аминокислотная последовательность S12 протеина в 30S субчастице рибосомы. При этом рибосома теряет способность связывать стрептомицин и микробная клетка приобретает устойчивость к антибиотику. Такой тип возникновения резистентности после кратковременного контакта с лекарственным препаратом характерен для макролидов, фузидина, рифампицина и некоторых других антибиотиков. Однако чаще устойчивость возникает вследствие небольших дискретных изменений, обусловленных последовательными мутациями во многих локусах. В этом случае устойчивость у микроорганизмов возрастает постепенно, в процессе длительного контакта с постепенно увеличивающимися концентрациями антибактериального препарата.
По скорости развития лекарственной устойчивости микроорганизмов антимикробные препараты подразделяют на три группы.
Скорость развития лекарственной устойчивости к антимикробным препаратам у микроорганизмов
| Медленно | Постепенно | Быстро |
| Амфотерицин Б Леворин Нистатин Гризеофульвин Фурацилин Фурадонин Фуразолин Фуразолидон Фурагин | Соли бензилпенициллина Феноксиметилпенициллин Бициллины Метициллин Оксациллин Диклоксациллин Ампициллин Карбенициллин Цефалоридин Цефалотин Цефалексин Неомицин Канамицин Гентамицин Сизомицин Апрамицин Тетрациклин Окситетрациклин Хлортетрациклин Доксициклин Левомицетин Полимиксин Сульфаниламиды | Стрептомицин Эритромицин Олеандомицин Линкомицин Фузидин Рифампицин |
Скорость развития и степень выраженности устойчивости связаны с видом и даже штаммом возбудителя. Наиболее быстро и часто резистентность к антибактериальным препаратам возникает у стафилококков, эшерихий, сальмонелл, микоплазм, протея, синегнойной палочки. Среди пастерелл, эризипелотриксов, клостридий, стрептококков группы А, сибиреязвенных и гемофильных палочек резистентные штаммы выделяют сравнительно редко.
Наиболее частой генетической основой резистентности служит наличие в бактериях внехромосомных факторов устойчивости к лекарственным веществам — плазмид и транспозонов.
Плазмиды — это стабильно существующие внехромосомные элементы, представляющие собой ковалентнозамкнутые кольца ДНК, способные автономно реплицироваться в бактериальной клетке. В одной клетке может одновременно находиться несколько плазмид, отвечающих за различные свойства микроорганизма, например резистентность, колициногенность, токсичность.
Бактериальные плазмиды, связанные с переносом маркеров лекарственной устойчивости в процессе конъюгации клеток, получили название R-факторов. Плазмиды резистентности R (конъюгирующие) состоят из двух компонентов — фактора переноса устойчивости RTF, обеспечивающего передачу генетической информации, и r-фактора, отвечающего за резнстентность к антибиотикам. В отдельных случаях r-факторы (неконъюгирующие плазмиды) существуют в бактериальных клетках самостоятельно. Межбактериальный перенос таких r-факторов может осуществляться посредством их мобилизации и коинтеграции с конъюгирующими плазмидами. R-фактор одновременно может содержать 1—10 и более детерминант устойчивости к различным антибактериальным соединениям.
Транспозонные элементы — это фрагменты ДНК, которые свободно перемещаются от одного репликона к другому. Транспозоны определяют различные фенотипические признаки бактериальной клетки, в частности антибиотикорезистентность, и способствуют переносу детерминант устойчивости к антибиотикам между хромосомой, плазмидами и фагами. Они не подчиняются rec-системам клетки, которые ограничивают передачу хромосомных маркеров между неродственными видами. Гены, входящие в состав транспозонов, окружены особыми нуклеотидными последовательностями (IS-элементами), которые и обеспечивают их включение в негомологичный геном. Вхождение детерминант устойчивости в состав транспозонов при постоянно действующем в условиях производства селективном давлении антимикробных препаратов на бактериальные популяции может привести к образованию гибридных плазмид, обусловливающих новые комбинации устойчивости к химиотерапевтическим веществам.
Транспозоны могут перемещаться в пределах одного вида, а также попадать в новые виды и роды микроорганизмов. Установлено, что транспозоны Т1699 и Т1700, присутствующие в неконъюгативных плазмидах S. marcescens, первоначально проникают в конъюгативную плазмиду этого вида, вместе с которой перемещаются в другие роды семейства Enterobacteriaceae.
Способность R-факторов передаваться от клетки к клетке путем конъюгации или трансдукции объясняет быстрое распространение их по микробной популяции. Нередко в результате автономной репликации в одной клетке находятся десятки копий плазмид, что способствует быстрому развитию внехромосомной резистентности.
При трансдукции детерминанты устойчивости к антимикробным препаратам переходят от клетки к клетке с помощью бактериофага, играющего роль переносчика. Фаговая ДНК встраивается в бактериальный геном и при репликации, высвобождаясь из хромосомы или плазмиды, может захватывать генетические элементы, отвечающие за резистентность. Детерминанты устойчивости реплицируются совместно с фаговой ДНК и при лизисе бактерий каждый вновь образовавшийся фаг несет копию маркера резистентности. Последующее заражение такими фагами бактериальных клеток, чувствительных к лекарственному препарату, делает инфицированные микроорганизмы реэистентными к данному препарату. Фаговая трансдукция играет важную роль в распространении лекарственной устойчивости у грамположительных микроорганизмов, особенно стафилококков и стрептококков.
Перенос плазмид при конъюгации осуществляется посредством половых пилей при установлении контакта между двумя клетками. При этом в донорской клетке (R+) происходит репликация плазмидной ДНК, одна цепь которой проникает в реципиентную клетку (R-), где образует новую плазмиду. Если плазмиды интегрированы с хромосомой, то при конъюгации возможен захват генетического материала из хромосомы плазмидной ДНК. При этом могут передаваться детерминанты резистентности, локализованные в хромосоме.
Передача генетической информации между микроорганизмами с помощью трансформации имеет значение только для лабораторных исследований и не принимает участия в распространении лекарственной устойчивости в условиях производства.
В то же время R-плазмидная передача устойчивости к лекарственным веществам является наиболее важным механизмом возникновения резистентности в бактериальной популяции, особенно в семействе энтеробактерий. С эпизоотической точки зрения наиболее опасна передача детерминант устойчивости от одного вида микроорганизмов к другому.
В опытах in vitro установлено, что устойчивость к трем антибиотикам от резистентного штамма сальмонелл может быть передана при конъюгации чувствительным штаммам шигелл и сальмонелл. Е. coli в качестве донора способна передавать детерминанты устойчивости к стрептомицину, левомицетину, канамицину, неомицину и сульфаниламидам сальмонеллам и шигеллам. Отмечена возможность переноса плазмид резистентности от стафилококков к эшерихиям с последующей репликацией плазмиды в реципиентной клетке. Еще одним примером межвидовой передачи лекарственной устойчивости служит перенос R-плазмиды, определяющей устойчивость к гентамицину, амикацину, карбенициллину, цефалоридину, левомицетину от К. pneumoniae к Е. coli и Pr. morganii.
В пищеварительном тракте в огромных количествах содержатся энтеробактерий, что создает условия для трансмиссивной передачи плазмид резистентности. Экспериментально была осуществлена передача R-факторов среди эшерихий, сальмонелл, шигелл в желудочно-кишечном тракте лабораторных животных, цыплят, поросят, овец и телят. Перенос R-факторов в пищеварительном тракте идет менее интенсивно, чем в опытах in vitro. Это связано с тем, что желчные кислоты и среда кишечника неблагоприятно влияют на образование пар между донорской и реципиентными клетками. Кроме того, клетки Bacteroides за счет выделения продуктов жизнедеятельности ингибируют процесс конъюгации у Е. coli.
К наиболее существенным факторам R-плазмид относят их способность к мобилизации и коинтеграции с другими плазмидами, что в условиях селекции антимикробными препаратами создает условия, благоприятные для отбора полиплазмидных штаммов, содержащих наряду с R-плазмидами плазмиды вирулентности и патогенности. Описаны случаи совместной передачи двух плазмид — R и Ent (плазмида, детерминирующая продукцию энтеротоксина у кишечной палочки) при конъюгации с последующей локализацией генов продукции энтеротоксина и резистентности на одной плазмиде.
Циркуляция плазмид от животных к животным, от животных к человеку и от человека к животным способствует быстрому распространению лекарственной реэистентности во всем мире.
Плазмиды резистентности распространяются в результате контактного перезаражения лекарственно-устойчивыми микроорганизмами больших групп животных, сконцентрированных на ограниченных площадях животноводческих помещений. Отмечена передача JR-факторов от животных к человеку. Так, у персонала, работающего в животноводстве, количество резистентной микрофлоры в несколько раз выше, чем у людей, не контактирующих с животными. Высокая обсемененность туш забитых животных и птицы лекарственно-устойчивыми микроорганизмами способствует распространению Д-факторов среди работников мясокомбинатов, а также лиц, занятых переработкой мясопродуктов и употребляющих в пищу мясо, не подвергнутое необходимой термической обработке.
Большинство штаммов Е. coli — комменсалы кишечника, которые легко перемещаются как внутри популяции животных и человека, так и между ними, о чем свидетельствует сходный набор плазмид резистентности. Основная масса этих штаммов устойчива к большинству антибактериальных соединений. Апатогенные эшерихии служат постоянным резервуаром плазмид резистентности, в котором попадающий в организм возбудитель, сам по себе не несущий R-фактор, при конъюгации может приобрести детерминанты устойчивости к лекарственным препаратам. Установлено, что при вспышке сальмонеллеза в Великобритании детерминанта устойчивости к левомицетину была получена от непатогенной кишечной палочки.
Передача детерминант устойчивости в организме животных — не единственный фактор распространения лекарственно-устойчивых штаммов микроорганизмов. Не менее важную роль играет селекция устойчивых клеток, обусловленная применением антимикробных веществ или более высокой патогенетической активностью таких микроорганизмов. При селекции под влиянием антибиотиков резистентные клетки выживают за счет чувствительных и, размножаясь, становятся доминирующей частью микрофлоры. Увеличение количества лекарственно-устойчивых клеток приводит к учащению передачи детерминант устойчивости, и, как следствие этого, происходит их дальнейшее распространение во внешней среде.
В некоторых случаях селективное преимущество резистентных штаммов энтеробактерий связано с их лучшей способностью по сравнению с чувствительными микроорганизмами колонизировать слизистую оболочку кишечника. Это вызвано тем, что антимикробные препараты снижают адгезивность чувствительной микрофлоры и не влияют на адгезивность устойчивых бактерий, что позволяет им быстро расселяться по всему кишечнику. Другим механизмом, объясняющим селективное преимущество резистентной микрофлоры, служит наличие у отдельных штаммов Е. coli pKMR-плазмид, контролирующих одновременно лекарственную резистентиость и адгезивность.
Использование антимикробных средств в заниженных дозах, увеличение интервалов между введением препарата приводят к созданию в организме субтерапевтических концентраций антибактериальных соединений и, как следствие этого, к селекции резистентных форм микроорганизмов.
Применение антибиотиков, предназначенных для этиотропной терапии, с целью повышения продуктивности животных привело к селекции микрофлоры, резистентной к лечебным препаратам. В результате широкого употребления в животноводстве тетрациклиновых антибиотиков в качестве кормовой добавки большинство штаммов сальмонелл и эшерихии приобрело резистентность к препаратам этой группы. В странах, где в последние годы было запрещено использование лечебных антибиотиков для стимуляции роста животных, наблюдается снижение частоты выделения резистентных штаммов энтеробактерий как у животных, так и у людей. В Голландии после запрещения применения тетрациклина в качестве кормовой добавки частота выделения от свиней резистентных штаммов сальмонелл снизилась с 90% в 1974 г. до 34% в 1980 г.
Установлена зависимость между интенсивностью проявления селективного действия антибактериальных препаратов и широтой распространения плазмид резистентности. Повышение количества применяемых антимикробных средств прямо пропорционально увеличению числа антибиотико-устойчивых штаммов микроорганизмов.
Устойчивость микроорганизмов к антимикробным препаратам в случае как плазмидной, так и хромосомной локализации детерминант резистентности может быть обусловлена несколькими механизмами.
Наиболее часто лекарственная устойчивость связана со способностью микроорганизмов вырабатывать ферменты, инактивирующие антибактериальные препараты. Характерный пример устойчивости этого типа — способность бета-лактамаз (пенициллиназ) бактерий гидролиэировать бета-лактамные кольца пенициллинов и цефалоспоринов. В результате разрыва бета-лактамной связи антибиотики теряют свою специфическую активность в отношении микроорганизмов. Бета-лактамазы бывают как широкого спектра действия, расщепляющие пенициллины и цефалоспорины, так и узкого — активные в отношении только одной из групп этих антибиотиков. Пенициллиназы грамположительных микроорганизмов служат индуцируемыми ферментами, поэтому их синтез начинается только в момент контакта бактерии с бета-лактамами. При этом пенициллиназа высвобождается из бактериальных клеток и инактивирует антибиотик в межклеточном пространстве. В то же время бета-лактамазы грамотрицательных бактерий детоксицируют антибиотик в периплазматическом пространстве. Таким образом они инактивируют проникшие через наружную мембрану бета-лактамы еще до того, как антибиотик связался с ферментами, участвующими в синтезе клеточной стенки. Пенициллиназы резистентных грамотрицательных микроорганизмов синтезируются конститутивно и постоянно находятся в периплазматическом пространстве.
Для аминогликозидных антибиотиков также характерна конститутивная ферментная инактивация в периплазматическом пространстве. При этом начальная скорость инактивации должна превышать скорость поступления аминогликозида в клетку. Только в этом случае антибиотик, модифицированный ферментами, нарушает систему транспорта полиаминов, отвечающую за поступление новых молекул аминогликозида в клетку. Модифицированный антибиотик не подавляет синтез белка у микроорганизмов, так как не может взаимодействовать с активным центром рибосом, что сопровождается резистентностью к препарату.
Таким образом, устойчивость достигается при инактивации только проникшего в клетку аминогликоэида и не зависит от концентрации препарата в межклеточном пространстве. В случае высокой скорости поступления аминогликозида в микробную клетку антибиотик успевает нарушить процесс трансляции раньше, чем инактивируется, и подавить систему переноса аминогликозида в клетку.
Детерминанты резистентности, определяющие ферментативную инактивацию аминогликозидных антибиотиков, обычно имеют плазмидное происхождение. Модификация аминогликозидов у резистентной микрофлоры происходит под действием разнообразных ферментов. Некоторые из них обеспечивают перекрестную резистентность почти ко всей этой группе антибиотиков, другие — только к отдельным препаратам. Ферментативная инактивация аминогликозидных антибиотиков идет путем фосфорилирования и аденилирования гидроксильных групп, а также ацетилирования аминогрупп.
Резистентные микроорганизмы, кроме пенициллияов и аминогликозидов, ферментативно инактивируют левомицетин, сульфаниламиды и триметоприм.
Другой важный механизм, обусловливающий антибиотико-резистентность, заключается в нарушении проницаемости микробных клеток для антибиотика. Так, изменение у стафилококков и синегнойной палочки липидного состава клеточной стенки нарушает ее проницаемость соответственно для фузидиевой кислоты и левомицетина. Появление неспецифических белков в наружной мембране Е. coli снижает ее чувствительность к антибиотикам. Резистентность к полимиксину у синегнойной палочки связана с изменением структуры наружной мембраны, что предотвращает проникновение антибиотика в микробную клетку.
. Резистентность к тетрациклинам чаще всего носит индуктивный характер. При контакте с антибиотиком у микроорганизмов начинается синтез специфических белков, которые в основном локализуются на наружной мембране и ограничивают поступление тетрациклина в клетку. По другим данным, индуцированные белки нарушают взаимодействие антибиотика с 30S-субчастицей рибосом или, изменяя проницаемость клеточной мембраны, обеспечивают свободный выход тетрациклина из бактериальной клетки.
Модификация чувствительных к антибиотику участков также приводит к развитию резистентности у микроорганизмов. Изменение белка S12, входящего в состав 30S-субчастицы рибосомы, или белков L4 и L12, входящих в состав 50S-субчастицы, уменьшает связывание соответственно аминогликозидов или макролидов с рибосомами, что предотвращает ингибирующее действие антибиотиков на синтез белка. Этот механизм устойчивости обычно обусловлен хромосомными мутациями.
Возможный механизм развития резистентности — это синтез соединений, не инактивирующихся под действием антибактериальных веществ. Так, устойчивость к сульфаниламидам и триметоприму связана с выработкой нечувствительных к действию этих препаратов дигидроптероатсинтетазы и дигидрофолатредуктазы.
Широкое распространение лекарственно-устойчивых микроорганизмов требует разработки комплекса мероприятий, ограничивающих циркуляцию резистентных бактерий среди сельскохозяйственных животных. Меры по ограничению распространения лекарственно-устойчивых микроорганизмов должны быть направлены, во-первых, на предупреждение формирования резистентных популяций и, во-вторых, на подавление уже сформировавшихся популяций.
Поскольку ферменты, инактивирующие аминогликозиды, в основном относятся к трансферазам, химическая трансформация или модификация аминогликозидов основана или на удалении из молекулы антибиотика отдельных функциональных групп, подвергающихся замещению остатками фосфорной, адениловой или уксусной кислот, или на экранировании этих групп. Таким образом было получено производное канамицина — амикацин, в котором NH3-rpyппa в положении 1 замещена боковой цепью гидроксиаминомасляной кислоты. Кроме этого, пространственная конфигурация молекулы амикацина по сравнению с исходным антибиотиком изменена таким образом, что чувствительные к фосфорилированию функциональные группы не доступны для соответствующих ферментов. В результате этих изменений амикацин устойчив к действию всех энзимов, модифицирующих аминогликозиды, за исключением канамицин-N-ацетилтрансферазы и специфической для амикацина фосфотрансферазы.
Полусинтетическим 1-производным другого аминогликозидного антибиотика — сизомицина со сниженной чувствительностью к аденнлирующим и ацетилирующим ферментам является нетилмицин.
Практически любая молекула антибиотика может инактивироваться в микробной клетке за счет определенного механизма резистентности, поэтому спустя некоторое время после начала использования нового препарата отмечают распространение детерминант резистентности к этому соединению в плазмидах и транспозонах. В связи с этим эффективность каждого антибиотика начинает уменьшаться, что обусловливает необходимость синтеза все новых антимикробных препаратов.
Перспективными методами в борьбе с лекарственно-устойчивыми микроорганизмами служит использование соединений, подавляющих определенные механизмы резистентности в бактериальной клетке. Наибольшие успехи в этом направлении достигнуты в результате применения неконкурентных ингибиторов бета-лактамаз, первый представитель — клавулановая кислота. Она обладает слабой антибактериальной активностью, и как антибактериальный препарат ее не используют. Основное ее свойство — способность необратимо ингибировать пенициллиназы грамположительных и грамотрицательных микроорганизмов. Эта кислота проявляет синергизм в отношении бета-лактамазообразующих возбудителей в комбинации с ампициллином, амоксициллином, тикарциллином, цефалексином и многими другими бета-лактамными антибиотиками. Уже разработаны и применяются в клинической практике комплексные препараты на основе амоксициллина и клавулановой кислоты.
Производные пенициллановой кислоты также можно практически использовать в качестве ингибиторов бета-лактамаз. К другим эффективным ингибиторам пенициллиназ относят оливановые кислоты и тиенамицины, которые, помимо защиты антибиотика от действия ферментов, обладают широким антимикробным спектром действия.
Протамин, экмолин и трифенилметановые красители подавляют хлорамфениколацетилтрансферазу у левомицетин-резистентных микроорганизмов. Но из-за низкой стабильности, токсичности, штаммоспецифичности эти соединения не нашли практического применения в медицине и ветеринарии в качестве ингибитора хлорамфениколацетилтрансферазы.
Для остальных групп антибиотиков, кроме беталактамов и левомицетина, еще не найдены специфические ингибиторы механизмов резистентности.
Перспективное направление в борьбе с резистентностью бактерий — использование фосфогликолипидных антибиотиков. Препараты этой группы взаимодействуют с половыми пилями микроорганизмов, в связи с чем в первую очередь подавляют R+-клетки, несущие детерминанты резистентности. Среди фосфогликолипидов широко используют в животноводстве и птицеводстве флавомицин и макарбомицин, которые в желудочно-кишечном тракте сельскохозяйственных животных значительно снижают количество антибиотико-резистентной микрофлоры.
Другим подходом к решению проблемы воздействия на лекарственно-устойчивую популяцию микроорганизмов является использование соединений, обеспечивающих элиминацию плазмид из резистентных бактерий и действующих на детерминанты лекарственной устойчивости. Одним из способов, ведущих к элиминации плазмид из микробной клетки, стало применение ДНК-тропных веществ. Акрифлавин и хинакрин вызывают элиминацию R-факторов из сальмонелл, шигелл и эшерихий. Способностью элиминировать плазмиды резистентности к лекарственным препаратам обладают рифампицин, фурагин, антигистаминные препараты, бромистый этидий, акридиновые красители и ряд других веществ. ДНК-тропные соединения действуют в первую очередь на R+-клетки, приводя к накоплению в микробной популяции R-клеток. Механизм этого процесса связан с тем, что ДНК-тропные вещества взаимодействуют с плазмидной ДНК и тем самым нарушают ее репликацию, необходимую при переносе плазмид из клетки в клетку.
Помимо непосредственного влияния на R-факторы, ДНК-тропные соединения за счет снижения мутаций замедляют развитие резистентности микроорганизмов к антимикробным препаратам. Так, акрихин и акрифлавин подавляют развитие антибиотико-устойчивых штаммов бактерий к пенициллину, ампициллину, неомицину, рифампицину и стрептомицину.
Еще один путь предупреждения распространения плазмид реэистентности — это использование соединений, эффективно подавляющих процессы переноса детерминанты устойчивости при конъюгации бактерий. Наиболее интенсивно на этот процесс воздействуют рифампицин, бромистый этидий, кофеин, протамин, неомицин и нитрофураны. Некоторые из этих соединений обладают относительно низкой токсичностью и могут оказаться перспективными при использовании в ветеринарной практике. Так, введение цыплятам протамина и фуразолидона подавляет передачу плазмид резистентности у эшерихий.
Механизм действия некоторых препаратов этой группы обусловлен снижением компетентности R+-клеток без изменения реципиентной способности R—клеток, что связано с подавлением активности ферментов, необходимых для нормального осуществления переноса плазмид или их репликации.
Нарушение трансдукции химиотерапевтическими веществами, подавляющими перенос фагами детерминант устойчивости к лекарственным веществам, может ограничивать распространение устойчивых штаммов. Бромистый этидий и рифампицин подавляют частоту передачи R-фактора у эшерихий в 100 раз, что связано с подавлением адсорбции бактериофага на поверхности реципиентной клетки. Роккал и хлоргексидин предупреждают появление и накопление канамицин-резистентных микроорганизмов за счет антифагового действия в отношении трансдуцирующих бактериофагов.
Некоторые поверхностно-активные вещества, такие, как диметилсульфоксид, додецилсульфат натрия, динатриевая соль ЭДТА, действуют на мембрану микробной клетки и ведут к лизису половых пилей, обеспечивающих перенос плазмид. В связи с этим в резистентной популяции микроорганизмов в первую очередь снижается количество имеющих половые пили R+-клеток, ответственных за межбактериальную передачу плазмид в процессе конъюгации.
Наиболее перспективный и реальный метод, ограничивающий появление и накопление устойчивых бактерий в организме животных — это повышение эффективности химиотерапии за счет использования комбинаций различных антимикробных препаратов. Если бы развитие лекарственной устойчивости основывалось исключительно на принципе селекции хромосомных мутантов в организме, то комбинированным введением препаратов ее можно было бы полностью предотвратить. Так, при обычной частоте хромосомных мутаций порядка 1 на 10 8 клеточных делений вероятность появления мутантов, устойчивых к двум препаратам, составит 1 на 10 16 клеточных делений, к трем препаратам — 1 на 10 24 и т. д. В организме животного количество микроорганизмов составляет гораздо меньшую величину, и поэтому мутанты, резистентные к двум-трем препаратам, никогда не должны возникать. К сожалению, частота мутаций в некоторых случаях может быть выше, а распространение устойчивости происходит при участии плазмид. Тем не менее комбинированная химиотерапия служит важным сдерживающим фактором в борьбе с лекарственной устойчивостью. Так, быстрого приобретения устойчивости золотистого стафилококка к новобиоцину удается избежать благодаря его применению с тетрациклином. Использование изониазида со стрептомицином предупреждает развитие резистентных к антибиотику штаммов микобактерий туберкулеза. Метициллин и бензилпенициллин предотвращают быстрое формирование устойчивости к фузидину у стафилококков.
Помимо предупреждения развития резистентности, рационально подобранные сочетания антибактериальных препаратов могут воздействовать на устойчивые штаммы микроорганизмов с помощью подавления ферментов, инактивирующих один из компонентов смеси. Так, одна из возможностей защиты бета-лактамазолабильных пенициллинов от деградации пенициллиназой заключается в их использовании в сочетании с бета-лактамазостабильными пенициллинами. При этом последние блокируют активные центры фермента и тем самым предупреждают инактивацию пенициллиназолабильных антибиотиков. Этот механизм воздействия на резистентную клетку был положен в основу комплексного препарата ампиокс, состоящего из ампициллина и оксациллина, а также при использовании в клинической практике сочетания диклоксациллина с ампициллином,
При комбинировании левомицетина с ампициллином и окситетрациклина с пенициллином удается воздействовать на беталактамазопродуцирующие штаммы Haemophilus influenzae и стафилококка за счет ингибирования бактериостатическими антибиотиками процесса бета-лактамазообразования в микробной клетке, в связи с чем резистентные микроорганизмы становятся чувствительными к бета-лактамазолабильным антибиотикам.
Аналогичный эффект наблюдают при сочетании полимиксина с налидиксовой кислотой в отношении полимиксин-резистентных штаммов Serratia. При этом кислота блокирует синтез ферментов, инактивярующих антибиотик, и тем самым восстанавливает чувствительность микроорганизма к полимиксину.
Таким образом, высокоэффективным способом борьбы с резистентностью микроорганизмов является использование соединений, активных в отношении ферментов, ингибирующих антимикробные вещества. К сожалению, ассортимент таких веществ практически ограничен только противо-бета-лактамазными препаратами и не может полностью решить проблему лекарственной резистентности. Использование специфических ингибиторов репликации плазмидной ДНК и препаратов, влияющих на процессы конъюгации и трансдукции, также не нашло широкого применения, во-первых, из-за отсутствия 100 %-ного эффекта в отношении всех видов устойчивых микроорганизмов и, во-вторых, из-за высокой токсичности многих из этих веществ для макроорганизма. В связи с этим для предотвращения развития лекарственной резистентности и воздействия на устойчивую микрофлору наиболее широко используют комбинированную химиотерапию.