почему повышается мочевина в крови у женщин после 50 лет и что нужно делать
Почему повышается мочевина в крови у женщин после 50 лет и что нужно делать
Научно-диагностический центр лабораторных технологий

Личный кабинет клиента
Мочевина (Urea)
Мочевина – основной продукт распада белков. Она является той химической формой, в которой ненужный организму азот удаляется с мочой. Накопление мочевины и других азотсодержащих соединений в крови вследствие почечной недостаточности приводит к уремии. Она продуцируется в печени, переносится кровью в почки, там фильтруется через сосудистый клубочек, а затем выделяется. Результат теста на мочевину является показателем клубочковой продукции и экскреции мочи. Количество выделяемой мочевины находится в прямой зависимости от уровня потребляемого человеком белка, оно повышается при лихорадочных состояниях, при осложнениях диабета и при усиленной гормональной функции надпочечников. Повышенный уровень мочевины – маркер снижения клубочковой фильтрации. Мочевина – один из основных метаболитов крови, организм никак её не использует, а только избавляется от неё. Так как этот процесс выделения непрерывный, определенное количество мочевины всегда находится в крови. Уровень мочевины следует трактовать неотрывно от показателей креатинина. Термин «уремия» применяется, когда концентрация мочевины в крови поднимается выше 20 ммоль/л. Образование мочевины у здорового человека зависит от характера питания: преобладание в диете белковых продуктов (мясо, рыба, яйца, сыр, творог) концентрация мочевины может повышаться до верхних границ нормы, а при растительной диете – снижаться. При патологии печени вследствие нарушения её синтетической способности уровень мочевины в крови может снижаться. У детей раннего возраста, при беременности в связи с повышенным синтезом белка уровень мочевины несколько снижен по сравнению с нормой для взрослых. С возрастом уровень мочевины повышается.
Подготовка к исследованию
Не принимать пищу в течение 12 часов до исследования.
Исключить физическое и эмоциональное перенапряжение.
Показания к исследованию
Исследование функции почек и печени.
Интерпретация
Референсные значения (норма мочевины в крови):
Почему повышается мочевина в крови у женщин после 50 лет и что нужно делать
Мочевина – основной продукт распада белков. Она является той химической формой, в которой ненужный организму азот удаляется с мочой.
Накопление мочевины и других азотсодержащих соединений в крови вследствие почечной недостаточности приводит к уремии.
Диамид угольной кислоты, карбамид, мочевина в крови.
Синонимы английские
Urea nitrogen, Urea, Blood Urea Nitrogen (BUN), Urea, Plasma Urea.
УФ кинетический тест.
Ммоль/л (миллимоль на литр).
Какой биоматериал можно использовать для исследования?
Венозную, капиллярную кровь.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Мочевина – один из конечных продуктов белкового метаболизма, содержащий азот. Она продуцируется в печени, переносится кровью в почки, там фильтруется через сосудистый клубочек, а затем выделяется. Результат теста на мочевину в крови является показателем клубочковой продукции и экскреции мочи.
Метаболизированный азот находится в организме в виде аммиака, производимого из остатков распада и переработки белков. Аммиак в печени, соединяясь с углекислым газом, образует мочевину. Быстрое разрушение белков и повреждение почек стремительно поднимают уровень мочевины в крови (так же как и практически любая массивная гибель клеток).
Количество выделяемой мочевины находится в прямой зависимости от уровня потребляемого человеком белка, причинами повышения мочевины в крови являются лихорадочные состояния, осложнения диабета, усиленная гормональная функция надпочечников. Повышенный уровень мочевины – маркер снижения клубочковой фильтрации.
Мочевина – один из основных метаболитов крови, организм никак ее не использует, а только избавляется от нее. Так как этот процесс выделения непрерывный, определенное количество мочевины в норме всегда находится в крови.
Уровень мочевины следует трактовать неотрывно от показателей креатинина. Термин «уремия» применяется, когда уровень мочевины в крови поднимается выше 20 ммоль/л.
Азотемия, показателем которой также служит повышение концентрации мочевины, чаще всего является следствием неадекватной экскреции из-за заболеваний почек.
Уровень мочевины в крови снижается при многих заболеваниях печени. Это происходит из-за неспособности поврежденных клеток печени синтезировать мочевину, что, в свою очередь, ведет к повышению концентрации аммиака в крови и развитию печеночной энцефалопатии.
Почечная недостаточность проявляется при утрате клубочка способности фильтровать через себя метаболиты крови. Это может произойти внезапно (острая почечная недостаточность) в ответ на заболевание, введение лекарств, ядов, повреждение. Иногда это следствие хронических заболеваний почек (пиелонефрита, гломерулонефрита, амилоидоза, опухоли почек и др.) и других органов (диабета, гипертонической болезни и др.).
Анализ на мочевину обычно назначают в комбинации с тестом на уровень креатинина в крови.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Возраст, пол
Референсные значения
Причины повышения уровня мочевины в крови:
Причины понижения уровня мочевины в крови:
Что может влиять на результат?
Кто назначает исследование?
Терапевт, уролог, нефролог, инфекционист, эндокринолог, гастроэнтеролог, гинеколог, кардиолог.
Повышенная мочевина в крови
Повышение в крови мочевины обнаруживают при биохимическом анализе крови. Если других жалоб нет, стоит задуматься о питании. Такие показатели могут быть при употреблении большого количества белковой пищи, например, мяса, рыба, курицы и др. Скорректировать содержание мочевины в крови помогает диета №6. В ней упор делается на продукты, в составе которых сложные углеводы. При этом количество белковой пищи снижается.
Физиологические причины повышения мочевины в крови могут быть связаны со злоупотреблением алкоголем или физическим перенапряжением. Также подобный эффект возникает в качестве побочного действия некоторых лекарственных препаратов.
Из патологических причин выделяют болезни сердечно-сосудистой системы, эндокринные поражения, лишний вес, патологии почек и заболевания крови.
Само по себе повышение концентрации мочевины в крови не информативно. Нужны дополнительные обследования, включая определение уровня мочевой кислоты и креатинина в крови. Если превышение нормы обнаруживается и по этим показателям, нужно посетить нефролога или уролога для консультации.
Повышенная мочевина в крови: почему возникает и как лечить
Иногда в результатах анализов пациенты видят то, что их беспокоит, и ждать приема у врача – мука. Хотя говорить о точном диагнозе по одному исследованию нельзя, можно примерно описать, при каких заболеваниях возможно получение подобных результатов. Например, повышенная мочевина в крови появляется как при физиологических процессах, так и при некоторых патологиях.
Причины состояния
Если обнаружено повышение мочевины в крови, причины могут быть двух типов: физиологические и патологические. В зависимости от того, к какой группе относится предрасполагающий фактор, разрабатывается план по нормализации состояния.
Записаться на прием
к врачу
можно по телефону
или с помощью системы онлайн-записи на сайте
Физиологические причины:
Они не требуют медикаментозного лечения, рекомендуется коррекция поведения и образа жизни.
Патологические причины:
Если физиологические причины исключены, нужно проводить обследование и выяснять, какой патологией вызвано состояние.
Возможные заболевания
Повышение в крови уровня мочевины возникает при поражении различных органов и систем.
Заболевания, для которых характерен симптом:
При обширных ожогах, а также при болезни Дауна также может наблюдаться повышение концентрации мочевины. Установить диагноз поможет комплексное обследование, план которого зависит от жалоб пациента.
В каком случае обращаться к врачу
Есть типичные симптомы, сочетание которых с повышенным содержанием мочевины говорит о возможном наличии патологии. В этом случае нужно обратиться к врачу как можно скорее.
Настораживающие симптомы:
Если ничего не беспокоит, кроме повышенного содержания мочевины, визит к врачу можно отложить на 2-3 недели. На это время стоит пересмотреть свои привычки и образ жизни. При отсутствии положительной динамики в анализах, обратиться к специалисту все же стоит. Начать можно с терапевта.
Диагностика
План обследования зависит от жалоб пациента. Если беспокоят проявления со стороны сердечно-сосудистой системы, потребуется консультация кардиолога. Он может назначить ЭКГ, ЭхоКГ, холтер.
При наличии жалоб со стороны выделительной системы, обследование проводит нефролог. Дополнительно назначается определение уровня креатинина и мочевой кислоты в крови, а также УЗИ почек.
Лечение
Если только повышена мочевина в крови, лечение не требуется. Но скорректировать привычки все же рекомендуется.
Образ жизни при повышенной мочевине:
Если повышение концентрации мочевины вызвано приемом лекарственных средств, нужно дождаться окончания курса, подождать 2 недели и измерить уровень снова. При наличии отклонений нужно обратиться к врачу.
При повышении уровня мочевины в связи с патологическим состоянием, необходимо провести лечение основного заболевания. Нормализация показателей крови происходит при достижении стойкой ремиссии.
Помните, что поставить точный диагноз, определить причины и характер заболевания, назначить эффективное лечение может только квалифицированный врач. Записаться на прием к нашим специалистам или вызвать врача на дом Вы можете по телефону
Будьте здоровыми и счастливыми!
Урологи клиники «Гармония»
Акутин
Роман Михайлович
Записаться
Уролог
Валенков
Николай Викторович
Записаться
Уролог
Демьяненко
Ярослав Игоревич
Записаться
Уролог
Крупянко
Игорь Дмитриевич
Записаться
Уролог
Светлов
Владислав Викторович
Записаться
Хирург, Уролог, кандидат медицинских наук, врач высшей категории
Аденома простаты у мужчин: лечение, симптомы, причины возникновения, удаление
Аденома простаты – это нераковая опухоль, развитие которой сопровождается симптомами нарушения мочеиспускания. Согласно статистике, она является частой причиной обращения пациентов к урологу. В нашей клинике мы предлагаем полный комплекс диагностики и лечения этой болезни.
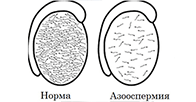
Азооспермия у мужчин: виды, причины, лечение
Часто к мужскому бесплодию приводит азооспермия – патологическое состояние, при котором в сперме не обнаруживают сперматозоидов. Диагностируют его при проведении спермограммы. Наша клиника предлагает полноценное обследование этого состояния и дальнейшее ведение пациента.
Варикоцеле у мужчин: причины, симптомы, диагностика, лечение в Твери
Варикоцеле – это заболевание, при котором расширяются вены семенного канатика. Преимущественно его диагностируют у пациентов молодого возраста (15-30 лет), чаще у спортсменов и работников, которые имеют значительные физические нагрузки. Наша клиника предлагает диагностику варикоцеле, лечение этой патологии.
© 2012-2020 ООО медицинский центр
«Клиника мужского и женского здоровья»
Лицензия №ЛО-69-01-001044 от 23.05.2013
г. Тверь, ул. Желябова, 75 Смотреть на карте
Осложнения на почки после ковида: кто в группе риска
Коронавирусная инфекция опасна не только воспалением и поражением легочной ткани. Осложнения заболевания, перенесенного в любой форме, касаются сердца, головного мозга и почек. Мочевыделительная система страдает в 59% всех случаев осложнений. Исследования в провинциях Сычуань и Хубэй подтвердили наличие белка в моче у пациентов, почти у каждого второго обнаруживается и кровь.
Симптомы осложнений на почки после коронавируса
При тяжелом течении вирусного заболевания симптомы почечных осложнений появляются практически сразу. Если ковид уже перенесен, первые признаки осложнений напоминают простуду: озноб, дискомфорт, головная боль.
Выраженная клиническая картина:
Болевой синдром в поясничной области, ноющая и простреливающая боль, которая временами усиливается.
При первых симптомах осложнений на почки при коронавирусе купировать состояние легче. Если вы недавно перенесли заболевание, тщательно отслеживайте свое состояние и обращайтесь к врачу сразу, как только появится дискомфорт.
Какие осложнения на почки дает коронавирус
Заболевания почек после ковида связаны с угнетением работы клеток – в моче пациентов обнаруживаются следы ДНК вируса, что говорит о его присутствии и в мочевыделительной системе. Чаще всего состояние выражается в почечной недостаточности – острой, переходящей в хроническую.
Острое повреждение почек – один из факторов смертности от ковида при тяжелом течении болезни, потому скрининг необходим как можно быстрее. У некоторых больных вялотекущие и скрытые нарушения в мочевыделительной системе проявляются тут же при заболевании коронавирусом.
Как диагностируется постковидный синдром
Осложнения на почки после коронавируса диагностируются инструментальными и лабораторными методами:
Патология чаще беспокоит пациентов с повышенной свертываемостью крови, потому и коагулограмма входит в перечень диагностических мероприятий.
Факторы риска
Риск получить осложнения на почки после ковида выше у пациентов с такими состояниями:
Таким пациентам особенно важно вовремя проходить диагностику, даже когда признаков отклонений от нормы нет.
Как лечить постковидные осложнения
Если состояние допущено до хронического течения, его можно облегчить под руководством опытного уролога, нефролога. Чем дольше откладывается диагностика, тем больше степень поражения почечной ткани.
Самолечение всевозможными чаями и препаратами только ухудшит состояние – назначать схему лечения может только врач после получения результатов обследования.
Специалисты Государственного центра урологии в Москве занимаются лечением осложнений коронавируса на почки. Обратитесь к опытным врачам высшей категории для своевременной диагностики и терапии – все анализы и прием в одном учреждении. Возможен срочный прием в день обращения!
Диагностика и лечение подагрического артрита
Подагра — хроническое прогрессирующее заболевание, связанное с нарушением пуринового обмена, которое характеризуется повышением мочевой кислоты в крови и отложением в тканях опорно-двигательного аппарата и внутренних органах натриевой соли мочевой кислот
Подагра — хроническое прогрессирующее заболевание, связанное с нарушением пуринового обмена, которое характеризуется повышением мочевой кислоты в крови и отложением в тканях опорно-двигательного аппарата и внутренних органах натриевой соли мочевой кислоты (уратов) с развитием рецидивирующего острого артрита и образованием подагрических узелков (тофусов).
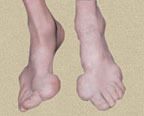
Подагра относится к «старым» болезням и известна со времен глубокой древности. Термин «подагра» происходит от греческих слов pus, что означает стопа, и agra — захват. Таким образом, уже в названии заболевания подчеркивается одно из кардинальных проявлений подагрического артрита. Подагра рассматривается не только как недуг, при котором патологический процесс локализуется в опорно-двигательном аппарате, но и как системное заболевание, характеризующееся поражением жизненно важных органов, и прежде всего почек. Распространенность подагры в различных регионах варьирует в широких пределах и во многом связана с особенностями питания населения, составляя в среднем 0,1%. В США этот показатель равен 0,84% (возможно, эта цифра завышена).
Подагрой болеют преимущественно мужчины (отношение мужчины/женщины составляет 9:1). У мужчин и в норме наблюдается более высокий уровень мочевой кислоты. У женщин репродуктивного возраста повышенное содержание эстрогенов способствует увеличению почечного клиренса уратов. В постменопаузальном периоде уровень мочевой кислоты у них такой же, как и у мужчин соответствующего возраста. Поэтому, если пик заболеваемости у мужчин падает на возраст 35–50 лет, то у женщин — на 55–70 лет. Однако подагра может развиваться и в более молодом возрасте и отмечается даже у детей.
Как известно, мочевая кислота является конечным продуктом расщепления пуринов и выделяется из организма почками. У здоровых лиц за 24 ч выделяется с мочой 400–600 мг мочевой кислоты. Для понимания патогенеза подагры следует остановиться на клиренсе мочевой кислоты. Он характеризует объем крови, способный очиститься в почках от мочевой кислоты за 1 мин. В норме этот показатель равен 9 мл/мин. Источником образования мочевой кислоты в организме являются пуриновые соединения, которые поступают с пищей или образуются в организме в процессе обмена нуклеотидов. В плазме крови мочевая кислота находится в виде свободного урата натрия. В норме верхняя граница этого показателя для мужчин составляет 0,42 ммоль/л (7 мг%) и для женщин — 0,36 ммоль/л (6 мг%). Содержание мочевой кислоты выше этих цифр расценивается как гиперурикемия и рассматривается в качестве фактора высокого риска развития подагры. Так, по данным Фремингемского исследования, развитие подагрического артрита наблюдается у 17% мужчин и женщин с урикемией 7,0–7,9 мг%, у 25% — с 8–8,9 мг% и у 90% — при уровне мочевой кислоты выше 9,0 мг%.
При наличии стойкого повышения мочевой кислоты в сыворотке крови выше для данного индивидуума уровня она начинает откладываться в тканях в виде свободного урата натрия, который в мочевых путях переходит в мочевую кислоту.
Выделяются следующие клинические варианты подагры:
Гиперурикемия может длительное время протекать без каких-либо субъективных и объективных симптомов и лишь случайно диагностироваться при обследовании больного. Однако она не столь безобидна, как это может показаться на первый взгляд, и нередко ассоциируется с нарушениями жирового и углеводного обмена, а также, что еще более серьезно, приводит к уратной нефропатии. Следует отметить условность дефиниции «асимтоматическая подагра». Для ее выявления необходимо повторно исследовать уровень мочевой кислоты, особенно у «подагрической личности», т. е. у мужчин молодого возраста с пристрастием к алкоголю, ожирением и артериальной гипертонией. В некоторых случаях период асимптоматической (химической) гиперурикемии длится несколько лет и только после этого происходит клиническая презентация подагры. Следует иметь в виду, что гиперурикемии обычно предшествует гиперурикозурия. Поэтому у больных с мочекислым диатезом нужно повторно исследовать уровень мочевой кислоты не только в крови, но и в моче с целью своевременного выявления подагры.
Содержание мочевой кислоты в крови может повышаться под влиянием различных факторов, как внутренних, так и внешних. Эти факторы способствуют либо увеличению образования эндогенных пуринов, либо замедлению их выделения почками. С этих позиций выделяют два типа гиперурикемии — метаболический и почечный. Метаболический тип характеризуется повышением синтеза эндогенных пуринов при наличии высокой урикозурии и нормальном клиренсе мочевой кислоты. Напротив, при почечном типе наблюдается низкий клиренс мочевой кислоты и, следовательно, нарушение выделения мочевой кислоты почками. Представленные типы гиперурикемии имеют первостепенное значение в выборе противоподагрических модифицирующих болезнь препаратов, используемых в терапии этого заболевания.
Причины повышенного биосинтеза пуринов
Нозологические формы и клинические синдромы:
Лекарства, диета и хронические интоксикации:
Причины замедления выведения мочевой кислоты почками
Нозологические формы и клинические синдромы:
Лекарства и хронические интоксикации:
Выделяют также первичную и вторичную подагру. При первичной подагре какое-либо фоновое заболевание, предшествующее ее развитию, отсутствует. В основе такой подагры лежит семейно-генетическая аномалия пуринового обмена, детерминированная несколькими генами, или так называемый «конституциональный диспуризм». Исследования уратного гомеостаза показали аутосомно-доминантный тип наследования таких аномалий. В частности, это наблюдается при врожденных нарушениях в содержании энзимов, занимающих ключевое положение в метаболизме пуринов. Так, при снижении активности гипоксантин-гуанин-фосфорибозилтрансферазы происходит увеличение ресинтеза пуринов из нуклеотидов, что способствует развитию синдрома Леша-Найхана. Этот синдром встречается только у детей и у лиц молодого возраста и обычно заканчивается уратной нефропатией с летальным исходом. При высоком содержании фосфорибозилпирофосфата также наблюдается метаболический тип гиперурикемии, так как этот фермент участвует в синтезе предшественников мочевой кислоты. Что касается вторичной подагры, то она является одним из синдромов другого заболевания, «второй болезнью», развивающейся при многих патологических процессах и чаще всего при хронической почечной недостаточности.
Большое значение в распознавании подагры, особенно ее ранней стадии, имеет клиническая картина острого подагрического артрита. Она хорошо известна, однако частота диагностических ошибок в первый год заболевания достигает 90%, а через 5–7 лет правильный диагноз ставится только в половине случаев. Поздняя диагностика связана с недооценкой классических ранних признаков заболевания, а также с многообразием дебюта и течения подагры. Ее диагностика строится на особенностях клинической картины заболевания, повышенного содержания мочевой кислоты в крови и обнаружения кристаллов урата натрия в тканях. На практике широко применяются следующие так называемые Римские диагностические критерии подагры:
Диагноз подагры считается достоверным при наличии любых двух из четырех критериев.
Менее распространены диагностические критерии подагры, предложенные Американской коллегией ревматологов (АСК) в 1977 г., которые скорее характеризуют острый воспалительный артрит или его рецидивирующие атаки, нежели подагру в целом. Согласно этим критериям, достоверный диагноз ставится при наличии 6 из 12 признаков:
В первые 3–4 года подагра протекает по типу рецидивирующего острого воспалительного моноартрита с полным обратным развитием и восстановлением функции суставов, при этом межприступный период продолжается от нескольких месяцев до 1–2 лет. В дальнейшем этот период укорачивается, в процесс вовлекаются все новые и новые суставы и воспалительные явления локализуются не только в суставах стоп, но распространяются на суставы верхних конечностей, что обычно совпадает с образованием тофусов. Тофусы представляют собой депозиты кристаллов мочевой кислоты. Они появляются в среднем спустя 6 лет после первого приступа подагры, но иногда и через 2–3 года. Ураты чаще всего откладываются на поверхности суставного хряща, в синовиальной оболочке, синовиальных влагалищах, сухожилиях, а также в субкортикальной области эпифизов костей. Наиболее часто они располагаются на ушных раковинах и на задней поверхности локтевых суставов. Тофусы подразделяются на единичные и множественные, а также классифицируются в соответствии с их размерами, при этом к мелким относят тофусы до 1 см в диаметре, к средним — от 1 до 2,5 см и к крупным — более 2,5 см. Подагрические узлы с локализацией в опорно-двигательном аппарате являются основным элементом формирования хронического подагрического артрита. Тофусы могут располагаться в почках и других висцеральных органах.
Хроническое течение подагры не ограничивается только вовлеченностью суставов и формированием тофусов, но и характеризуется поражением внутренних органов. Подагрическая нефропатия является наиболее важным с прогностической точки зрения проявлением подагры и самой распространенной причиной летальных исходов при этом заболевании. Среди отдельных вариантов подагрической нефропатии выделяют острую мочекислую блокаду канальцев почек, мочекислый нефролитиаз, обусловленный отложением солей мочевой кислоты в чашечках и лоханках почек, хроническую уратную нефропатию и диффузный гломерулонефрит. Острая мочекислая блокада канальцев почек происходит, например, при распаде опухоли вследствие массивной медикаментозной или рентгенотерапии. Хроническая уратная нефропатия связана с отложением уратов в интерстиции почек, а развитие диффузного гломерулонефрита — с иммунными нарушениями у лиц с дисрегуляцией пуринового обмена. Такой гломерулонефрит по своей иммуноморфологии чаще всего является мезангиопролиферативным и при нем выявляют депозиты IgG и комплемента. Следует иметь в виду, что подагра часто ассоциируется с такими патологическими состояниями, как артериальная гипертония, ожирение, гиперлипидемия, жировая дистрофия печени, атеросклероз, нарушения мозгового кровообращения, алкогольная зависимость.
Течение подагры характеризуется разнообразием темпов развития болезни. Возможно относительно доброкачественное течение с редкими приступами, небольшой гиперурикемией и урикозурией и длительным сохранением функциональной недостаточности опорно-двигательного аппарата. В других случаях, напротив, с самого начала заболевания наблюдаются частые атаки острого артрита с сильными болями или непрерывные атаки с множественным поражением суставов на протяжении нескольких недель или месяцев (подагрический статус). Рефрактерное к проводимой терапии течение подагры приводит к быстрому развитию функциональной недостаточности суставов и почек.
В основе выделения вариантов течения подагры лежат: количество приступов артрита в течение года, число пораженных суставов, выраженность костно-хрящевой деструкции, наличие тофусов, патология почек и ее характер.
Варианты течения подагры
Легкое: приступы артрита 1–2 раза в год и захватывают не более 2 суставов, нет поражения почек и деструкции суставов, тофусы отсутствуют или они единичные и не превышают 1 см в диаметре.
Средней тяжести: 3–5 приступов в год, поражение 2–4 суставов, умеренно выраженная костно-суставная деструкция, множественные мелкие тофусы, поражение почек ограничено почечно-каменной болезнью.
Тяжелое: частота приступов более 5 в год, множественное поражение суставов, множественные тофусы крупных размеров, выраженная нефропатия.
Основными задачами терапии подагрического артрита являются:
Купирование острого подагрического артрита проводится противовоспалительными средствами. Для этих целей используются: колхицин — колхицин, колхикум-дисперт; нестероидные противовоспалительные препараты (НПВП) — вольтарен, дикловит, диклоран, целебрекс, мовалис); кортикостероиды — полькортолон, преднизолон, метилпреднизолон; или комбинация НПВП и кортикостероидов — амбене. Как колхицин, так и НПВП способствуют обратному развитию острого артрита в течение нескольких часов, в то время как у не прошедших лечение больных он может длиться несколько недель. До недавнего времени полагали, что лучшим препаратом для купирования приступа острого артрита при подагре является колхицин. Ярко выраженный и быстрый (в течение 48 ч) эффект колхицина рассматривался как один из диагностических признаков этого заболевания. Колхицин способен предупредить дальнейшее развитие острого приступа подагры при его назначении в первые 30–60 мин атаки. Его лечебное действие обусловлено угнетением фагоцитарной активности нейтрофилов. При остром приступе подагры мононатриевые соли уратов, фагоцитированные нейтрофилами, приводят вследствие мембранолитического их действия к гибели этих клеток и высвобождению лизосомальных ферментов, которые отвечают за развитие острого воспаления.
Из НПВП предпочтение отдают индометацину (индотард, метиндол) и диклофенаку (вольтарен, диклоран, диклофен). Эти препараты назначают в дозе 200–250 мг/сут, причем в первые часы приступа применяют большую часть суточной дозы. Проведенные контролированные исследования не выявили более высокой эффективности традиционных НПВП по сравнению с селективными ингибиторами ЦОГ-2 (нимесил, нимулид, целебрекс), например целекоксибами (коксиб, целебрекс). Однако окончательное суждение о сравнительной эффективности этих препаратов можно вынести только в ходе дальнейших исследований. Суточная доза колхицина составляет 4–6 мг/сут, причем 2/3 этой дозы больной принимает до 12 ч дня в первый день приступа. Обычно разовая доза составляет 0,6 мг и ее принимают каждый час до явного снижения подагрического воспаления. После значительного уменьшения воспаления дозу колхицина начинают снижать по 0,6 мг 2 раза в день, вплоть до полной отмены. Нередко у больных не удается наращивать суточную дозу до оптимальной из-за появления побочных реакций. Основными побочными эффектами колхицина являются тошнота, рвота, понос, возможны также геморрагический гастроэнтерит, лейкопения, нейропатия. При подагрическом статусе, характеризующемся непрерывными атаками острого артрита, рефрактерными к терапии НПВП, возможно внутривенное введение колхицина.
Противоподагрическая терапия (базисная, модифицирующая болезнь) направлена на профилактику рецидивов острого артрита, снижение содержания мочевой кислоты в крови, предупреждение дальнейшего формирования тофусов и их обратное развитие. Все противоподагрические препараты делятся на две большие группы: урикодепрессоры (урикостатики) и урикозурики. Урикодепрессоры тормозят синтез мочевой кислоты путем ингибирования фермента ксантиноксидазы, превращающего гипоксантин в ксантин, а ксантин в мочевую кислоту. Урикозурики повышают экскрецию мочевой кислоты, подавляя обратную реабсорбцию уратов почечными канальцами.
К препаратам первой группы относится аллопуринол (аллопуринол, аллопуринол-эгис, аллупол, пуринол, ремид, тиопуринол, милурит), который занимает лидирующее положение среди дру-гих противоподагрических средств. Показанием к применению аллопуринола являются метаболическая подагра, высокая гиперурикемия, частые острые атаки артрита, мочекислая болезнь, генетически обусловленный дефицит гипоксантин-гуанин-фосфорибозилтрансферазы. Применение аллопуринола возможно и у больных с подагрической нефропатией с начальными проявлениями хронической почечной недостаточности и небольшой азотемии. Начальная доза аллопуринола составляет 300 мг/сут. В случае неэффективности такой дозы ее увеличивают до 400–600 мг/сут, а при достижении клинического эффекта постепенно снижают. Поддерживающая доза определяется уровнем гиперурикемии и обычно составляет 100–300 мг/сут.
Аллопуринол способствует исчезновению атак острого артрита или их заметному ослаблению, обратному развитию тофусов и отчетливому их размягчению, снижению уровня мочевой кислоты до субнормальных цифр, нормализации показателей мочевого синдрома, урежению почечных колик и выделительной функции почек. У некоторых больных он поначалу вызывает повышение уровня мочевой кислоты и обострение подагрического артрита, поэтому на первом этапе терапии его комбинируют с противовоспалительными препаратами, в частности с низкими дозами колхицина или НПВП. По этой причине его не следует принимать при остром подагрическом артрите. При лечении аллопуринолом нередко развиваются побочные реакции, которые проявляются желудочно-кишечной токсичностью, аллергическими реакциями (кожная сыпь, эозинофилия), гепатотоксичностью с повышением сывороточных аминотрансфераз.
Урикозурические препараты, представляющие собой слабые органические кислоты, имеют меньшее значение в терапии подагры, чем урикостатики. Их не следует назначать при высоком содержании мочевой кислоты в крови, а также при нефропатии даже с начальными проявлениями почечной недостаточности. Из урикозурических препаратов сульфинпиразон и пробенецид особенно широко используются в США. Сульфинпиразон (сульфинпиразон, апо-сульфинпиразон, антуран) назначают по 200–400 мг/сут в два приема. Его, как и другие урикозурические средства, принимают с большим количеством жидкости, которую для профилактики нефролитиаза следует ощелачивать. Побочные реакции встречаются относительно часто и проявляются желудочной и кишечной диспепсией, лейкопенией, аллергическими реакциями. Противопоказанием к назначению сульфинпиразона является язвенная болезнь желудка и, конечно, подагрическая нефропатия.
Пробенецид (бенемид) является производным бензойной кислоты. Препарат назначается по 1,5–2,0 г/сут. Бензойная кислота содержится в клюкве, а также в ягодах и листьях брусники. Поэтому отвары и морсы из ягод и листьев этих растений показаны больным подагрой и в большей степени больным с подагрической нефропатией, тем более что помимо бензойной кислоты они содержат гиппуровую кислоту, обладающую урикосептическими свойствами. Урикозурическая активность присуща блокатору рецептора ангиотензина II и фенофибрату (грофибрат, нофибал). Наиболее эффективны производные бензбромарона, которые обладают не только урикозурическими свойствами, но и урикодепрессорными. Они используются в качестве монотерапии или в сочетании с аллопуринолом. Таким комбинированным препаратом является алломарон. Алломарон содержит 20 мг бензбромарона и 100 мг аллопуринола, его обычно принимают по 1 таблетке 2 раза в день.
Составной частью комплексной терапии подагры являются ощелачивающие препараты и ощелачивающие растворы, которые способны снизить риск развития нефропатии и, в частности, мочекаменной болезни. К этим препаратам относятся магурлит, блемарен и уралит. Их применение должно регулярно контролироваться показателем рН мочи. Помимо этих средств, можно принимать питьевую соду 2–4 г в день или щелочные минеральные воды.
При выраженных симптомах артрита необходимо также проводить местное лечение (долобене, финалгон, диклоран плюс, долгит крем, немулид гель, бишофит-гель).
Диете при подагре придают наибольшее значение по сравнению с другими ревматическими болезнями. Она предусматривает снижение общего калоража пищи, тем более что при подагре обычно наблюдается повышенная масса тела. Необходимо уменьшить поступление в организм экзогенных пуринов и животных жиров. Жиры снижают экскрецию мочевой кислоты почками. Крайне осторожно следует подходить к употреблению любых алкогольных напитков, включая пиво и красное вино. Исключают из пищевого рациона печенку, почки, жирные сорта мяса, мясные бульоны, копчености, горох, бобы, чечевицу, шпинат, цветную капусту, шпроты, сельдь. Следует ограничить потребление мяса до 2–3 раз в неделю, при этом лучше употреблять его в отварном виде.
Сочетание строгой диеты с длительным применением противоподагрических препаратов, а также активное воздействие на заболевания, которые повышают содержание мочевой кислоты в крови, способны существенно замедлить темпы прогрессирования костно-хрящевой деструкции, предупредить дальнейшее формирование тофусов и сохранить функциональное состояние опорно-двигательного аппарата и почек.
В. В. Бадокин, доктор медицинских наук, профессор
РМАПО, Москва